-
在离子RO3n-中共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的质子数目是
A.A–x+n+48 B.A–x+n+24 C.x-n-24 D.x+n-24
难度: 简单查看答案及解析
-
下列关于元素周期表的叙述中不正确的是( )
A.元素种类最多的族是第Ⅷ族
B.第ⅠA族金属元素单质均能与水反应
C.第ⅡA族中无非金属元素
D.金属元素的种类比非金属元素多
难度: 简单查看答案及解析
-
某反应由两步反应A→B→C构成,其反应能量量变化曲线如图所示,下列叙述正确的是( )
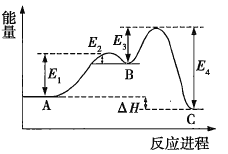
A.两步反应均为吸热反应 B.三种物质中C最稳定
C.A与C的能量差为
D.A→B的反应一定需要加热
难度: 简单查看答案及解析
-
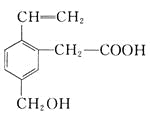
使0.5 mol乙烯与氯气发生加成反应,然后该加成产物与氯气在光照条件下发生取代反应,则两个过程中消耗氯气的总物质的量最多是
A.1.5 mol B.2.5 mol C.2.0 mol D.3.0 mol
难度: 简单查看答案及解析
-
反应C(s)+H2O(g)⇌CO(g)+H2(g)在一定密闭容器中进行,则下列说法或结论中,能够成立的是( )
A.其他条件不变仅将容器的体积缩小一半,反应速率减小
B.反应达平衡状态时:v(CO)正=v(H2O)(逆)
C.保持体积不变,充入少量He使体系压强增大反应速率一定增大
D.其他条件不变,适当增加C(s)的质量会使反应速率增大
难度: 简单查看答案及解析
-
短周期的三种元素X、Y、Z位于同一周期,其最高价氧化物对应的水化物的酸性由强到弱的顺序是:HXO4 >H2YO4>H3ZO4,则下列判断正确的是
A.非金属性:X>Y>Z B.原子半径:X>Y>Z
C.原子的最外层电子数:X<Y<Z D.气态氢化物的稳定性:X<Y<Z
难度: 中等查看答案及解析
-
我国科学家发明的一种可控锂水电池的工作原理如图所示。下列有关说法不正确的是( )
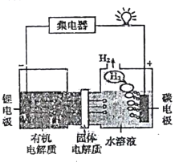
A.电池工作时,锂离子向正极移动 B.电池总反应为
C.有机电解质可用水溶液代替 D.该装置不仅可提供电能,还可得到清洁的氢气
难度: 中等查看答案及解析