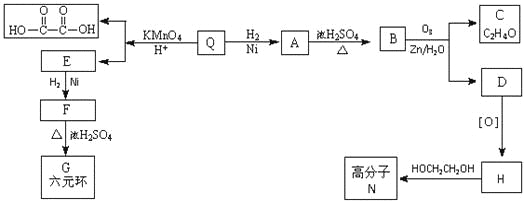
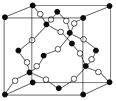
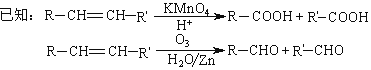-
下列现象中,其原因与氢键存在无关的是( )
A.水的熔沸点比H2S高
B.HCl的熔沸点比HI低
C.NH3极易溶于水
D.邻位羟基苯甲醛的沸点比对位羟基苯甲醛沸点低
难度: 简单查看答案及解析
-
下列说法中,错误的是( )
A.无论是乙烯的加成反应还是乙烯使酸性KMnO4溶液褪色,都与乙烯分子内含有的碳碳双键有关
B.使用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.使用溴的四氯化碳溶液或酸性KMnO4溶液都可以除去乙烷中混有的乙烯
D.乙烯的化学性质比乙烷的化学性质活泼
难度: 中等查看答案及解析
-
解释下列物质性质的变化规律与物质结构间的因果关系时,与键能无关的变化规律是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱
B.H2O在高温下也难分解
C.金刚石、SiC、晶体Si的熔点依次减低
D.F2、Cl2、Br2、I2的熔沸点逐渐升高
难度: 中等查看答案及解析
-
下列关于CH4和CO2的说法正确的是( )
A.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
B.CH4分子中含有极性共价键,是极性分子
C.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp2
D.固态CO2属于分子晶体
难度: 中等查看答案及解析
-
科学家艾哈迈德·泽维尔使“运用激光技术观察化学反应时分子中原子的运动”成为可能,在他的研究中证实了光可诱发下列变化:

这一事实可用于解释人眼的夜视功能,有关X、Y的叙述不正确的是( )
A.X和Y为同一种物质 B.X和Y与氢气加成后生成同一种物质
C.X和Y都可以发生加聚反应 D.X和Y物理性质有差异
难度: 中等查看答案及解析
-
下列说法正确的是( )
①NH3的熔、沸点比VA族其他元素氢化物的都高②多元醇比一元醇在水中溶解度大③冰的密度比液态水的密度小④尿素(CO(NH2)2)的熔、沸点比醋酸的高⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低⑥水分子稳定是因为水分子间存在氢键
A.①②③④⑤⑥
B.②③④⑤
C.①②③④
D.①②③
难度: 困难查看答案及解析
-
下列说法中正确的是( )
A.金刚石晶体中的最小碳原子环由12个碳原子构成
B.AlCl3晶体属于分子晶体
C.1molSiO2分子中含4molSi—O键
D.金刚石化学性质稳定,即使在高温下也不会和O2反应
难度: 简单查看答案及解析
-
下列结论中正确的是( )
A.氢化物的沸点顺序是HF>H2O>NH3
B.ⅤA族元素氢化物沸点顺序AsH3>PH3>NH3
C.过氧化钠和氧化纳中阴离子与阳离子个数比都是1:2
D.干冰(CO2)和SiO2属于同主族非金属氧化物,所以物理性质相同
难度: 简单查看答案及解析
-
对于苯乙烯的下列叙述:①能使酸性KMnO4溶液褪色②可发生加聚反应③可溶于水④可溶于苯中⑤苯环能与溴水发生取代反应⑥所有的原子可能共面。其中完全正确的是( )
A.①②④⑥
B.①②④⑤⑥
C.①②③④
D.①②③④⑤⑥
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A.CS2、SO3都是极性键构成的非极性分子
B.在[Co(NH3)4Cl2]+中存在配位键且配位数是4
C.元素第一电离能越大的原子,非金属性越强
D.每个干冰的晶胞中占有14个CO2分子
难度: 简单查看答案及解析
-
关于下列有机化合物的说法正确的是( )
A.溴乙烷和乙烷都是饱和烃
B.甲烷和甲苯都可以与氯气反应
C.高锰酸钾可以氧化苯和甲烷
D.乙烯可以与氢气发生加成反应,苯不能与氢气加成
难度: 简单查看答案及解析
-
关于卤代烃RCH2CH2X性质叙述中,下列说法正确的是( )
A.发生水解反应的条件是强碱的醇溶液、加热
B.可以直接加硝酸银溶液检验卤素原子类型
C.发生消去反应生成烯烃
D.该卤代烃易溶于水
难度: 简单查看答案及解析
-
下列关于晶体的说法不正确的是( )
A.晶体尽可能采取紧密堆积方式,以使其变得比较稳定
B.晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
C.12g金刚石晶体和12g石墨晶体含有的C—C键数目之比为4:3
D.相同质量的乙酸和甲酸甲酯的化学键数目都是8NA
难度: 简单查看答案及解析
-
用分子式C8H10O所表示的某类化合物具有苯环,并且和FeCl3溶液发生反应且溶液显紫色,这种化合物的同分异构体有( )
A.9种
B.10种
C.11种
D.12种
难度: 中等查看答案及解析
-
下列关于化学键的叙述,正确的一项是
A.离子化合物中一定含有离子键
B.单质分子中均存在化学键
C.含有极性键的分子一定是极性分子
D.含有共价键的化合物一定是共价化合物
难度: 简单查看答案及解析
-
下列说法正确的是(NA为阿伏加德罗常数)( )
A.124gP4含有P—P键的个数为6NA
B.24g石墨中含有六元环个数为3NA
C.46g乙醇中含有极性键的个数为6NA
D.18g冰中含氢键的个数为4NA
难度: 中等查看答案及解析
-
下列各组微粒的空间构型和中心原子杂化方式均相同的是( )
①NH3和H2O②NH4+和H3O+③NH3和H3O+④O3和SO2⑤CO2和BeCl2⑥CO32-和SO42-⑦BF3和Al2Cl6
A.全部
B.④⑥⑦
C.③④⑤
D.②⑤⑥
难度: 简单查看答案及解析
-
下列描述中不正确的是( )
A.AsH3空间构型为三角锥形
B.SiO2为V形的极性分子
C.S2Cl2所有原子均满足8电子结构
D.SiF4和SO42-的中心原子均为sp3杂化
难度: 简单查看答案及解析
-
下列有关物质的表达式正确的是( )
A.乙炔分子的比例模型:
B.溴乙烷的电子式:
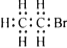
C.2-氯丙烷的结构简式: CH3CHClCH3 D.丙烯的键线式:
难度: 中等查看答案及解析
-
具有下列电子层结构或性质的原子:①2p轨道上有2对成对电子的原子;②外围电子构型为2s22p3的原子;③短周期第一电离能最小;④第三周期离子半径最小。则下列有关比较中正确的是( )
A.第一电离能:②>③>①>④
B.原子半径:④>③>②>①
C.电负性:①>②>④>③
D.最高正化合价:②>③>①>④
难度: 中等查看答案及解析