-
X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z原子的最外层电子数是内层电子总数的3倍。下列有关叙述正确的是( )
A.Y原子的价层电子排布式为3s23p5
B.稳定性:Y的氢化物>Z的氢化物
C.第一电离能:Y<Z
D.X、Y两元素形成的化合物为离子化合物
难度: 中等查看答案及解析
-
化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列有关说法正确的是
A.该合成中所有的电能和热能全部转化为化学能
B.该合成氨过程不属于氮的固定
C.空气、水、太阳能均为可再生资源
D.断裂N2中的N≡N键会释放出能量
难度: 中等查看答案及解析
-
下面的排序不正确的是( )
A. 晶体熔点由低到高:F2<Cl2<Br2<I2
B. 熔点由高到低: Na>Mg>Al
C. 硬度由大到小: 金刚石>碳化硅>晶体硅
D. 晶格能由大到小: MgO>CaO>NaF> NaCl
难度: 中等查看答案及解析
-
下列关于杂化轨道的叙述正确的是( )
A. 杂化轨道可用于形成σ键,也可用于形成π键
B. 杂化轨道可用来容纳未参与成键的孤电子对
C. NH3中N原子的sp3杂化轨道是由N原子的3个p轨道与H原子的s轨道杂化而成的
D. 在乙烯分子中,1个碳原子的3个sp2杂化轨道与3个氢原子的s轨道重叠形成3个C—H σ键
难度: 简单查看答案及解析
-
某烷烃的结构简式为
,它的正确命名是( )
A. 4-甲基-3-乙基戊烷 B. 3-丙基戊烷
C. 2-甲基-3-乙基戊烷 D. 3-乙基-2-甲基戊烷
难度: 中等查看答案及解析
-
乙二酸,又称草酸,通常在空气中易被氧化而变质。其两分子结晶水(H2C2O4·2H2O)却能在空气中稳定存在。在分析化学中常用H2C2O4•2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是
A.草酸是二元弱酸,其电离方程式为H2C2O4═2H++C2O42−
B.草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂
C.乙二酸可通过乙烯经过加成、水解、氧化再氧化制得
D.将浓H2SO4滴加到乙二酸上使之脱水分解,分解产物是CO2和H2O
难度: 中等查看答案及解析
-
如图所示是探究发生腐蚀的装置图。发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升。下列说法不正确的是
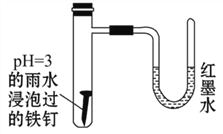
A.两种腐蚀负极的电极反应式均为Fe-2e-=Fe2+
B.开始时发生的是析氢腐蚀
C.一段时间后发生的是吸氧腐蚀
D.析氢反应的总反应式为2Fe+O2+2H2O=2Fe(OH)2
难度: 简单查看答案及解析
-
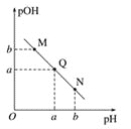
常温下,浓度均为0.1 mol·L-1、体积均为100 mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg[c(H+)/c(OH-)]随加入NaOH的物质的量的变化如图所示。下列叙述正确的是( )

A.HX的酸性弱于HY B.c点溶液中:c(Y-)>c(HY)
C.a点由水电离出的c(H+)=10-12 mol·L-1 D.b点时酸碱恰好完全中和
难度: 困难查看答案及解析
 2NH3(g) △H,该反应的能量变化如图所示:
2NH3(g) △H,该反应的能量变化如图所示: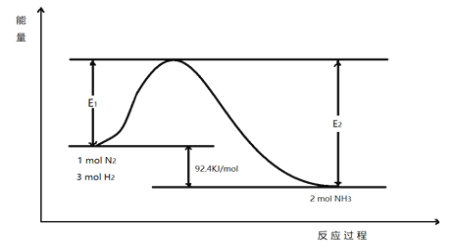
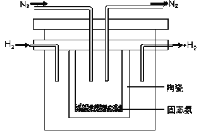
 的说法正确的有______(双选,填字母);
的说法正确的有______(双选,填字母);