-
古文中蕴含着十分丰富的化学道理。下列语句中涉及化学变化的是:
A.白玉为床,金作马 B.挹苦泉水熬之则成胆矾,烹胆矾则成铜
C.疏影横斜水清浅,暗香浮动月黄昏 D.千里冰封,万里雪飘
难度: 简单查看答案及解析
-
C2H4O2的有机酸与分子式为C3H7OCl的化合物发生酯化反应,生成酯的同分异构体有(不考虑立体异构):
A.5种 B.6种 C.7种 D.8种
难度: 中等查看答案及解析
-
下列说法正确的是:
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.甲苯与氯气在光照条件下反应主要生成2,4,6—三氯甲苯
C.通过红外光谱分析可以区分乙醇和乙酸乙酯
D.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的数值。下列有关叙述正确的是:
A.标准状况下,22.4 LCC14中所含C—Cl键的数目为4NA
B.在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA
C.向密闭容器中充入1 mol N2O4,加热使之充分分解,生成 NO2的分子数为2NA
D.7.8g Na2O2中所含的阴离子数目为0.1NA
难度: 中等查看答案及解析
-
A、B、C、D四种短周期元素,其原子半径及最高正化合价如下表所示,C与D两原子的电子层数相同,下列说法正确的是:
A
B
C
D
原子半径(nm)
0.053
0.077
0.102
0.186
最高正化合价
+1
+4
+6
+1
A.BC2分子呈折线型 B.B与C形成氢化物的稳定性B<C
C.D2C的水溶液显酸性 D.这四种元素的单质分别在氧气中燃烧,对应的产物只有一种
难度: 中等查看答案及解析
-
电解原理在化学工业中有广泛应用。图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。下列说法不正确的是:
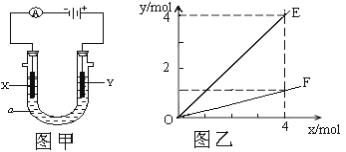
A.若此装置用于电镀铜,则Y为铜电极,电解液a可以是硫酸铜或氯化铜溶液。
B.按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量。
C.若X、Y为铂电极,a溶液为250mL CuSO4和KNO3的混合液,经过一段时间后,两极均得到标准状况下5.6L气体,则原混合液中CuSO4的物质的量浓度为1mol·L-1
D.按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.1mol的氧化铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为0.4mol。
难度: 中等查看答案及解析
-
25℃时,将浓度均为0.1mol/L,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是( )
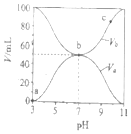
A.Ka(HA)=1×10-6mol/L
B.b点c(B+)=c(A-)=c(OH-)=c(H+)
C.c点时,
随温度升高而减小
D.a→c过程中水的电离程度始终增大
难度: 中等查看答案及解析
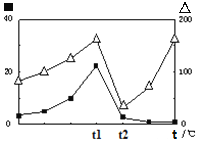 (∆代表CO的生成速率,■代表催化剂的催化效率)
(∆代表CO的生成速率,■代表催化剂的催化效率)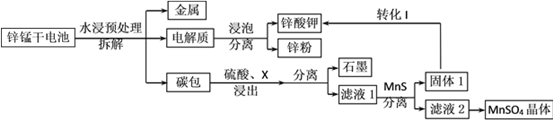
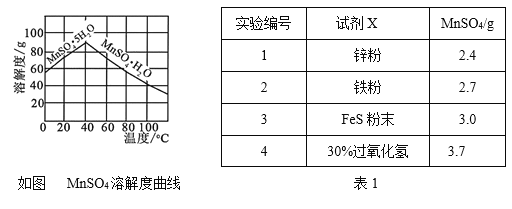
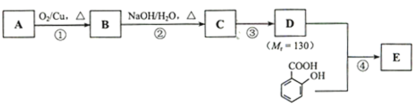
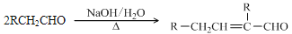 。水杨酸酯E为紫外线吸收剂,可用于配制防晒霜。E的一种合成路线如下:
。水杨酸酯E为紫外线吸收剂,可用于配制防晒霜。E的一种合成路线如下: