-
下列说法正确的是
A. 聚乙烯、蛋白质、淀粉和油脂都是有机高分子化合物
B. 能与NaHCO3溶液反应的有机物C5H10O2有4种
C. 利用乙醇的可燃性可检查司机是否酒后驾车
D. 石蜡油分解的产物均能使溴的四氯化碳溶液褪色
难度: 中等查看答案及解析
-
W、X、Y、Z均为短周期主族元素,原子序数依次增大,W是周期表中原子半径最小的原子,X与Y形成的某种化合物能与水发生氧化还原反应,且生成酸,W、X、Y三种元素的核电荷数之和等于Z的原子序数,则下列说法正确的是
A.原子半径:X>Y>Z>W
B.W和X形成的某种化合物中,可能既有离子键,又有共价键
C.单质的氧化性:Y<Z
D.简单氢化物的稳定性:X<Y<Z
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.乙醇的酯化反应和酯的水解反应均属于取代反应
B.乙烯能使酸性高锰酸钾溶液褪色,是因为乙烯分子中含有碳碳双键
C.乙醛分子式为C2H4O2它可以还原生成乙醇
D.苯与溴水混合,反复振荡后溴水层颜色变浅是因为苯与溴水发生了加成反应
难度: 简单查看答案及解析
-
已知:H2(g)+Cl2(g)
2HCl(g)反应的能量变化示意图如下:
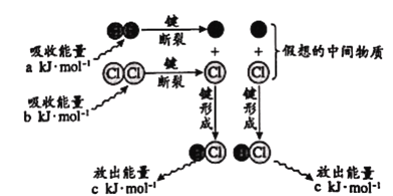
下列说法正确的是
A. 点燃条件和光照条件下,反应的ΔH不同
B. 反应的ΔH约为[2c- (a+b)]kJ·mol-1
C. “假想的中间物质”的总能量低于起始态H2和Cl2的总能量
D. 反应涉及的物质中,既有含极性键的物质,也有含非极性键的物质
难度: 中等查看答案及解析
-
已知:原子序数小于18的同一主族的两种元素X和Y,其原子半径:X<Y。下列说法正确的是( )
A.若X和Y均位于VIIA,则键能大小为HX<HY
B.若X和Y均位于VIA,则H2X分子间易形成氢键
C.若X和Y均位于IVA,则半径Y<X
D.若X和Y均位于IIA,则第一电离能大小为X<Y
难度: 中等查看答案及解析
-
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中不正确的是

A.该能量转化系统中的水也是可能循环的
B.燃料电池系统产生的能量实际上来自于水
C.水电解系统中的阳极有
放出
D.燃料电池放电时的负极反应:
难度: 中等查看答案及解析
-
用NaOH溶液吸收烟气中的SO2,将所得的吸收液用三室膜电解技术处理,原理如图所示.下列说法错误的是
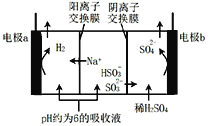
A.电极a为电解池阴极
B.阳极上有反应HSO3—-2e—+H2O=SO42—+3H+发生
C.当电路中通过1mol电子的电量时,理论上将产生0.5mol H2
D.处理后可得到较浓的H2SO4和NaHSO3产品
难度: 中等查看答案及解析
 2CO2(g)+N2(g)△H<0
2CO2(g)+N2(g)△H<0