-
空气中体积分数约为21%的气体是
A.氧气 B.氮气 C.二氧化碳 D.水蒸气
难度: 简单查看答案及解析
-
下列变化属于物理变化的是( )
A.玻璃破碎
B.牛奶变酸
C.蜡烛燃烧
D.铁锅生锈
难度: 简单查看答案及解析
-
下列食物中,富含糖类的是( )
A.大豆
B.玉米
C.萝卜
D.牛油
难度: 简单查看答案及解析
-
下列生活用品所含的主要材料,属于有机合成材料的是( )
A.
 纯羊毛衫
纯羊毛衫B.
 钛合金表链
钛合金表链C.
 塑料桶
塑料桶D.
 钛合金壶
钛合金壶难度: 简单查看答案及解析
-
下列化肥中,属于复合肥的是( )
A.KNO3
B.NH4Cl
C.Ca(H2PO4)2
D.K2CO3
难度: 简单查看答案及解析
-
“保护环境人人有责”,下列做法正确的是( )
A.用过的医用口罩回收利用
B.塑料垃圾就地焚烧
C.生活垃圾分类摆放
D.工业废水直接排放
难度: 简单查看答案及解析
-
晴天衣服容易晒干,原因是( )
A.水分子的质量很小
B.水分子之间有间隔
C.温度越高,水分子运动越快
D.水分子的体积变大
难度: 简单查看答案及解析
-
一些物质的pH范围如下,其中显碱性的是( )
A.食醋(2~3)
B.牙膏(8~9)
C.西瓜汁(5-6)
D.橘子汁(3~4)
难度: 简单查看答案及解析
-
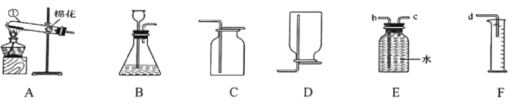
下列实验基本操作中正确的是()
A.
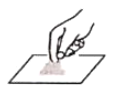 取用固体
取用固体B.
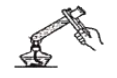 加热液体
加热液体C.
 测溶液的pH
测溶液的pHD.
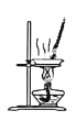 蒸发溶液
蒸发溶液难度: 简单查看答案及解析
-
下列少量物质分别放入水中,充分搅拌,不能形成溶液的是( )
A.汽油
B.氯化氢
C.酒精
D.冰糖
难度: 简单查看答案及解析
-
84消毒液是一种以次氯酸钠(NaClO)为主的高效消毒剂,次氯酸钠中氯元素的化合价为()
A.-1
B.+1
C.+3
D.+5
难度: 简单查看答案及解析
-
下图是钇元素在元素周期表中的信息和氧离子结构示意图。下列说法正确的是( )
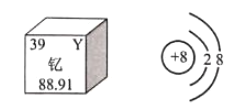
A.钇原子中的质子数为88.91
B.钇原子中的中子数为39
C.氧离子的符号为O2+
D.氧离子已达到相对稳定结构
难度: 简单查看答案及解析
-
根据化学实验常识,下列做法正确的是( )
A.进入地窖前,先进行灯火实验
B.森林起火,应快速顺风逃跑
C.楼房着火,可乘坐电梯逃离
D.浓硫酸不慎溅到皮肤上,要立即用氢氧化钠溶液清洗
难度: 简单查看答案及解析
-
下列实验现象描述正确的是( )
A.碳在氧气中燃烧发出白光,生成黑色固体
B.镁在空气中燃烧发出耀眼的白光,生成氧化镁
C.生锈的铁钉放入稀盐酸中,溶液变为黄色
D.氢氧化钠溶液中滴加石蕊溶液,溶液变为红色
难度: 简单查看答案及解析
-
下图是某化学变化的微观示意图,X、Y、Z分别表示不同类别的原子,下列有关该反应的说法不正确的是( )
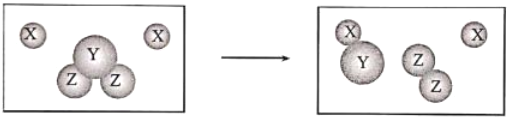
A.该反应属于置换反应
B.该化学反应中生成物的粒子个数比为1: 1: 1
C.X原子可以直接构成物质
D.反应前后原子的种类、数目不变
难度: 简单查看答案及解析
-
阿司匹林(化学式为C9H8O4)是一种历史悠久的解热镇痛药。下列关于阿司匹林的说法不正确的是( )
A.阿司匹林由碳、氢、氧三种元素组成
B.阿司匹林中碳元素的质量分数最大
C.阿司匹林中碳、氢、氧元素的质量比为9∶8∶4
D.1个阿司匹林分子由9个碳原子、8个氢原子、4个氧原子构成
难度: 简单查看答案及解析
-
在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如下图所示:
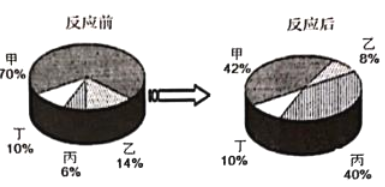
下列说法正确的是( )
A.丙可能是单质
B.该反应是化合反应
C.丁一定是该反应的催化剂
D.甲和乙两物质的化学计量数之比为14:3
难度: 中等查看答案及解析
-
下列实验方法能达到实验目的的是( )
选项
实验目的
实验方法
A
鉴别氢氧化钠和硝酸铵
加水后测温度变化
B
鉴别实验室里的食盐水和蔗糖水
品尝味道
C
除去CaO中的CaCO3
加入稀盐酸,过滤
D
除去NaCl溶液中的MgCl2
加入过量的NaOH溶液,过滤
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
硝酸钾和氯化钠的溶解度曲线如下图所示。30℃时,分别将30g硝酸钾和氯化钠放入100 g水中,充分溶解。下列结论中,不正确的是
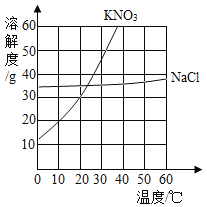
A.两种溶液中溶质的质量分数相等
B.通常情况下,采取降温的方法能将两种溶液都变成饱和溶液
C.若将硝酸钾溶液降温到20℃,溶液中溶质和溶剂的质量比为3∶10
D.若将硝酸钾溶液变为10℃时的饱和溶液,溶液中溶质的质量分数一定减小
难度: 中等查看答案及解析
-
下列说法不正确的说法有( )
①化学反应一定伴随着能量的变化
②有机物中含有碳元素,所以H2CO3、 C6H12O6都属于有机物
③实验室里用过氧化氢制氧气的反应中,硫酸铜溶液也能作该反应的催化剂
④向某溶液中滴加氯化钡溶液,产生白色沉淀,则该溶液中一定含有硫酸根离子
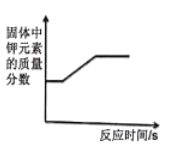
⑤加热一定质量的高锰酸钾,反应过程中钾元素在固体中的质量分数随时间的变化关系如右图所示
A.1种
B.2种
C.3种
D.4种
难度: 中等查看答案及解析