-
下列实验方案不可行的是( )
A.用熟石灰区分氯化铵和氯化钾
B.用水区分氯化钙和碳酸钙
C.用pH试纸区分澄清石灰水和食盐水
D.用酚酞溶液区分氯化钠溶液和盐酸
难度: 中等查看答案及解析
-
生活中处处有化学,化学与人体健康密切相关。下列说法正确的是
A.霉变的大米淘洗后可食用
B.食用新鲜蔬菜、水果可补充维生素
C.为延迟食品的保质期,可用甲醛作防腐剂
D.烹饪过程中,可用工业用盐(亚硝酸钠)作调味品
难度: 简单查看答案及解析
-
2019年世界环境日,我国提出了“蓝天保卫战,我是行动者”的主题。下列行为不符合这一活动主题的是( )
A.植树造林,增加绿地面积
B.提倡坐公共交通工具出行
C.生活垃圾分类科学处理
D.蔬菜大棚的塑料膜就地焚烧处理
难度: 简单查看答案及解析
-
清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图(图中的微粒恰好完全反应)。下列说法正确的是( )
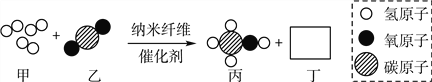
A. 丁的化学式为H2O,该反应为置换反应
B. 参加反应的甲与乙的质量比为3∶1
C. 甲是单质,乙、丙、丁均为氧化物
D. 该反应体现了无机物可以转化为有机物
难度: 中等查看答案及解析
-
某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )
①需称取氢氧化钠固体2.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量
④选用250mL量筒量取18mL的水
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A.
B.
C.
D.
难度: 中等查看答案及解析
-
食醋、纯碱、食盐均为家庭厨房中常用的物质,利用这些物质,不能完成的实验是( )
A.除去热水瓶中的水垢 B.鉴别氯化钙和硝酸钙
C.检验贝壳能否溶于酸 D.检验久置的烧碱是否变质
难度: 中等查看答案及解析
-
工业上,锻烧石灰石(主要成分是CaCO3)可制得生石灰(CaO),现有一包CaCO3和CaO的固体混合物。己知Ca元素与C元素的质量比是5∶l,则此混合物中Ca元素与O元素的质量比是( )
A.15∶16 B.15∶14 C.5∶4 D.15∶8
难度: 中等查看答案及解析
-
向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,反应过程中,测得混合物中溶液的质量与加入铁粉的质量关系如图所示。有关该反应过程中的下列说法正确的是
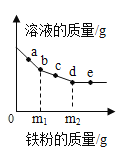
A. a点,向溶液中滴加稀盐酸,无白色沉淀
B. c点,向过滤后得到的固体中滴加稀盐酸,无气泡产生
C. d点,溶液中的溶质为Fe(NO3)2和Cu(NO3)2
D. e点,过滤后得到的固体中只含有2种物质
难度: 困难查看答案及解析
-
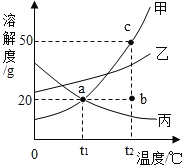
甲、乙两种物质的溶解度曲线如图所示。下列说法不正确的是( )
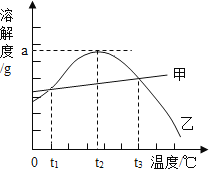
A.在t1℃、t3℃时甲、乙两物质的溶解度相等
B.在t1℃至t3℃之间,乙的溶解度大于甲的溶解度
C.将甲、乙的饱和溶液从t3℃降到t1℃,析出甲、乙的质量相等
D.将t2℃时接近饱和的乙溶液变为饱和溶液可采取升温或降温的方法
难度: 困难查看答案及解析
-
某材料只含金属镁和铝,课外小组为测定该材料中Mg的含量做了如下实验:取102g材料完全溶于盐酸得到溶液,将溶液分成两等份,向其中一份中逐渐加入NaOH固体,NaOH固体与溶液中产生沉淀的质量关系如图所示,则该材料中Mg的质量分数为( )
已知:
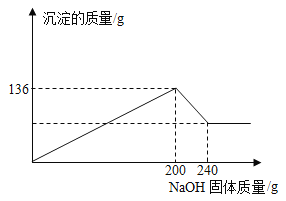
A.23.53% B.42.65% C.21.32% D.47.06%
难度: 困难查看答案及解析