-
化学与生活密切相关,下列说法正确的是( )
A.食品中的抗氧化剂对人体均无害且均具有氧化性
B.尼龙绳是由天然高分子化合物制成的,其强度很大
C.某雨水样品采集后放置一段时间,pH由4.68变为4.18,是因为水中溶解了较多CO2
D.蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极其微量的银离子,可杀死牛奶中的细菌,防止牛奶变质
难度: 简单查看答案及解析
-
自然界中的许多植物中含有醛,其中有些具有特殊香味,可作为植物香料使用,例如桂皮含肉桂醛(
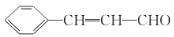 ),杏仁含苯甲醛(
),杏仁含苯甲醛()。则下列说法中错误的是( )
A.肉桂醛和苯甲醛互为同系物
B.苯甲醛分子中所有原子可能位于同一平面内
C.肉桂醛能发生加成反应、取代反应和加聚反应
D.与肉桂醛互为同分异构体且含相同官能团和苯环结构的共有4种(不考虑顺反异构)
难度: 中等查看答案及解析
-
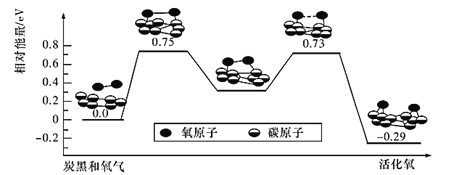
我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H将CO2高效还原为重要工业原料之一的甲醇,其反应机理如图所示。则下列有关说法不正确的是( )
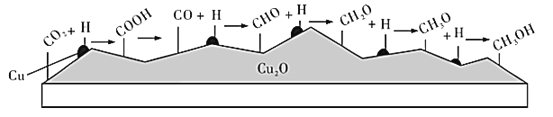
A.CO2生成甲醇是通过多步氧化反应实现的
B.该催化反应过程中涉及了化学键的形成及断裂
C.有可能通过调节控制反应条件获得甲醛等有机物
D.催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
难度: 中等查看答案及解析
-
中科院长春应化所张新波团队提出了一种独特的锂-氮电池(Li-N2),该电池在放电过程中消耗氮气,充电过程中释放氮气,实现氮气的循环,并对外提供电能。该电池在充电时发生反应:2Li3N
N2↑+6Li。现以该电池为电源进行如图所示实验,下列说法正确的是( )
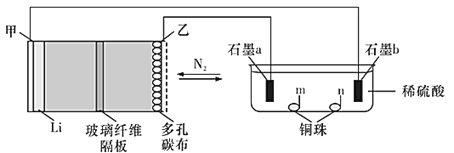
A.乙电极上的反应为2Li3N-6e-=N2↑+6Li+
B.充电过程中Li+由甲电极迁移向乙电极,并在多孔碳布表面生成Li3N
C.电极“石墨a”和m、n处均可能有铜析出
D.锂氮电池为绿色固氮提供了一种可能
难度: 中等查看答案及解析
-
已知:[FeCl4(H2O)2]-呈黄色,由下列实验所得结论不正确的是( )
①
②
③
④
0.1mol/L Fe2(SO4)3溶液
酸化的0.1mol/L Fe2(SO4)3溶液
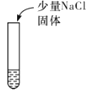
酸化的0.1mol/L Fe2(SO4)3溶液
0.1mol/L FeCl3溶液
加热前溶液为浅黄色,加热后颜色变深
加热前溶液接近无色,加热后溶液颜色无明显变化
加入NaCl后,溶液立即变为黄色,加热后溶液颜色加深
加热前溶液为黄色,加热后溶液颜色变深
注:加热为微热,忽略溶液体积变化。
A.实验①中,Fe2(SO4)3溶液显浅黄色的原因是Fe3+水解产生了少量Fe(OH)3
B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C.实验③中,存在平衡:Fe3+ +4Cl- +2H2O
[FeCl4(H2O)2]-
D.实验④中,可证明升高温度,Fe3+水解平衡一定正向发生移动
难度: 中等查看答案及解析
-
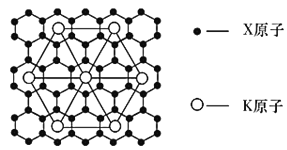
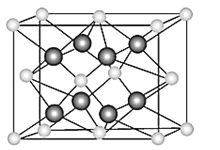
科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半,下列说法正确的是( )
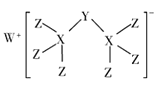
A.氧化物对应的水化物的酸性:Z> Y> X
B.元素X可与元素W形成化合物W2X,该化合物与水能产生可燃气体
C.该新化合物中Y不满足8电子稳定结构
D.Z氢化物的沸点一定比X氢化物的佛点高.
难度: 中等查看答案及解析
-
常温下联氨(N2H4)的水溶液中存在有:①N2H4+ H2O
N2H5++OH- K1②N2H5+ +H2O
N2H6++OH- K2。该溶液中的微粒的物质的量分数(X)随-lg c(OH-)变化的关系如图所示。则下列叙述不正确的是( )
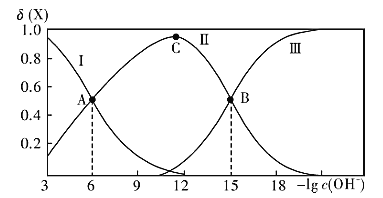
A.图中Ⅲ对应的微粒为N2H62+
B.若C点为N2H5Cl溶液,则存在:c(Cl-)>c(N2H5+ )+2c(N2H62+ )
C.将10mL0.1mol/L的联氨溶液与5mL0.1mol/L.的盐酸溶液混合后,所得溶液pH等于8
D.常温下羟胺(NH2OH)的Kb=10-10,将少量联氨水溶液加入到足量NH3OHCl溶液中,发生的反应为N2H4+NH3OH+=N2H5+ +NH2OH
难度: 困难查看答案及解析
 f.
f.  g.
g.  h.
h.