-
苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有
A.氧化性 B.还原性 C.碱性 D.酸性
难度: 中等查看答案及解析
-
很多地区连日雾霾天气的罪魁祸首之一是PM2.5 ,2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标。下面关于PM2.5的说法中不正确的是:
A.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物
B.PM2.5只是地球大气成分中含量很少的组分,对空气质量和能见度等没什么影响
C.PM2.5粒径小,富含大量的有毒、有害物质且在大气中的停留时间长、输送距离远
D.PM2.5主要来自化石燃料的燃烧(如机动车尾气、燃煤)、挥发性有机物等
难度: 简单查看答案及解析
-
能区分胶体和溶液的方法是
A.静置,有沉淀现象的是胶体 B.能透过滤纸的是溶液
C.有丁达尔现象的是胶体 D.用肉眼观察,均匀透明的是溶液
难度: 简单查看答案及解析
-
用Na2 CO3固体配制一定物质的量浓度的Na2 CO3溶液时,不需要使用的玻璃仪器是
A.圆底烧瓶 B.玻璃棒 C.容量瓶 D.胶头滴管
难度: 中等查看答案及解析
-
下列物质既可以通过金属与氯气反应制得,又可以通过金属与稀盐酸反应制得
A.FeCl2 B.FeCl3 C.CuCl2 D.AlCl3
难度: 简单查看答案及解析
-
用NA表示阿伏德罗常数,下列叙述正确的
A.标准状况下,22.4LH2O含有的分子数为1 NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
C.通常状况下,1 NA个CO2分子占有的体积为22.4L
D.标准状况下,22.4L CO2和SO2混合气中氧原子数为0.2NA
难度: 中等查看答案及解析
-
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数118,中子数为175的超重元素,该元素原子核内中子数与核外电子数之差是
A.47 B.57 C.61 D.293
难度: 中等查看答案及解析
-
在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟,应理解为
A、单质 B、分子 C、元素 D、氧化物
难度: 简单查看答案及解析
-
下列有关3He和4He的叙述中正确的是
A.3He比4He少1个质子 B.3He和4He互为同位素
C.3He和4He是同一种核素 D.3He和4He的中子数相同
难度: 简单查看答案及解析
-
在溶液中能大量共存的离子组是
A.Na+、OH一、HCO3- B.NH4+、NO3—、OH—
C.H+、K+、CO32-、 D.Ba2+、OH一、C1—
难度: 简单查看答案及解析
-
在盛有碘水的试管里加入少量四氯化碳,振荡后静置,可观察到
A.分层,上层呈紫红色,下层颜色变浅
B.分层,上层颜色变浅,下层呈紫红色
C.不分层,液体呈紫红色
D.不分层,液体为无色
难度: 简单查看答案及解析
-
只用一种试剂,可区别Na2SO4、FeCl3、NH4Cl、MgSO4四种溶液,这种试剂是
A.HCl B.BaCl2 C.AgNO3 D.NaOH
难度: 中等查看答案及解析
-
如果2g甲烷含有x个分子,那么22gCO2中所含分子数是
A.x B.4x C.0.5x D.3x
难度: 中等查看答案及解析
-
对于反应MnO2 + 4HCl(浓)
MnCl2 + 2H2O + Cl2↑,下列说法不正确的是
A.若生成7.1 g Cl2,则转移0.1 mol电子
B.MnO2是氧化剂
C.HCl是还原剂
D.该反应是氧化还原反应
难度: 中等查看答案及解析
-
实验室里可按如图装置来干燥、收集气体R,多余的气体R可用水吸收,则R是
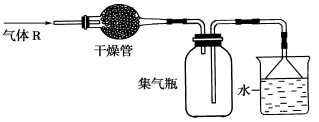
A.HCl B.Cl2 C.CO D.NH3
难度: 中等查看答案及解析
-
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.分别在这两种物质的溶液中,加入少量澄清石灰水
B.分别加热这两种固体,将生成的气体通入澄清石灰水中
C.分别在这两种物质的溶液中,加入少量氯化钙溶液
D.分别在这两种物质的等浓度的溶液中,加入少量的稀盐酸
难度: 中等查看答案及解析
-
下列说法正确的是
A.因为SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4溶液、石蕊试液褪色
B.能使品红褪色的不一定是SO2
C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D.盐酸能使滴有酚酞的NaOH溶液褪色,所以盐酸也有漂白性
难度: 中等查看答案及解析
-
氨水中存在的粒子有
①NH3 ②NH3·H2O ③H2O ④OH- ⑤NH ⑥H+
A.①②③④ B.②④⑤⑥
C.①②③④⑤ D.①②③④⑤⑥
难度: 中等查看答案及解析
-
对于铝热反应:Fe2O3 + 2Al
2Fe + Al2O3,下列说法中正确的是
A.Fe元素的化合价升高
B.若27 g Al参加反应则有3 mol电子转移
C.Fe2O3发生氧化反应
D.Al被还原
难度: 中等查看答案及解析
-
下列有关物质的性质或用途的叙述中,错误的是
A.硅晶体是一种重要的半导体材料
B.石墨可用做绝缘材料
C.漂白粉的有效成分是次氯酸钙
D.常温下,运输浓硫酸、浓硝酸时可用铝制或铁制槽车
难度: 中等查看答案及解析
-
下列除去杂质(括号内为杂质)的方法中,正确的是
A.NO(NO2):通过装有水的洗气装置
B.Cu粉(铁粉):加足量稀硝酸,过滤
C.NH3(H2O):通过装有浓硫酸的洗气装置
D.KCl(CaCl2):加适量Na2CO3溶液,过滤
难度: 中等查看答案及解析
-
X、Y、Z均为短周期元素,在元素周期表中它们的相对位置如图,已知3种元素的原子序数之和为31,下列有关叙述中正确的是
A.Y元素为Al
B.Z的氧化物不能与强碱溶液反应
C.原子半径大小为Y>Z>X
D.X只能形成一种氧化物
难度: 中等查看答案及解析
-
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路(已知发生的反应为 2FeCl3 + Cu =2FeCl2 + CuCl2)。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取100 mL废液加入足量的AgNO3溶液,生成沉淀 86.1g。(2)另取100 mL废液放入铜片充分反应,铜片质量减少了2.56 g。下列关于原废液组成的判断错误的是
A.c(Fe2+)︰c(Fe 3+)︰c(Cu2+) = 2︰1 ︰1
B.c(Fe2+)︰c(Cu2+) = 2︰1
C.一定含有Fe 2+、Fe 3+、Cu2+、Clˉ
D.c(Clˉ) = 6mol / L,c(Fe 2+) = 1.2mol / L
难度: 中等查看答案及解析

