-
标准状况下,两个容积相等的贮气瓶,一个装有O2,另一个装有CH4,两瓶气体具有相同的
A. 密度 B. 分子数 C. 质量 D. 原子总数
难度: 简单查看答案及解析
-
2mol Cl2和2mol CO2相比较,下列叙述中正确的是
A. 体积相等 B. 原子数相等 C. 分子数相等 D. 质量相等
难度: 简单查看答案及解析
-
下列说法正确的是
A.在常温常压下,11.2LN2含有的分子数为 0.5NA
B.标准状况下,22.4LH2和O2的混合物所含分子数为NA
C.标准状况下,18gH2O 的体积是 22.4L
D.1molSO2的体积是 22.4L
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 一定温度、压强下,气体体积由其分子的大小决定
B. 一定温度、压强下,气体体积由其物质的量的多少决定
C. 气体摩尔体积是指1mol任何气体所占的体积为22.4L
D. 不同的气体,若体积不等,则它们所含的分子数一定不等
难度: 简单查看答案及解析
-
1 mol·L-1硫酸溶液的含义是( )
A.1 L水中含有1 mol硫酸 B.1 L溶液中含有1 mol氢离子
C.将98 g硫酸溶于1 L水中配成溶液 D.1 L硫酸溶液中含98 g硫酸
难度: 简单查看答案及解析
-
在NaCl、MgCl2和MgSO4三种盐配成的混合溶液中,若Na+的浓度为0.1 mol/L,Mg2+的浓度为0.25 mol/L,Cl-的浓度为0.2 mol/L, 则SO42-的物质的量浓度为( )
A.0.5 mol/L B.0.2 mol/L
C.0.45 mol/L D.0.25 mol/L
难度: 中等查看答案及解析
-
同质量的下列气体中,所含原子数最少的是 ( )
A.CH4 B.CO2 C.H2S D.N2
难度: 简单查看答案及解析
-
下列关于阿伏加德罗常数的说法中正确的是
A.阿伏加德罗常数是12 g碳中所含的碳原子数
B.阿伏加德罗常数是0.012 kg12C中所含的原子数
C.阿伏加德罗常数是6.02×1023
D.阿伏加德罗常数的符号为NA,近似为6.02×1023
难度: 中等查看答案及解析
-
下列叙述中正确的是
A.1mol任何纯净物都含有相同的原子数
B.1mol O2中约含有6.02×1023个氧气分子
C.1mol氢中含有2mol氢原子
D.阿伏加德罗常数就是6.02×1023
难度: 简单查看答案及解析
-
某原子的摩尔质量是 M g /mol,则一个该原子的实际质量是( )
A.Mg B.
C.
D.
难度: 中等查看答案及解析
-
水电解的化学方程式为2H2O
2H2↑+O2↑,某同学电解一定量的水,制得8 g H2,则该8 g H2的物质的量为( )
A.2 mol B.4 mol C.8 mol D.89.6 mol
难度: 中等查看答案及解析
-
1.6 g某物质中含有6.02×1022个分子,则该物质的相对分子质量为 ( )
A.16 B.64
C.32 D.96
难度: 简单查看答案及解析
-
在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当l.6gX与Y完全反应后,生成4.4gR,则在此反应中Y和M的质量之比为( )
A.23:9 B.16:9 C.32:9 D.46:9
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.1mol任何气体所占体积都约为22.4L
B.1mol H2O在标准状况下体积为22.4L
C.1mol气体体积为22.4L,则一定是标准状况
D.气体摩尔体积不一定是22.4L/mol
难度: 中等查看答案及解析
-
在0℃和1.01×105 Pa条件下,将0.1g H2、3.2g SO2、2.2g CO2混合,该混合气的体积是( )
A. 3.36 L B. 2.24 L C. 4.48 L D. 6.72 L
难度: 简单查看答案及解析
-
同温、同压下,某容器充满O2重116 g,若充满CO2重122 g,现充满某气体重114 g,则该气体的相对分子质量为
A.28 B.60 C.32 D.44
难度: 简单查看答案及解析
-
在标准状况下,W L氮气含有n个氮气分子,则阿伏加德罗常数可表示为
A.Wn B.22.4n C.
D.
难度: 中等查看答案及解析
-
设阿伏伽罗常数的值为NA,标准状况下某种O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积应是( )
A.
L B.
L C.
L D.
L
难度: 中等查看答案及解析
-
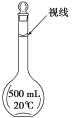
在配制物质的量浓度溶液的实验中,最后用胶头滴管定容后,液面正确的是( )
A.
B.
 C.
C.D.
难度: 简单查看答案及解析
-
下列有关实验的叙述正确的是( )
A.用分液的方法分离水和酒精的混合物
B.容量瓶用水洗净后,可不经干燥直接用于配制溶液
C.配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体
D.用滴管滴加液体时,为防止液滴溅出,滴管紧贴试管内壁
难度: 中等查看答案及解析
-
利用碳酸钠晶体(Na2CO3·10H2O)来配制0.5 mol/L的碳酸钠溶液1000 mL,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
A. 称取碳酸钠晶体100 g
B. 定容时俯视观察刻度线
C. 移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗
D. 定容后将容量瓶振荡均匀,静置发现液面低于刻度线,又加入少量水至刻度线
难度: 中等查看答案及解析
-
在相同体积、相同物质的量浓度的酸中,必然相等的是( )
A.H+ 的物质的量 B.溶质的质量分数
C.溶质的质量 D.溶质的物质的量
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值,下列关于0.2 mol·L-1 K2SO4溶液的说法正确的是( )
A.1 000 mL溶液中所含K+、SO42-总数为0.3NA
B.500 mL溶液中有0.1NA个K+
C.1 L溶液中K+的浓度为0.4 mol·L-1
D.1 L溶液中SO42-的浓度是0.4 mol·L-1
难度: 简单查看答案及解析
-
物质的量浓度相同的
三种溶液,当溶液体积比为3:2:1时,三种溶液中
的物质的量之比为( )
A.1:1:1 B.3:2:1 C.1:2:3 D.3:4:3
难度: 简单查看答案及解析
-
将4克NaOH溶解在10ml水中,在稀释成1L溶液,从中取出10ml,这10ml溶液的物质的量浓度为( )
A.0.01mol/L B.0.1mol/L C.1mol/L D.10mol/L
难度: 简单查看答案及解析
-
配制250mL1mol/L的稀盐酸溶液,需要12mol/L的浓盐酸的体积为( )
A.12mL B.25mL C.20.8mL D.12.5mL
难度: 中等查看答案及解析
-
下列关于物质的量的叙述,正确的是
A.1 mol任何物质均含有约6.02×1023个分子
B.1 mol水中含有2 mol氢和1 mol氧
C.0.012 kg碳-12中含有约6.02×1023个碳原子
D.1 mol H2含有6.02×1023个电子
难度: 简单查看答案及解析
-
在空气中的自由离子附着在分子或原子上形成的空气负离子被称为“空气维生素”,O22-就是一种空气负离子,则O22-的摩尔质量为( )
A.32 g B.34 g C.32 g·mol-1 D.34 g·mol-1
难度: 简单查看答案及解析
-
下列说法不正确的是
A.标准状况下,气体摩尔体积约为22.4 L/mol
B.非标准状况下,1 mol任何气体都不可能为22.4 L
C.标准状况下,22.4 L任何气体的物质的量都约为1 mol
D.标准状况下,1 mol H2O的体积小于22.4 L
难度: 简单查看答案及解析
-
下列说法正确的是
A.摩尔是基本物理量之一
B.1 mol H2O所含氧的质量为16 g
C.10 L H2比8 L H2所含H2的物质的量更多
D.某物质含有6.02×1023个粒子,那么此物质所占的体积为22.4 L
难度: 简单查看答案及解析
-
标准状况下,112 mL某气体的质量是0.14 g,该气体可能是
A.O2 B.N2 C.H2 D.CO2
难度: 简单查看答案及解析
-
一定量的14%的KOH溶液,若将其蒸发掉100g水后,其质量分数为28%,体积为125mL,则浓缩后的KOH的物质的量浓度为
A.2.2mol/L B.4mol/L C.5mol/L D.6.25mol/L
难度: 中等查看答案及解析
-
配制100 mL 1.0 mol/LNa2CO3溶液,下列操作正确的是
A.称取10.6 g无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容
B.称取10.6 g无水碳酸钠,加入100 mL蒸馏水,搅拌、溶解
C.转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中
D.定容后,塞好瓶塞,反复倒转、摇匀
难度: 中等查看答案及解析
-
标准状况下的aLHCl(g)溶于1000g水中,得到的盐酸密度为bg·cm-3,则该盐酸的物质的量浓度是( )
A.
mol·L-1 B.
mol·L-1
C.
mol·L-1 D.
mol·L-1
难度: 简单查看答案及解析