-
根据下列叙述,写出微粒符号。
(1)原子核外有2个电子层,核外有10个电子的原子___________;
(2)原子核内没有中子,核外没有电子的微粒__________;
(3)质量数为24,质子数等于中子数的离子____________________;
(4)由两个原子组成的具有10个电子的分子是________;
(5)由两个原子组成的具有10个电子的阴离子是________;
(6)由三个原子组成的具有10个电子的分子是________。
难度: 中等查看答案及解析
-
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断。
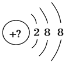
(1)该微粒是中性微粒,这种微粒的符号是________。
(2)该微粒的盐溶液能使溴水褪色,并出现浑浊,这种微粒的符号是________。
(3)该微粒的氧化性很弱,得到1个电子后变为原子,原子的还原性很强,这种微粒的符号是________。
(4)该微粒的还原性很弱,失去1个电子后变为原子,原子的氧化性很强,这种微粒的符号是________。
难度: 简单查看答案及解析
-
用
表示原子:
(1)中性原子的中子数:N=________。
(2)阳离子的中子数:
共有x个电子,则N=________。
(3)阴离子的中子数:
共有x个电子,则N=________。
(4)中性分子或原子团的中子数:
分子中,N=________。
(5)A2-原子核内有x个中子,其质量数为m,则ng A2-所含电子的物质的量为________。
难度: 简单查看答案及解析
-
(1)写出表示含有8个质子,10个中子的原子的化学符号:______;
(2)最外层电子数为次外层电子数
的原子______或______;(填元素符号)
(3)根据下列微粒回答问题:
H、
H、
H、
C、
、
、
、
①以上8种微粒共有______种核素,共______种元素.
②互为同位素的是______.
③质量数相等的是______和______,中子数相等的是______和______.
难度: 简单查看答案及解析
-
某微粒A的结构示意图为
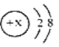
(1)若A是原子,则A的元素符号为__;若A是带一个正电荷的阳离子,则X=___
(2)若X=8,则此阴离子与(1)中带一个正电荷的阳离子形成一种常见化合物的化学式是___,它是不是电解质(填是或否)____。写出此化合物与盐酸反应的化学方程式:________________________________
(3)1mol微粒A含有10mol电子,下列微粒各1mol,也含有10mol电子的有:___(填序号)
①CH4 ②H2O2 ③HF ④Al3+ ⑤Cl- ⑥NH4+
(4)若A的阳离子为An+且质量数为a,则其质子数为____________,中子数为_______________(用含有a,n的代数式表达)
难度: 简单查看答案及解析