-
关于氧化还原反应,下列说法正确的是
A.被还原的物质是还原剂
B.氧化剂被还原,还原剂被氧化
C.失去电子,化合价降低的物质是还原剂
D.氧化剂失去电子,化合价升高
难度: 简单查看答案及解析
-
随着资源的开发和现代化工业的发展,你认为减少酸雨以保护环境可采取的措施是( )
①尽量少用煤作燃料 ②把工厂的烟囱加高 ③将燃料脱硫后再燃烧
④开发新的清洁能源 ⑤植树造林 ⑥在已酸化的土壤中加石灰
A.①②③④ B.③④⑤⑥ C.①③④ D.①③④⑤
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A.过氧化氢是由氢气和氧气组成的
B.酸和碱中都一定含有氢元素和氧元素
C.碱中一定含有氢氧根离子
D.氧化物和盐中一定含有氧元素
难度: 简单查看答案及解析
-
2019年新发现的元素鉝(Lv)是116号主族元素,其原子核外最外层电子数是6。下列说法不正确的是 ( )
A.Lv位于第七周期第VIA族 B.Lv在同主族元素中金属性最弱
C.Lv的同位素原子具有相同的电子数 D.中子数为177的Lv核素符号为
难度: 中等查看答案及解析
-
下列物质对应的化学式错误的是
A.偏铝酸钡 Ba(AlO2)2 B.明矾 KAl(SO4)2·12H2O
C.醋酸钙 (CH3COO)2Ca D.亚硫酸氢钙 CaHSO3
难度: 中等查看答案及解析
-
硒(Se)是人体健康必需的一种微量元素,已知Se的原子结构示意图如图,下列说法不正确的是
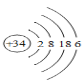
A. 该原子的质量数为34
B. 该元素处于第四周期第ⅥA族
C. SeO2既有氧化性又有还原性
D. 酸性:H2SO4>H2SeO4
难度: 简单查看答案及解析
-
在下列给定条件的溶液中,一定能大量共存的离子组是
A.无色溶液:Ca2+、、H+、Cl-、
B.能使pH试纸呈红色的溶液:Na+、
、I-、
C.FeCl2溶液:K+、、Na+、
、
D.
=0.1mol/L的溶液:Na+、K+、
、
难度: 中等查看答案及解析
-
我国的“神舟五号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的
,每百吨
核聚变所释放出的能量相当于目前人类一年消耗的能量。地球上氦元素主要以
形式存在。下列说法正确的是( )
A.
原子核内含有4个质子 B.
和
互为同位素
C.
原子核内含有3个中子 D.
与
的性质完全相同
难度: 简单查看答案及解析
-
只用一种试剂就可以鉴别乙醇溶液、乙酸溶液、葡萄糖溶液,这种试剂是
A.金属 Na B.盐酸
C.NaOH 溶液 D.新制
浊液
难度: 中等查看答案及解析
-
用NaOH固体配制一定物质的量浓度的NaOH溶液,下列操作中正确的是
A.称量时,将固体NaOH直接放在天平右盘上
B.将称量好的固体NaOH放入容量瓶中,加蒸馏水溶解
C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
D.将烧杯中溶解固体NaOH所得溶液,冷却到室温后转移至容量瓶中
难度: 中等查看答案及解析
-
焰色实验过程中,铂丝的清洗和灼烧与钾焰色实验的观察两项操作如图所示,下列叙述中不正确的是( )
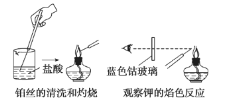
A.每次实验中都要先将铂丝灼烧到火焰颜色,再蘸取被检验物质
B.钾的焰色实验要透过蓝色钴玻璃观察
C.焰色实验是某种金属元素灼烧时所具有的特殊颜色,是化学变化
D.没有铂丝可用无锈铁丝代替进行实验
难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A.向盐酸中滴加氨水:
B.
溶于氢碘酸:
C.铜溶于稀硝酸:
D.
溶液与
溶液混合:
难度: 简单查看答案及解析
-
下列关于碳、硅的说法正确的是( )
A.碳、硅的最外层均有4个电子,易得电子表现较强氧化性
B.硅是构成岩石的基本元素,地壳中含量处于第二位
C.硅在自然界中既有游离态又有化合态
D.碳的氧化物和硅的氧化物在常温常压下均为气体
难度: 简单查看答案及解析
-
某同学受喷泉实验原理的启发,设计如图所示装置进行“喷烟”实验.下列对实验的有关说法错误的是( )
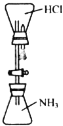
A.由于
的密度比HCl小,实验中二者的位置不能调换
B.“白烟”是由于生成
固体小颗粒的缘故
C.若用HBr代替HCl进行相同的操作,可得到相同的现象
D.实验时,打开活塞并挤出胶头滴管中的水即可看到白烟
难度: 简单查看答案及解析
-
同温同压下,等质量的CO和CO2相比较,下列叙述中正确的是( )
A.物质的量为1:1 B.体积比为11:7
C.原子数比为1:1 D.密度比为11:7
难度: 简单查看答案及解析
-
下列实验过程中产生的现象与对应的图象不相符的是( )
A.
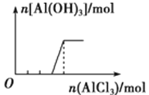 向NaOH溶液中滴加AlCl3溶液至过量
向NaOH溶液中滴加AlCl3溶液至过量B.
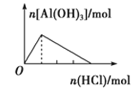 向NaAlO2溶液中滴加盐酸至过量
向NaAlO2溶液中滴加盐酸至过量C.
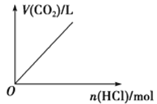 向Na2CO3溶液中逐滴加入稀盐酸
向Na2CO3溶液中逐滴加入稀盐酸D.
 向含有Mg2+和Al3+的溶液中加入NaOH溶液至过量
向含有Mg2+和Al3+的溶液中加入NaOH溶液至过量难度: 简单查看答案及解析
-
下列实验操作正确的是( )
A.
 读液体体积 B.
读液体体积 B. 引燃酒精灯
引燃酒精灯C.
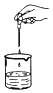 滴加液体 D.
滴加液体 D. 取固体药品
取固体药品难度: 简单查看答案及解析
-
在标准状况下,将VL A气体(摩尔质量为M g/mol)溶于0.1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为( )(单位为mol/L)
A.MV/[22.4(V+0.1)d] B.1000VdM/(MV+2240)
C.1000Vd/(MV+2240) D.Vd/(MV+2240)
难度: 中等查看答案及解析
-
在密闭容器中将2 mol NaHCO3(s)和一定量Na2O2混合,在加热条件下让其充分反应,150 ℃下所得气体仅含两种组分,反应后固体的物质的量(n)的取值范围是
A.n≥1 B.1<n<2 C.2≤n<4 D.n≥4
难度: 简单查看答案及解析
-
Cu粉放入稀H2SO4中,加热后无现象,当加入一种盐后,Cu粉质量减少,而溶液变蓝,同时有气体生成,此盐是
A.氯化物 B.硫酸盐 C.硝酸盐 D.碳酸盐
难度: 中等查看答案及解析


