-
下列属于电解质的是
A.氢氧化钠 B.三氧化硫 C.酒精 D.食盐水
难度: 简单查看答案及解析
-
仪器名称为“容量瓶”的是( )
A.
B.
 C.
C. D.
D.
难度: 简单查看答案及解析
-
镁粉在焰火、闪光粉、鞭炮中是不可缺少的原料。工业制造镁粉是将镁蒸气在某种气体中冷却,下列可作为冷却的气体是
A.Ar B.N2 C.空气 D.CO2
难度: 简单查看答案及解析
-
坩埚是实验室用于灼烧或熔融固体物质的常用仪器,材质种类很多,实验时应根据物质的性质加以选择。熔融烧碱应选用
A.石英坩埚 B.普通玻璃坩埚 C.瓷坩埚 D.铁坩埚
难度: 简单查看答案及解析
-
按照物质的组成和性质来分类,CaO属于
①化合物 ②混合物 ③金属氧化物 ④非金属氧化物 ⑤酸性氧化物 ⑥碱性氧化物
A.②④ B.①④⑤ C.①③⑥ D.②③⑤
难度: 简单查看答案及解析
-
化学与生产、生活密切相关。下列叙述正确的是
A.
溶液不能产生丁达尔效应,不属于胶体
B.
可用于文物的年代鉴定,
与
互称为核素
C.
在医学上用作“钡餐”,
对人体无毒
D.主要成分为
的磁铁矿,是工业炼铁的原料
难度: 中等查看答案及解析
-
下列说法中正确的是
A.用原子吸收光谱确定物质中含有哪些金属元素
B.在医疗上硫酸铁可用于生产防治缺铁性贫血的药剂
C.在电流作用下,硫酸钠在水溶液中电离成
和
D.加入少量铁粉可防止
溶液变质
难度: 中等查看答案及解析
-
下列实验中,所选装置不合理的是
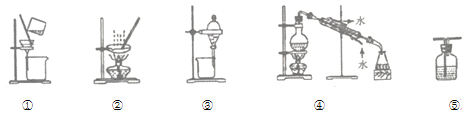
A.分离
溶液和汽油,选④ B.分离溶有碘的
层和水层,选③
C.用NaOH溶液吸收
气体,选⑤ D.粗盐提纯,选①和②
难度: 简单查看答案及解析
-
下列转化必须要通过加氧化剂才能实现的是(不考虑电解)
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列有关钠及其化合物的说法中正确的是
A.钠的硬度很大,无法用小刀切开 B.钠与氧气反应的产物只能是氧化钠
C.金属钠着火时,用细沙覆盖灭火 D.工业上通过电解氯化钠溶液制备金属钠和氯气
难度: 简单查看答案及解析
-
某盐的混合物中含有
、
、
、
离子,测得
、
、
离子的物质的量浓度分别为
、
、
,则
的物质的量浓度为
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列说法正确的是
A.从金属矿物中获得金属单质是金属元素被氧化的过程
B.炼铁时,加入石灰石的目的是促进氧化铁生成铁
C.由黄铜矿冶炼所得的铜单质可直接用于电气工业
D.接触法制备硫酸中的主要设备有沸腾炉、接触室和吸收塔
难度: 中等查看答案及解析
-
在同温同压下,分别用如图所示的气体吹出体积相等的甲、乙两个气球,则这两个气球中气体的有关量之比(甲:乙)正确的是
A.质量之比为
B.原子总数之比为
C.分子总数之比为
D.碳原子数之比为
难度: 中等查看答案及解析
-
检验氯化氢气体中是否混有氯气,可采用的方法是( )
A.用干燥的蓝色石蕊试纸 B.用干燥有色布条
C.将气体通入硝酸银溶液 D.用湿润的淀粉碘化钾试纸
难度: 中等查看答案及解析
-
下列关于原子结构的说法中正确的是
A.卢瑟福根据
粒子散射现象提出“葡萄干面包式”的原子结构模型
B.原子中,核对核外电子吸引作用实质是核内的质子对核外电子的吸引
C.质子数决定元素的种类,中子数决定核素的种类
D.所有的原子都含有质子、中子和电子3种基本粒子
难度: 中等查看答案及解析
-
下列表示化学反应的离子方程式正确的是
A.
溶液中滴入稀盐酸:SO32-+2H+=H2O+SO2↑
B.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+
C.碳酸钙溶于稀醋酸:CaCO3+2H+=Ca2++H2O+CO2↑
D.钠与硫酸铜水溶液反应:2Na+Cu2+=Cu+2Na+
难度: 中等查看答案及解析
-
实验室需配制
溶液,下列说法不正确的是
A.应用托盘天平称取
晶体
B.配制操作必需的玻璃仪器是烧杯、玻璃棒、胶头滴管、500mL容量瓶
C.采用加热来加快
晶体的溶解,需趁热迅速将溶液转移至容量瓶中
D.定容摇匀后发现溶液液面低于刻度线,不需要再滴加蒸馏水至刻度线
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A.
和CO的混合物共
,其中碳原子的数目为NA
B.
重水
分子中含有的中子数为0.8NA
C.
放入过量的98%浓
中,转移电子数为3NA
D.
的NaCl溶液中微粒数大于0.5NA
难度: 中等查看答案及解析
-
下列关于硫及其化合物的叙述正确的是
A.浓硫酸滴加到少量胆矾晶体上,晶体变白,体现浓硫酸脱水性
B.硫在足量空气中燃烧生成大量
C.二氧化硫可在葡萄酒中微量添加
D.向
水溶液中滴加
溶液,有白色沉淀生成
难度: 中等查看答案及解析
-
wg铁粉与含有
的
稀溶液完全反应后,得到wg铜,则参与反应的
与
的物质的量之比为
A.
B.
C.
D.
难度: 中等查看答案及解析
-
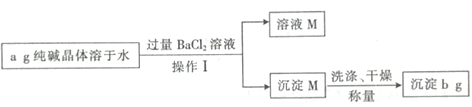
纯碱和小苏打是厨房中常用品,它们都是白色固体。下列区分这两种物质的方法中正确的是
A.先将两种样品配制成溶液,分别加入石灰水,无白色沉淀生成的是小苏打
B.用两小玻璃杯,分别加入少量的两种样品,再加入等量食醋,产生气泡快的是小苏打
C.用洁净铁丝蘸取两种样品在煤气火焰上灼烧,火焰颜色发生明显变化的是小苏打
D.分别用砂锅加热两种样品足够长的时间,没有固体残留的是小苏打
难度: 中等查看答案及解析
-
某同学用下列装置完成了浓硫酸和
性质实验(夹持装置已省略)
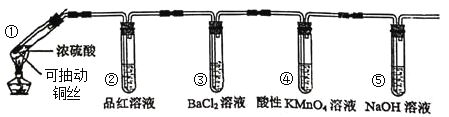
下列说法错误的是
A.反应后,试管①中出现白色固体,将其放入水中溶液显蓝色
B.试管②中品红溶液逐渐褪色,对其加热溶液又恢复红色
C.试管④中酸性高锰酸钾溶液褪色,体现了
的漂白性
D.试管⑤可以改为装有碱石灰的干燥管
难度: 中等查看答案及解析
-
从海带中提取碘的一种工业生产过程如下:
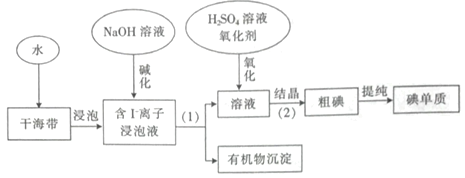
下列说法中错误的是
A.步骤(1)需要过滤装置
B.步骤(2)需要用到分液漏斗
C.“碱化”目的是让可溶性有机质形成沉淀
D.“氧化”是让I-转化为I2,可以用适量氯气作氧化剂
难度: 中等查看答案及解析
-
某固体混合物X可能是由
、Fe、
、
中的两种或两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,进行如下实验(所加试剂均过量)
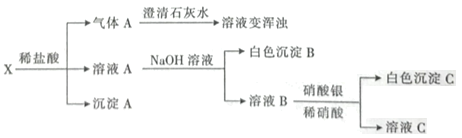
下列说法不正确的是
A.气体A是混合气体
B.沉淀A是
C.白色沉淀B在空气中迅速变为灰绿色,最后变为红褐色
D.该固体混合物一定含有
、
难度: 中等查看答案及解析
-
通过实验得出的结论正确的是
A.某固体试样溶于水,向其中滴加NaOH溶液,没有产生使湿润红色石蕊试纸变蓝的气体,说明原固体中无
B.某固体试样溶于稀盐酸,先滴加KSCN溶液无明显现象,再滴加氯水后显红色,说明原固体中含有
C.某固体试样溶于水得无色溶液,滴加少量新制氯水,再滴加少量
,振荡后静置,下层出现橙红色,说明原固体中含有
D.某固体试样溶于稀盐酸,取少量溶液进行焰色反应为黄色,说明原固体为钠盐
难度: 中等查看答案及解析