-
化学与科技、生产、生活密切相关,下列说法正确的是( )
A.使用含有CaCl2的融雪剂会加速对桥梁的腐蚀
B.二氧化氯(ClO2)具有还原性,故可用作自来水的杀菌消毒
C.碳酸氢钠(NaHCO3)是一种抗酸药,服用时喝些醋能提高药效
D.“华为麒麟980”手机中芯片的主要成分是二氧化硅
难度: 中等查看答案及解析
-
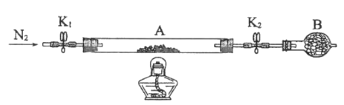
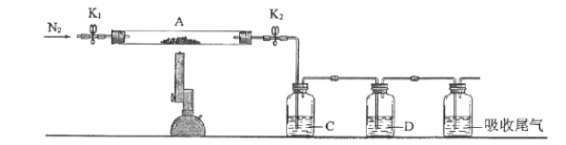
实验室制备硝基苯的实验装置如图所示,关于实验操作或叙述错误的是( )
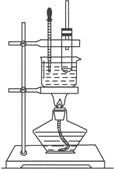
A.配制一定比例的浓H2SO4和浓HNO3混合酸时是往浓HNO3注入浓H2SO4,并及时搅拌和冷却
B.在50~60℃下发生反应,图中加热方式是水浴加热
C.实验中长导管能除了导气外还起冷凝回流的作用
D.反应后的混合液经稀碱溶液洗涤、结晶,得到硝基苯
难度: 中等查看答案及解析
-
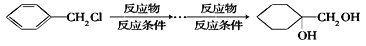
有机物W在工业上常用作溶剂和香料,其合成方法如图,下列说法不正确的是
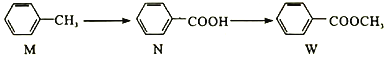
A. M、N、W均能发生加成反应和取代反应
B. N、W组成上相差一个CH2原子团,所以互为同系物
C. 1molM与1molw完全燃烧消耗O2的物质的量相同
D. M苯环上的二氯代物有6种
难度: 中等查看答案及解析
-
在下列各溶液中,一定能大量共存的离子组是( )
A.常温下水电离的c(H+)为1×10-12mol/L的溶液中:I-、Na+、Cl-、NO3-
B.滴加石蕊后呈蓝色的溶液中:K+、AlO2-、Cl-、HCO3-
C.无色透明的溶液中:MnO4-、K+、H+、SO42-
D.弱碱性溶液中:Na+、K+、Cl-、CO32-
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的数值。下列说法正确的是( )
A.0.1mol⋅L-1的AlCl3溶液中含Al3+的数目小于0.1NA
B.0.5mol环己烷中含非极性键的数目为2.5NA
C.30g由葡萄糖和乳酸(C3H6O3)组成的混合物中含氢原子数目为2NA
D.7.1gCl2完全反应转移的电子数一定为0.2NA
难度: 中等查看答案及解析
-
关于小苏打溶液的表述错误的是
A. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
C. HCO3-的电离程度小于其水解程度
D. c(Na+)>c(HCO3-)>c(OH-)>c(CO32-)>c(H+)
难度: 简单查看答案及解析
-
2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。磷酸铁锂锂离子电池充电时阳极反应式为,
,放电工作示意图如图。下列叙述不正确的是
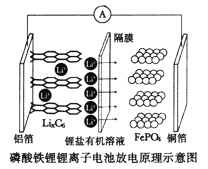
A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不发生变化
难度: 简单查看答案及解析