-
下列说不正确的是
A. 金属钠有强还原性,能和硫酸铜溶液反应,析出金属铜
B. 用Al(OH)3治疗胃酸过多
C. 过氧化钠可用于呼吸面具中作为氧气的来源
D. 绚丽缤纷的烟花中添加了含钾、钙、钠、铜等金属元素化合物
难度: 中等查看答案及解析
-
在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,一定能大量共存的是
A. NH4+、SO42-、CO32-、K+ B. Na+、Ba2+、Ca2+、HCO3-
C. Mg2+、SO42-、K+、Cl- D. K+、Cl-、Na+、SO42-
难度: 中等查看答案及解析
-
将直径在1 nm~100 nm之间的食盐晶体超细粒子分散到酒精中,激光笔照射能看到丁达尔效应,所形成的分散系是
A. 溶液 B. 胶体 C. 悬浊液 D. 乳浊液
难度: 中等查看答案及解析
-
下列物质中既能跟稀 H2SO4 反应,又能跟 NaOH 溶液反应的有
① Mg ② Al2O3 ③ Al(OH)3 ④ CuCl2
A. ①③ B. ①④ C. ②③ D. ②④
难度: 中等查看答案及解析
-
下列溶液中Cl-浓度最小的是
A.25 mL 1 mol·L−1 AlCl3 溶液 B.30 mL 3 mol·L−1 KCl 溶液
C.20 mL 2 mol·L−1 MgCl2 溶液 D.30 mL 2 mol·L−1 NaCl 溶液
难度: 中等查看答案及解析
-
碳酸钠是一种非常重要的化工原料,它属于
A.酸 B.碱 C.盐 D.氧化物
难度: 简单查看答案及解析
-
下列物质属于电解质的是
A.铜 B.氯化钠 C.一氧化氮 D.乙醇
难度: 中等查看答案及解析
-
下列化学用语表示正确的是
A.Mg2+的结构示意图:
B.明矾的化学式: Al2(SO4)3
C.过氧化钠的化学式: Na2O2
D.碳酸氢钠的电离方程式: NaHCO3 = Na+ + H+ + CO32−
难度: 中等查看答案及解析
-
在含有大量 H+、Ba2+、Cl— 的溶液中,还可能大量共存的离子是
A.Ag+ B.Ca2+ C.CO32- D.SO42-
难度: 中等查看答案及解析
-
下列说法正确的是
A. O2 的摩尔质量是32 g B. 1 mol Na2O 的质量是62 g
C. 18 g H2O 含有氢原子数目为1 mol D. 22.4 L SO2 的物质的量是 1 mol
难度: 中等查看答案及解析
-
相同物质的量的H2O和H2O2相比较,下列有关叙述中正确的是
①它们所含的分子数目之比为1∶1
②它们所含的O原子数目之比为1∶2
③它们所含的原子总数目之比为3∶4
④它们所含的H原子数目之比为1∶1
⑤它们所含的电子数目之比为5∶9
A.①②③④ B.②和③ C.④和⑤ D.①②③④⑤
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是
A.钠与水反应:Na + H2O = Na+ + OH- + H2↑
B.铁与盐酸反应: Fe +2H+ = Fe2+ + H2↑
C.用醋酸除水垢:CaCO3 + 2H+= Ca2+ + H2O + CO2↑
D.碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A.少量AlCl3溶液滴入过量的NaOH溶液中:Al3++4OH-=AlO2-+2H2O
B.铜片插入硝酸银溶液: Cu + Ag+ = Cu2+ + Ag
C.用小苏打治疗胃酸过多:CO32-+2H+=CO2+H2O
D.向AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
难度: 中等查看答案及解析
-
下列有关实验装置进行的相应实验,能达到实验目的的是
A.
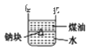 用装置证明:ρ(煤油)<ρ(钠)<ρ(水)
用装置证明:ρ(煤油)<ρ(钠)<ρ(水)B.
 用装置读数
用装置读数C.
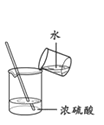 用所示装置稀释浓H2SO4
用所示装置稀释浓H2SO4D.
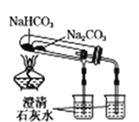 用装置比较NaHCO3和Na2CO3的热稳定性
用装置比较NaHCO3和Na2CO3的热稳定性难度: 中等查看答案及解析
-
铝热反应可用于焊接钢轨,反应为:2Al + Fe2O3
2Fe + Al2O3,下列关于该反应说法正确的是( )
A. Al 是还原剂 B. Fe2O3 发生氧化反应
C. Fe 是氧化产物 D. 当生成 1 mol Fe 时,转移 6 mol 电子
难度: 中等查看答案及解析
-
下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)
物质
除杂试剂
操作
A
CO2 (HCl)
氢氧化钠溶液
洗气
B
FeCl2 溶液 (CuCl2)
锌粉
充分反应后过滤
C
Na2CO3固体(NaHCO3)
无
充分加热
D
Fe2O3 (Al2O3)
稀硫酸
充分反应后过滤
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列关于离子检验叙述正确的是
A.用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,火焰呈黄色,原溶液中可能存在 Na+,一定无 K+
B.某溶液中加入 BaCl2 溶液,产生白色沉淀,则原溶液中一定存在 SO42-
C.向某溶液中滴加NaOH溶液,先产生白色沉淀后沉淀溶解,则原溶液可能存在 Al3+
D.某溶液中加入 AgNO3 溶液,产生白色沉淀,说明原溶液中一定存在Cl-
难度: 中等查看答案及解析
-
下列各组物质中,存在X→Y或Y→Z不能通过一步反应完成转化的一组是
选项
X
Y
Z
A
AlCl3
Al(OH)3
NaAlO2(aq)
B
MgO
Mg(OH)2
Mg
C
H2O(g)
Fe3O4
Fe
D
NaOH(aq)
Na2CO3(aq)
NaHCO3(aq)
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列各项操作中符合“先出现沉淀后沉淀完全溶解”现象的是
A.向Fe(OH)3胶体中逐滴滴加稀H2SO4至过量
B.向BaCl2溶液中通入CO2至过量
C.向Al2(SO4)3溶液中逐滴滴加Ba(OH)2至过量
D.向NaOH溶液中逐滴滴加AlCl3至过量
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值,下列说法中不正确的是
A.7.8 g Na2O2与足量CO2完全反应时转移电子数为0.1NA
B.一定条件下,1.0 mol Cl2与足量铁完全反应转移电子数为2NA
C.2.3 g Na与O2完全反应生成3.6 g产物时失去的电子数为0.1NA
D.25℃时,0.1 mol·L-1 Na2S溶液中含有Na+的数目为0.2NA
难度: 中等查看答案及解析