-
XY2是离子化合物,X和Y离子电子层结构都与氖原子相同,则X、Y分别为( )。
A.Ca和Cl B.K和S C.Ca和F D.Mg和F
难度: 中等查看答案及解析
-
下列性质中,可以证明某化合物内一定存在离子键的是( )
A.可溶于水 B.具有较高的熔点 C.水溶液能导电 D.熔融状态能导电
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.离子键就是使阴阳离子结合成化合物的静电引力
B.所有金属元素与所有非金属元素之间都能形成离子键
C.在化合物CaCl2中,两个氯离子之间也存在离子键
D.含有离子键的化合物一定是离子化合物
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.含有离子键的化合物一定是离子化合物
B.阳离子一定由金属元素组成
C.离子化合物中一定含有金属元素
D.非金属元素所组成的化合物中不可能含有离子键
难度: 中等查看答案及解析
-
下列各离子化合物中,阳离子与阴离子的半径之比最小的是( )
A. KCl B. NaBr C. LiI D. KF
难度: 简单查看答案及解析
-
氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应放出氢气,下列叙述中不正确的是( )
A.NaH的电子式为Na+[:H]—
B.NaH与水反应时水作氧化剂
C.NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同
D.半径:H+>H—
难度: 中等查看答案及解析
-
下列说法正确的是
A.钠原子与氯原子反应生成食盐后,其结构的稳定性增强
B.阴、阳离子之间有强烈的吸引作用而没有排斥作用,所以离子键的核间距离相当小
C.失电子难的原子获得电子的能力一定强
D.任何离子键在形成过程中必定有电子的得与失
难度: 中等查看答案及解析
-
Y元素最高正价与负价的绝对值之差是6;Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物是( )
A.KCl B.NaF C.Na2O D.NaCl
难度: 中等查看答案及解析
-
下列各式用电子式表示的物质的形成过程,其中正确的是( )
A.
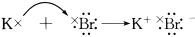
B.
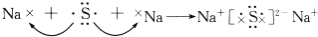
C.
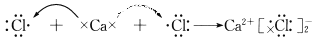
D.
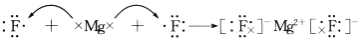
难度: 中等查看答案及解析
-
M、R均为主族元素,已知M的一个原子失去2个电子与R的一个原子得到一个电子后,均可形成与某稀有气体元素相同的电子层结构。下列关于M与R形成的化合物的叙述中正确的是( )。
A.M与R可形成MR2型离子化合物
B.在MR2中M的离子半径比R的离子半径大
C.M与R形成的离子化合物一定难溶于水
D.MR2的电子式为
难度: 中等查看答案及解析