-
依据元素周期表和元素周期律,下列推断正确的是
A.H3BO3的酸性比H2CO3的强
B.Mg(OH)2的碱性比Be(OH)2的强
C.HCl 、HBr 、HI的热稳定性依次增强
D.若M+和R2-的核外电子层结构相同,则原子序数:R>M
难度: 中等查看答案及解析
-
短周期金属元素甲~戊在元素周期表中的相对位置如表所示。下列判断正确的是( )
甲
乙
丙
丁
戊
A.丙的单质能从丁的硫酸盐溶液中置换出丁的单质
B.金属性:甲>丙
C.氢氧化物碱性:丙>丁>戊
D.丙与戊最高价氧化物的水化物间发生的反应,不能证明丙和戊的金属性强弱
难度: 中等查看答案及解析
-
能说明氯元素的非金属性比硫元素强的事实是
①Cl2与H2S溶液发生置换反应
②受热时H2S能分解,HCl则不能
③单质硫可在空气中燃烧,Cl2不能
④HCl是强酸,H2S是弱酸
A.①② B.②③ C.③④ D.②④
难度: 中等查看答案及解析
-
下列各组物质中,所含化学键类型相同的是( )
A.NaF、HNO3 B.HCl、MgF2
C.CO2、CH4 D.Na2O、H2O
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.两个原子或多个原子之间的相互作用叫做共价键
B.阴、阳离子间通过静电引力而形成的化学键叫做离子键
C.只有金属元素和非金属元素化合时才能形成离子键
D.大多数的盐、碱和低价金属氧化物中含有离子键
难度: 简单查看答案及解析
-
W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y。下列说法正确的是
A.Y的低价氧化物与O3漂白的原理相同
B.Y的氢化物和W2Y所含化学键的类型相同
C.上述三种元素形成的简单离子,X离子半径最小
D.工业上常用电解相应的盐溶液制备W、X的单质
难度: 中等查看答案及解析
-
Cl、
Cl为不同的核素,下列说法正确的是
A.
Cl2的摩尔质量是74
B.通常情况下,氯气做氧化剂,但氯气也具有还原性
C.
Cl、
Cl互为同位素,
Cl2与
Cl2互为同素异形体
D.常温下,4.48L
Cl2含有8NA个中子(NA为阿伏加德罗常数的值)
难度: 简单查看答案及解析
-
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体。下列说法错误的是( )

A.S2Cl2为共价化合物
B.S2Cl2只含有极性共价键
C.S2Cl2与水反应时S—S键和S—Cl键都断裂
D.S2Cl2分子中S—S键和S—Cl键是通过共用电子对的相互作用形成的
难度: 简单查看答案及解析
-
下列各表为周期表的一部分(表中为原子序数),其中正确的是( )
A.
B.
C.
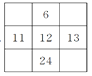 D.
D.难度: 简单查看答案及解析
-
根据原子结构及元素周期律的知识,下列推断正确的是
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. Cl‾、S2‾、Ca2+、K+半径逐渐减小
D.
与
得电子能力相同
难度: 简单查看答案及解析