-
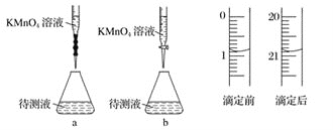
用标准浓度的NaOH溶液滴定未知浓度的盐酸时下列情况会使盐酸物质的量浓度偏低的是( )
A. 碱式滴定管用蒸馏水洗净后,直接注入标准浓度的NaOH溶液
B. 碱式滴定管尖端有气泡,滴定后气泡消失
C. 记录消耗的碱液,滴定前平视,滴定后俯视凹液面
D. 锥形瓶用蒸馏水洗净后,直接装入未知浓度的盐酸
难度: 中等查看答案及解析
-
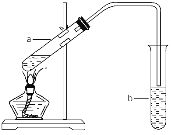
居民所用石油液化气的主要成分是丁烷,在使用过程中,常有一些杂质以液态沉积于钢瓶中,这些杂质可能是( )
A. 甲烷和丙烷 B. 丁烷和甲醛 C. 乙烷和丁烷 D. 戊烷和己烷
难度: 中等查看答案及解析
-
常用的打火机使用的燃料其分子式为C3H8,它属于( )
A. 烷烃 B. 烯烃 C. 炔烃 D. 芳香烃
难度: 简单查看答案及解析
-
塑化剂的成分主要是邻苯二甲酸二异丁酯等酯类,塑料管道、塑胶容器、瓶盖或其他塑料包装材料都含有塑化剂,塑化剂超标对人体有害.调查发现,最近深受关注的白酒中含有的塑化剂主要是由塑料制品中的塑化剂迁移到酒中所致,此处“迁移”所涉及的主要原理是( )
A.萃取 B.蒸馏 C.溶解 D.渗析
难度: 简单查看答案及解析
-
据报道,近来发现了一种新的星际分子氰基辛炔,其结构简式为HC≡C—C≡C—C≡C—C≡C—C≡N。下列对该物质的判断正确的是( )
A.属于不饱和烃 B.不能使酸性KMnO4溶液褪色
C.所有原子都在同一条直线上 D.可由乙炔和含氮化合物加聚制得
难度: 中等查看答案及解析
-
下列有机物中,不属于烃的衍生物的是( )
A.卤代烃 B.醋酸
C.邻二甲苯 D.苯酚
难度: 中等查看答案及解析
-
下列电离方程式书写正确的是( )
A. NaHCO3===Na++H++
B. HF
H++F-
C. H2SO4
2H++
D. CH3COONH4
CH3COO-+
难度: 中等查看答案及解析
-
向5 mL NaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶解度关系为
A. AgCl=AgI=Ag2S B. AgCl<AgI<Ag2S
C. AgCl>AgI>Ag2S D. AgI>AgCl>Ag2S
难度: 中等查看答案及解析
-
下列有关离子反应的叙述不正确的是( )
A.溶液中有难溶于水的沉淀生成是离子反应的发生条件之一
B.离子反应发生的方向总是向着溶液中离子浓度降低的方向进行
C.离子反应生成的沉淀的溶解度为零
D.生成沉淀的离子反应之所以能发生,在于生成物的溶解度小
难度: 中等查看答案及解析
-
已知:a.C2H2(g)+ H2(g)= C2H4(g)ΔH<0
b. 2CH4(g)= C2H4(g)+ 2H2(g)ΔH>0
判断以下3个热化学方程式:
①C(s)+ 2H2(g)= CH4(g)ΔH1
②C(s)+
H2(g)=
C2H2(g)ΔH2
③C(s)+ H2(g)=
C2H4(g)ΔH3
ΔH1、ΔH2、ΔH3由大到小的顺序是( )
A.ΔH2 >ΔH3 >ΔH1 B.ΔH3 >ΔH2 >ΔH1
C.ΔH3 >ΔH1 >ΔH2 D.ΔH1 >ΔH2 >ΔH3
难度: 简单查看答案及解析
-
用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
A.3 mol·L-1 B.2 mol·L-1 C.4 mol·L-1 D.1 mol·L-1
难度: 中等查看答案及解析
-
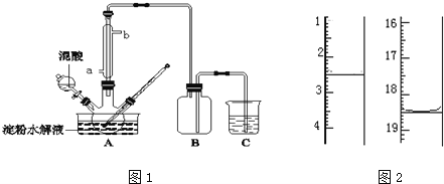
将图1所示装置中的盐桥(琼脂-饱和
溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是

A.图1中,铁棒质量减少5.6g,则甲池
溶液的质量增加5.6g
B.图1中的石墨电极与图2中乙池石墨
电极的电极反应式相同
C.两图所示装置的能量变化均是将化学能转化为电能
D.图2中电子流向为
电流计→石墨a→石墨b→铜丝→石墨c→
难度: 困难查看答案及解析
-
下列溶液中的离子关系正确的是( )
A.相同温度下,0.2 mol·L-1的醋酸溶液与0.l mol·L-1的醋酸溶液中c(H+)之比大于2 : 1
B.pH=3的醋酸和pH=3的FeCl3溶液中,由水电离出的c(H+)相等
C.0.l mol﹒L-1NaHSO4溶液中:c(H+)=c(SO
) +c(OH-)
D.pH=4、浓度均为0.l mol·L-1的CH3COOH、CH3COONa 混合溶液中:c(CH3COO-)-c(CH3COOH)=10-4-10-10mol/L
难度: 中等查看答案及解析
-
下列有关电解质的叙述正确的是( )
A.化合物都是电解质
B.电解质一定是化合物
C.SO3溶于水后,溶液能导电,所以SO3是电解质
D.NaCl固体不能导电,所以NaCl不是电解质
难度: 简单查看答案及解析
-
在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10-10。下列说法不正确的是( )
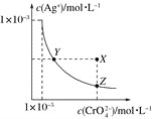
A.t℃时,Ag2CrO4的Ksp为1×10-8
B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.t℃时,Y点和Z点时Ag2CrO4的Ksp相等
D.t℃时,将0.01 mol·L-1AgNO3溶液滴入20 mL 0.01 mol·L-1KCl和0.01 mol·L-1K2CrO4的混合溶液中,Cl-先沉淀
难度: 困难查看答案及解析
-
燃烧是人类最早利用的化学反应之一,人类已有几十万年的利用燃烧反应的历史,燃烧需要具备的条件是( )
①可燃物 ②氧气(空气等助燃剂) ③温度达到着火点
A.①② B.②③ C.①③ D.①②③
难度: 简单查看答案及解析
-
下列能量中不能通过化学反应产生的是
A.热能 B.电能 C.光能 D.核能
难度: 简单查看答案及解析
-
某温度下,
分别在溶液中达到沉淀溶解平衡后,改变溶液
,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
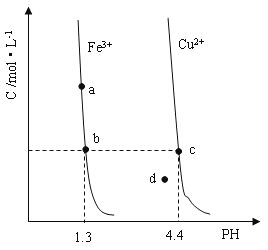
A.
B.加适量
固体可使溶液由
点变到
点
C.
两点代表的溶液中
与
乘积相等
D.
、
分别在
、
两点代表的溶液中达到饱和
难度: 中等查看答案及解析
-
下列表示物质结构的化学用语或模型正确的是( )
A.乙烯的最简式:CH2=CH2 B.CH4分子的比例模型:

C.羟基:
D.Cl-的结构示意图:
难度: 中等查看答案及解析
-
冰箱制冷剂氟氯甲烷在高空受紫外线辐射时产生Cl原子,并能发生下列反应:Cl+O3→ClO+O2 ClO+O→Cl+O2,下列说法不正确的是( )
A.反应过程中将O3转变为O2 B.Cl原子是总反应的催化剂
C.氟氯甲烷是总反应的催化剂 D.Cl原子起分解O3的作用
难度: 中等查看答案及解析
-
某炔烃经催化加氢后,得到2-甲基丁烷,该炔烃是:
A.2-甲基-1-丁炔 B.2-甲基-3-丁炔 C.3-甲基-1-丁炔 D.3-甲基-2-丁炔
难度: 中等查看答案及解析
-
下列说法错误的是
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的沸点和熔点都比乙烷和乙烯的沸点和熔点高
C.乙醇和乙酸都能发生氧化反应
D.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为可逆反应
难度: 中等查看答案及解析
-
下列说法中,正确的是( )
A.用氢氧化钠溶液清洗沾在皮肤上的苯酚 B.用浓硫酸吸收氨气中的水分
C.用稀硝酸洗去残留在试管内壁上的银 D.用酒精萃取碘水中的碘
难度: 简单查看答案及解析
-
下列反应不需要浓硫酸的是( )
A.制乙烯 B.苯的硝化
C.制TNT D.制乙炔
难度: 中等查看答案及解析
-
2000年诺贝尔化学奖授予两位美国化学家和一位日本化学家,以表彰他们在导电塑料领域的贡献,他们首先把聚乙炔树脂制成导电塑料,下列关于聚乙炔的叙述错误的是( )
A.聚乙炔是以乙炔为单体发生加聚反应形成的高聚物
B.聚乙炔的化学式为
C.聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质
D.聚乙炔树脂不加任何填充物即可成为电的良导体
难度: 简单查看答案及解析