-
在“新冠肺炎战疫” 中, 化学知识发挥了重要作用。下列物质不能杀灭冠状病毒的是
A.双氧水 B.84 消毒液
C.75%的医用酒精 D.明矾溶液
难度: 简单查看答案及解析
-
钇(Y)是一种重要超导材料的组成元素。下列关于
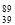 Y 的说法不正确的是
Y 的说法不正确的是A.质量数为 89 B.核外电子数为 39
C.中子数为 128 D.钇是金属元素
难度: 简单查看答案及解析
-
下列物质含有离子键是
A.H2 B.Fe
C.NaCl D.HCl
难度: 简单查看答案及解析
-
下列说法不正确的是
A.糖类都能水解
B.乙烯可用作水果催熟剂
C.可用灼烧的方法鉴别蚕丝和棉花
D.工业上利用油脂在碱性条件的水解反应制取肥皂
难度: 简单查看答案及解析
-
下列化学用语正确的是
A.葡萄糖的分子式:C12H22O11 B.NH3的结构式:
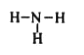
C.Cl-的结构示意图:
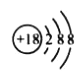 D.CO2的电子式:
D.CO2的电子式: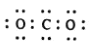
难度: 简单查看答案及解析
-
以下铜锌原电池工作原理认知模型图中, 不正确的是
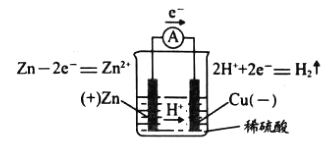
A.正负极标注 B.电极反应式
C.电子移动方向 D.H+的移动方向
难度: 简单查看答案及解析
-
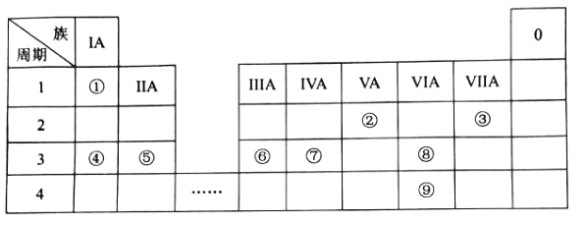
2019年是“国际化学元素周期表年”。下列对元素周期表的认识正确的是
A.周期表中共有18个族
B.第一、二、三周期为短周期
C.第三周期主族元原子半径自左向右依次增大
D.第二周期主族元素从左到右,最高正化合价从+1递增到+7
难度: 简单查看答案及解析
-
下列比较不正确的是
A.密度:Na>Li B.稳定性:HF<HCl
C.酸性:HClO4>H2SO4 D.碱性:NaOH>Mg(OH)2
难度: 简单查看答案及解析
-
决定化学反应速率的主要因素是
A.反应温度
B.反应物的浓度
C.反应物本身的性质
D.反应物之间的接触面积
难度: 简单查看答案及解析
-
下列金属的冶炼方法与工业上冶炼铝的方法相同的是
A.Fe2O3+3CO
 2Fe+3CO2
2Fe+3CO2B.2Ag2O
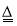 4Ag+O2↑
4Ag+O2↑C.Fe+CuSO4=FeSO4+Cu
D.2NaC1(熔融)
 2Na+C12↑
2Na+C12↑难度: 简单查看答案及解析
-
如图所示,有关化学反应和能量变化的说法正确的是
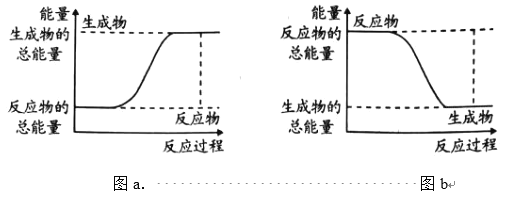
A.图 a 表示的是放热反应的能量变化
B.图 a 中反应物的总能量高于生成物的总能量
C.图 b 可以表示反应HCl+NaOH=NaCl+H2O的能量变化
D.图 b 所示反应不需要加热就能发生
难度: 简单查看答案及解析
-
某有机物的结构简式如图所示。下列关于该有机物的说法不正确的是
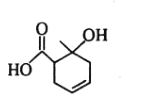
A.分子式为C8H11O2
B.能发生酯化反应
C.能使酸性 KMnO4溶液褪色
D.1 mol 该有机物最多能与1 mol H2发生加成反应
难度: 中等查看答案及解析
-
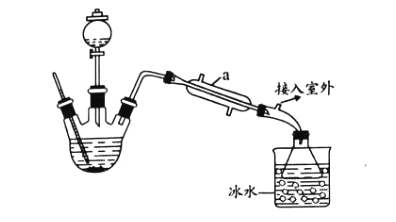
图是模拟煤的干馏实验装置。下列说法不正确的是
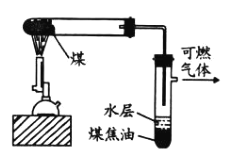
A.长导管的作用是导气和冷凝
B.可燃气体能用作基础化工原料
C.用分馏的方法从煤焦油中分离出苯
D.可用蓝色石蕊试纸检验水层液体中含有氨
难度: 简单查看答案及解析
-
X、Y、Z是短周期主族元素,X 的原子中只有1个电子,Y 的一种同位素在考古时用来测定文物的年代, Z 原子的最外层电子数是电子层数的 2倍,且其单质为黄色晶体。下列说法不正确的是
A.Z 为硫元素
B.原子序数:X<Y<Z
C.Y 的氢化物在常温常压下均为气体
D.YX4在光照条件下可与氯气发生反应
难度: 中等查看答案及解析
-
下列由实验得出的结论正确的是
实 验
结 论
A
在溴水中加入苯,振荡后水层接近无色
苯分子中含有碳碳双键
B
将乙烯通入溴的四氯化碳溶液,溶液变为无色且不分层
生成的 1, 2-二溴乙烷为无色、 可溶于四氯化碳的液体
C
用乙酸浸泡水壶中的水垢,可将其清除
碳酸的酸性大于乙酸的酸性
D
乙醇和水都可与金属钠反应产生氢气
乙醇分子羟基中的氢原子与水分子中的氢原子具有相同的活性
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
在隔绝空气条件下,11.12g FeSO4· nH2O受热脱水过程的热重曲线(固体质量随温度变化的曲线)如图所示,373℃时恰好完全失去结晶水。下列说法不正确的是
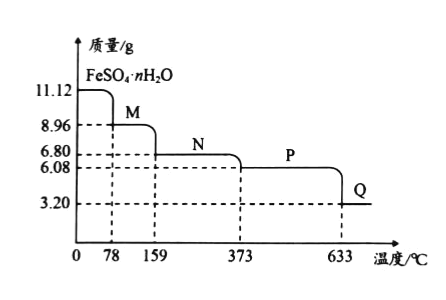
A.n=7
B.100℃时,所得固体M的化学式为FeSO4·5H2O
C.N生成P的化学方程式为FeSO4·H2O
 FeSO4+H2O
FeSO4+H2OD.将固体P加热至650℃,生成纯净固体Q的化学式为Fe2O3
难度: 中等查看答案及解析
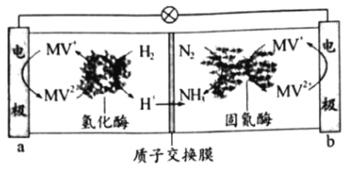
 2NH3(g),X,Y为反应体系中的两种物质,其浓度随时间变化关系如图所示:
2NH3(g),X,Y为反应体系中的两种物质,其浓度随时间变化关系如图所示:
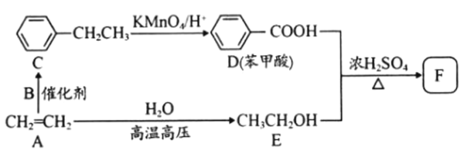

 CH3CH2OCH2CH3+ H2O
CH3CH2OCH2CH3+ H2O CH2=CH2↑ + H2O
CH2=CH2↑ + H2O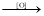 CH3COOH
CH3COOH
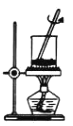 B.
B.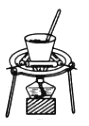 C.
C.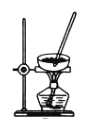 D.
D.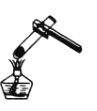
 存在,写出反应③得到I2的离子方程式_____。
存在,写出反应③得到I2的离子方程式_____。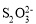 =2I-+
=2I-+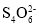 ),则废液中I2的含量为____mg/mL。
),则废液中I2的含量为____mg/mL。