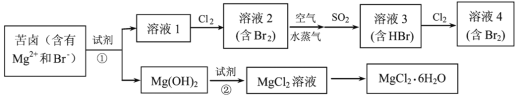
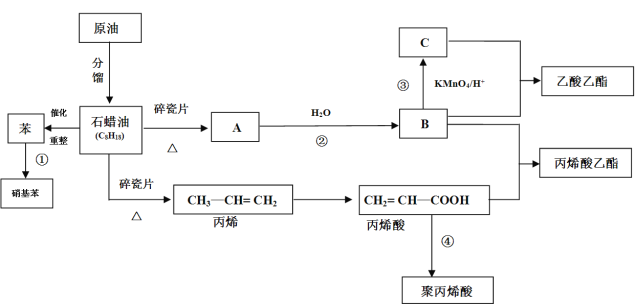
-
工业上或实验室提纯以下物质的方法不合理的是(括号内为杂质)( )
A.溴苯(溴):加NaOH溶液,分液
B.乙烷(乙烯):通入溴水,洗气
C.乙酸(水):加新制生石灰,蒸馏
D.乙酸乙酯(乙酸):加饱和碳酸钠溶液,分液
难度: 中等查看答案及解析
-
下列各组化合物中,只含有离子键的是( )
A.NaOH和NaHS B.CaCl2和Na2O
C.CO2和K2S D.H2O2和HCl
难度: 简单查看答案及解析
-
下列金属的冶炼中,通过在高温下加入还原剂来完成的是( )
A.Na B.Fe C.Al D.Ag
难度: 简单查看答案及解析
-
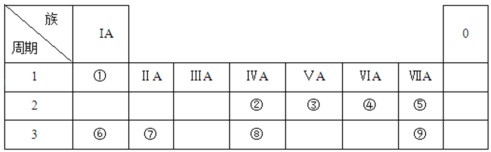
2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(37Rb)同周期。下列说法不正确的是
A.In是第五周期第ⅢA族元素
B.11549In的中子数与电子数的差值为17
C.原子半径:In>Al
D.碱性:In(OH)3>RbOH
难度: 中等查看答案及解析
-
下列说法正确的是
A.乙醇和乙醚(C2H5OC2H5)互为同分异构体 B.红磷和白磷属于同素异形体,燃烧产物相同
C.
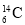 和
和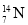 互为同位素 D.乙烯和苯乙烯属于同系物
互为同位素 D.乙烯和苯乙烯属于同系物难度: 简单查看答案及解析
-
下列化学用语表示正确的是
A.S2-的结构示意图:
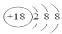
B.CO2的比例模型:

C.NH4Cl的电子式:
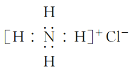
D.间硝基甲苯的结构简式:
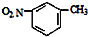
难度: 中等查看答案及解析
-
下列关于物质性质变化的比较,不正确的是
A.热稳定性:HF>HCl>HBr B.原子半径:Na>S>O
C.酸性强弱:H3PO4>H2SO4>HClO4 D.金属性强弱:K>Na>Li
难度: 中等查看答案及解析
-
今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是
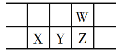
A.原子半径:W<X
B.常温常压下,Y单质为固态
C.气态氢化物热稳定性:Z<W
D.X的最高价氧化物的水化物是强碱
难度: 中等查看答案及解析
-
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第ⅤA族,甲与丙同主族,丁原子最外层电子数与电子层数相等,则下列说法正确的是
A.原子半径:丁>丙>乙
B.单质的还原性:丁>丙
C.甲、乙、丙的氧化物均为共价化合物
D.乙、丙、丁的最高价氧化物对应的水化物能相互反应
难度: 中等查看答案及解析
-
用NA表示阿伏伽德罗常数,下列说法不正确的是
A.3g3He中含有的中子数为1NA
B.1molOH-含有的质子数为9NA
C.标准状况下,2.24LCCl4中含有的共价键数目为0.4NA
D.标准状况下,11.2L甲烷和乙烯的混合物中含氢原子数目为2NA
难度: 简单查看答案及解析
-
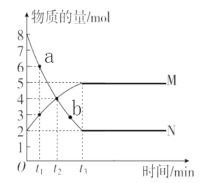
反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述正确的是
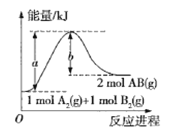
A.该反应是放热反应
B.1molA2(g)和1molB2(g)的总能量高于2molAB(g)的能量
C.该反应需要加热才能进行
D.1molA2(g)和1molB2(g)反应生成2molAB(g)吸收(a-b)kJ热量
难度: 中等查看答案及解析
-
氢气在氧气中燃烧产生淡蓝色火焰,在反应中,破坏1molH-H键吸收的能量为Q1kJ,破坏1molO=O键吸收的能量为Q2kJ,形成1molH-O键释放的能量为Q3kJ。下列关系式正确的是( )
A.2Q1+Q2>4Q3 B.2Q1+Q2<4Q3
C.Q1+Q2<Q3 D.Q1+Q2=Q3
难度: 简单查看答案及解析
-
下列装置能构成原电池的是( )
A.
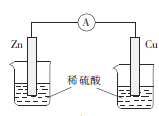 B.
B.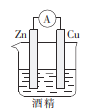
C.
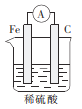 D.
D.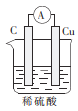
难度: 简单查看答案及解析
-
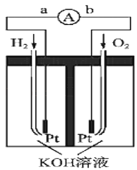
某课外活动小组设计化学电源使LED灯发光,装置如图。下列说法不正确的是
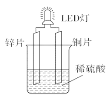
A.装置中存在“化学能→电能→光能”的转化
B.铜片上的反应为2H++2e‾=H2↑
C.电子由铜片经LED灯流向锌片
D.若将锌片换成铁片,电路中的电流方向不变
难度: 中等查看答案及解析
-
Al-Ag2O电池是水下大型机械常用电源,原理如图所示。该电池工作时总反应式为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则下列说法错误的是
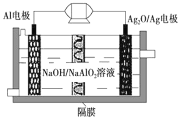
A.Al电极为负极
B.Al电极的反应式为Al-3e-+4OH-=AlO
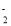 +2H2O
+2H2OC.放电时,电池正极附近溶液pH降低
D.放电时,Na+移向Ag2O/Ag电极
难度: 中等查看答案及解析
-
对于反应C(s)+H2O(g)⇋CO(g)+H2(g),当其他条件不变时,下列措施能加快反应速率的是
A.增加C的质量 B.恒容条件下充入氦气
C.降低温度 D.压缩容器体积
难度: 简单查看答案及解析
-
对于反应A(g)+3B(g)=2C(g)+D(g),下列反应速率最快的是
A.v(A)=0.3mol·L-1·min-1 B.v(B)=0.6mol·L-1·min-1
C.v(C)=0.5mol·L-1·min-1 D.v(D)=0.01mol·L-1·s-1
难度: 简单查看答案及解析
-
一定温度下,体积固定的密闭容器中,发生反应H2(g)+I2(g)⇋2HI(g)。下列能说明该反应一定达到平衡状态的是
A.单位时间内断裂1molH-H键,同时生成2molH-I键
B.容器内压强保持不变
C.容器内气体颜色保持不变
D.容器内H2、I2和HI的分子数之比为1:1:2
难度: 简单查看答案及解析
-
下列属于加成反应的是
A.乙烯能使酸性KMnO4溶液褪色 B.甲烷和氯气混合光照,黄绿色变浅
C.将苯与液溴在铁粉作用下反应 D.苯与氢气反应生成环己烷
难度: 简单查看答案及解析
-
某有机物M的结构如图,下列有关说法不正确的是
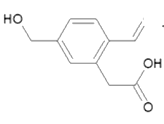
A.分子式为C11H12O3
B.能发生加聚、酯化反应
C.1molM能与2molNaOH反应
D.能使酸性KMnO4褪色
难度: 简单查看答案及解析
-
对三联苯是一种有机合成中间体,工业上合成对三联苯的化学方程式为:
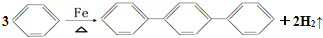 。下列说法不正确的是
。下列说法不正确的是A.上述反应属于取代反应 B.对三联苯的一溴代物有4种
C.对三联苯所有原子可能共平面 D.对三联苯可溶于水
难度: 中等查看答案及解析
-
从海带中提取碘的实验过程中,涉及下列操作,其中正确的是
A.将海带燃烧成灰
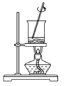 B.过滤得含I-溶液
B.过滤得含I-溶液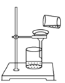
C.放出碘的苯溶液
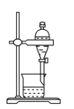 D.分离碘并回收苯
D.分离碘并回收苯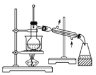
难度: 简单查看答案及解析
-
下列说法正确的是
A.煤的干馏和石油的分溜原理相同
B.直馏汽油和裂化汽油均能使酸性KMnO4溶液褪色
C.淀粉和纤维素水解产物相同
D.油脂和蛋白质均属于高分子化合物
难度: 简单查看答案及解析