-
等质量的氢氧化钠溶液和稀盐酸混合后,若所得溶液pH=7,则( )
A.所用氢氧化钠溶液和稀盐酸的溶质质量分数相等
B.混合溶液中钠离子与氯离子个数相等
C.混合前后水分子总数不变
D.混合前后阳离子总数不变
难度: 简单查看答案及解析
-
下列物质不能与稀硫酸发生反应的是
A. CuO B. Ag C. BaCl2 D. Mg(OH)2
难度: 中等查看答案及解析
-
下列物质存放在烧杯中一段时间后,质量变小且不变质的是( )
A.烧碱 B.浓硫酸 C.浓盐酸 D.生石灰
难度: 中等查看答案及解析
-
假设与排除是探索未知物的一种方法。《本草纲目拾遗》中记载:“强水性最烈,能蚀五金(金、银、铜、铅、铁)”,下列物质最可能是“强水”的是( )
A. 硫酸亚铁溶液 B. 稀盐酸 C. 浓硝酸和浓盐酸的混合物 D. 稀硫酸
难度: 中等查看答案及解析
-
运输下列物质时,应张贴“腐蚀品”标识的是( )

A.氢氧化钠 B.汽油 C.铁矿石 D.大理石
难度: 简单查看答案及解析
-
(2019郑州外国语一模)下列物质属于酸的是( )
A.BaCl2 B.H2SO4 C.Cu(OH)2 D.CaO
难度: 简单查看答案及解析
-
头发油腻是因为油脂的分泌,清洗时碱性溶液效果更好。从pH角度考虑效果最好的洗发水的pH为( )
A. 8 B. 7 C. 6 D. 4
难度: 简单查看答案及解析
-
下列溶液能使紫色石蕊溶液变成蓝色的是
A.澄清石灰水 B.NaCl溶液
C.稀硫酸 D.KNO3溶液
难度: 简单查看答案及解析
-
(2019北京)一些食物的pH范围如下,其中呈碱性的是( )
A.柠檬汁(2.0~3.0) B.番茄汁(4.0~4.4)
C.牛奶(6.3~6.6) D.鸡蛋清(7.6~8.0)
难度: 简单查看答案及解析
-
一些物质的近似pH如图,下列有关说法正确的是( )
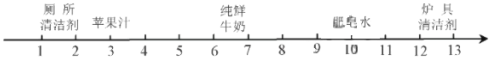
A.苹果汁的酸性比纯鲜牛奶的酸性弱。
B.肥皂水的碱性比炉具清洁剂的碱性强
C.厕所清洁剂与炉具清洁剂能混用
D.人被某些蚊虫叮咬后可涂抹肥皂水以减轻痛痒
难度: 简单查看答案及解析
-
(2019杭州)在①氧化铁②金属锌③氢氧化铜④氯化钡溶液四种物质中,跟稀硫酸、稀盐酸都能发生反应且反应中表现了“酸的通性”的组合是( )
A.①②③④ B.①②③
C.①③④ D.②③④
难度: 简单查看答案及解析
-
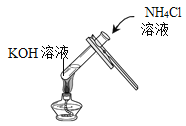
图中喷泉实验的现象与下列性质不相关的是
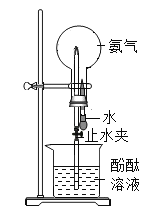
A.氨气密度比空气小
B.氨气易溶于水
C.氨气能与水反应
D.氨水显碱性
难度: 中等查看答案及解析
-
中和反应在工农业生产和日常生活中有广泛的应用。下列应用符合中和反应原理的是( )
A.蚊虫叮咬分泌的蚁酸可涂抹稀氨水消除
B.用熟石灰检验铵态氮肥
C.用硫酸铜和石灰乳配制农药波尔多液
D.用稀盐酸洗净久置石灰水试剂瓶瓶口上的白色固体
难度: 简单查看答案及解析
-
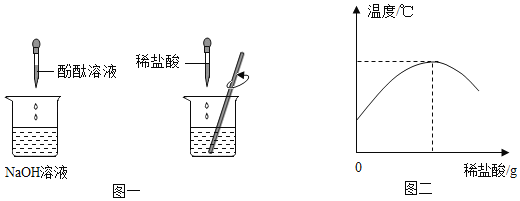
如图是室温下稀硫酸与氢氧化钠溶液反应过程中的pH变化曲线。下列有关说法正确的是( )
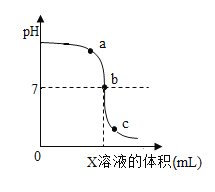
A.图中X是氢氧化钠
B.向图中a点所示溶液中加入几滴紫色石蕊溶液后,溶液变红
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4 + 2NaOH = Na2SO4+H2O
难度: 中等查看答案及解析
-
将4g镁和氧化镁的混合物加入100g稀硫酸中,恰好完全反应,则该稀硫酸的溶质质量分数可能是( )
A.5% B.10% C.20% D.30%
难度: 中等查看答案及解析
-
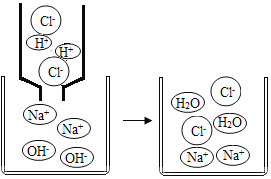
下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
A.
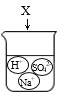 B.
B.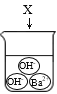 C.
C. D.
D.
难度: 中等查看答案及解析
-
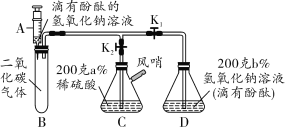
“化学棋”游戏规则:①每粒棋子代表一种物质;②吃子:所选棋子能与棋盘(如图)中的某棋子发生反应,则棋盘中的该棋子被吃掉;③连吃:前一次反应的生成物能与另一棋子发生反应时,则该棋子也被吃掉。若一次就可连续吃掉棋盘上的所有棋子,应选择的棋子是
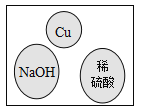
A.
 B.
B.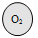 C.
C. D.
D.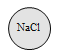
难度: 中等查看答案及解析
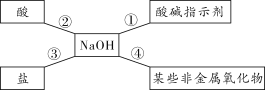
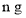 氢氧化钙与相同量盐酸反应,所得溶液中溶质的成分为____________。
氢氧化钙与相同量盐酸反应,所得溶液中溶质的成分为____________。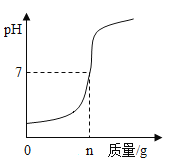
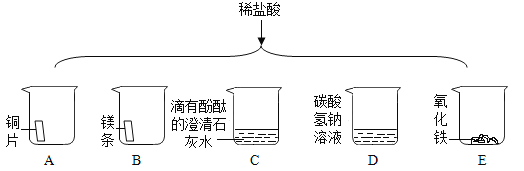
 2NaOH+Cl2↑+X↑。X的化学式为________(填字母代号)。
2NaOH+Cl2↑+X↑。X的化学式为________(填字母代号)。