-
能正确表示下列反应的离子方程式是
A. 在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O
B. NH4HCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32-
C. 氢氧化亚铁溶于稀硝酸中:Fe(OH)2+2H+=Fe2++2H2O
D. 澄清石灰水与过量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O
难度: 困难查看答案及解析
-
化学与生活、社会发展息息相关,下列说法错误的是
A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
C.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
D.古剑“湛泸”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
难度: 简单查看答案及解析
-
W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y。下列说法正确的是
A.Y的低价氧化物与O3漂白的原理相同
B.Y的氢化物和W2Y所含化学键的类型相同
C.上述三种元素形成的简单离子,X离子半径最小
D.工业上常用电解相应的盐溶液制备W、X的单质
难度: 中等查看答案及解析
-
下列分离物质的方法中,根据微粒大小进行分离的是( )
①分液 ②过滤 ③分馏 ④重结晶 ⑤渗析
A.②⑤ B.②④ C.①② D.①③⑤
难度: 简单查看答案及解析
-
下列有关物质结构的表述正确的是
A.次氯酸的电子式:
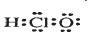 B.二氧化硅的分子式:SiO2
B.二氧化硅的分子式:SiO2C.CO2和CS2都是直线型分子 D.钠离子的结构示意图:
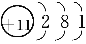
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值,下列说法正确的是
A.将162.5gFeCl3转化为氢氧化铁胶体后,氢氧化铁胶体粒子数等于NA
B.标准状况下,22.4LSO3中氧原子的个数约为NA
C.标准状况下,5.6L一氧化氮和5.6L氧气混合后的分子总数为0.5NA
D.标准状况下,用NaOH溶液吸收氯气22.4L,反应中转移的电子数目为NA
难度: 中等查看答案及解析
-
杀鼠灵是一种抗凝血性杀毒剂,其结构简式如图,下列说法正确的是( )
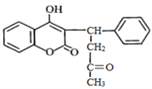
A. 分子中有1个手性碳原子 B. 遇FeCl3溶液显紫色
C. 1mol杀鼠灵最多能与9molH2反应 D. 能萃取碘水中的碘单质
难度: 困难查看答案及解析
-
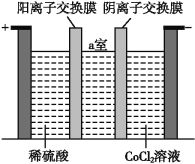
纯碱工业排放的废水中含少量Na2CO3,用三室式电渗析法处理可以得到氢气、氧气、浓度较高的碳酸和氢氧化钠溶液。下列说法正确的是
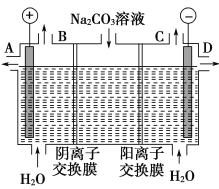
A.出口B导出的气体是H2
B.制得的氢氧化钠溶液从出口A导出
C.通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数
D.当有1molNa+通过阳离子交换膜时,会有0.5mol的O2生成
难度: 中等查看答案及解析
-
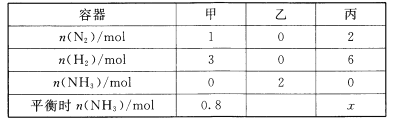
在一定温度时,容积为5L的某密闭容器中将1mol A和2mol B发生如下反应:A(s)+2B(g)
 C(g)+2D(g),经5min后,测得容器内B的浓度减少了0.2mol/L。下列叙述不正确的是( )
C(g)+2D(g),经5min后,测得容器内B的浓度减少了0.2mol/L。下列叙述不正确的是( )A.在5min内该反应用C的浓度变化表示的反应速率为0.02mol/(L·min)
B.5min时,容器内D的浓度为0.2mol/L
C.5min时容器内气体总的物质的量为3mol
D.当容器内压强保持恒定时,该可逆反应达到平衡状态
难度: 中等查看答案及解析
-
在混合体系中,确认化学反应先后顺序有利于问题的解决,下列反应先后顺序判断正确的是( )
A.在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+
B.在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:Fe3+、Cu2+、H+
C.在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:KOH、Ba(OH)2、BaCO3、K2CO3
D.在含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32-
难度: 中等查看答案及解析
-
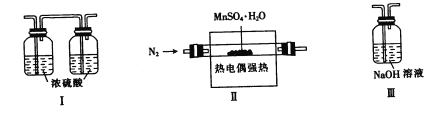
草酸亚铁(FeC2O4)可作为生产电池正极材料磷酸铁锂的原料,受热容易分解,为探究草酸亚铁的热分解产物,按下面所示装置进行实验。
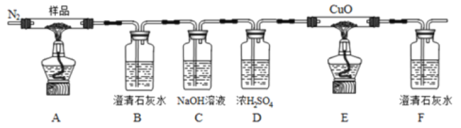
下列说法不正确的是
A.实验中观察到装置B、F中石灰水变浑浊,E中固体变为红色,则证明分解产物中有CO2和CO
B.反应结束后,取A中固体溶于稀硫酸,向其中滴加1~2滴KSCN溶液,溶液无颜色变化,证明分解产物中不含Fe2O3
C.装置C的作用是除去混合气中的CO2
D.反应结束后,应熄灭A,E处酒精灯后,持续通入N2直至温度恢复至室温
难度: 简单查看答案及解析
-
《Inorganic Syntheses》(无机合成)一书中,有一如图所示的装置,用以制备某种干燥的纯净气体。该装置中所装的药品正确的是( )
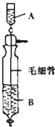
A.A中装浓盐酸,B中装浓硫酸
B.A中装浓硫酸,B中装浓盐酸
C.A中装氢氧化钠浓溶液,B中装浓氨水
D.A中装浓氨水,B中装氢氧化钠浓溶液
难度: 简单查看答案及解析
-
短周期主族元素W、X、Y、Z原子序数依次增大,W、Z位于同一主族,四种元素形成的一种化合物的结构如图所示。下列说法错误的是
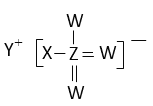
A.W的最简单氢化物稳定性比X的弱
B.Y与X、Z、W均能形成离子化合物
C.W与Y形成的化合物只含离子键
D.四种离子半径最大的是Z
难度: 中等查看答案及解析
-
pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用负对数值。如某溶液溶质的物质的量浓度为1×10-3mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。下列表达正确的是
A.中性溶液中,pC(H+)+pC(OH-)=14
B.pC(H+)=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol·L-1
C.pC(OH-)=a的氨水,稀释10倍后,其pC(OH-)=b,则a=b-1
D.pC(OH-)=3的NaOH溶液,稀释100倍,其pC(OH-)=5
难度: 中等查看答案及解析
-
亚氯酸钠(NaClO2)在溶液中对生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都是具有漂白作用。已知pOH=﹣lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析正确的是
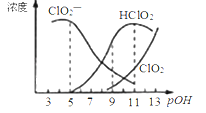
A.HClO2的电离平衡常数的数值Ka=10-8
B.pOH=11时,ClO2-部分转化成ClO2和Cl-离子的方程式为:5ClO2-+2H2O=4ClO2+ Cl-+4OH-
C.pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D.同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-)
难度: 困难查看答案及解析
-
某学生做如下实验:第一步,在淀粉KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列有关该同学对实验原理的解释和所得结论的叙述不正确的是( )
A.氧化性:ClO->I2>SO42—
B.蓝色消失的原因是Na2SO3溶液具有漂白性
C.淀粉KI溶液变蓝是因为I-被ClO-氧化为I2,I2使淀粉变蓝
D.若将Na2SO3溶液加入氯水中,氯水褪色
难度: 中等查看答案及解析
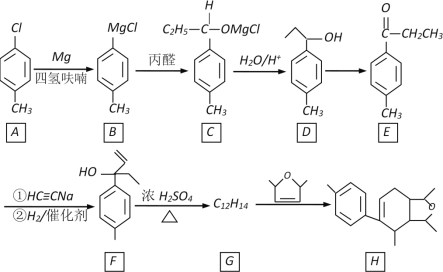
 的合成路线(无机试剂任选)_________。
的合成路线(无机试剂任选)_________。