-
十八大以来,我国科学技术迅猛发展。下列设备工作时,将化学能转化为电能的是
A. 锂离子电池
 B. 风力发电机
B. 风力发电机
C. 偏二甲肼燃烧
 D. 太阳能集热器
D. 太阳能集热器
难度: 简单查看答案及解析
-
下列化学用语表达正确的是
A.丙烷的结构简式:
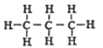 B.S2-的结构示意图:
B.S2-的结构示意图: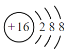
C.醋酸的分子式:CH3COOH D.CO2 的电子式:
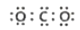
难度: 简单查看答案及解析
-
下列各组微粒或物质的相互关系,属于同位素的是
A.
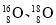 B.正丁烷、异丁烷
B.正丁烷、异丁烷C.CH4、C3H8 D.金刚石、石墨
难度: 简单查看答案及解析
-
下列关于化学与生产、生活的认识不正确的是
A.SO2和氮氧化合物(NOx)是形成酸雨的主要物质
B.煤的干馏是指将煤隔绝空气加强热使之分解的过程
C.葡萄糖、油脂、蛋白质都是高分子化合物
D.合理开发利用“可燃冰”(固态甲烷水合物)有助于缓解能源紧缺
难度: 中等查看答案及解析
-
以下金属都需要通过电解法冶炼得到的是
A.K、Na B.Mg、Cu C.Fe、Ag D.Au、Pt
难度: 简单查看答案及解析
-
2020年新春之际,出现了罕见的新型冠状病毒肺炎,威胁着人们的身体健康。以下消毒剂可以有效地灭活病毒,走进了百姓的生活中。下列叙述中,不正确的是
A.高锰酸钾(KMnO4)是电解质
B.H2O2分子中所有原子都达到了8电子结构
C.次氯酸钠(NaClO)是离子化合物
D.医用酒精是体积分数为75%的乙醇溶液
难度: 简单查看答案及解析
-
下列反应属于吸热反应的是
A.生石灰和水的反应 B.木炭在氧气中燃烧
C.盐酸与氢氧化钠溶液的反应 D.氯化铵与氢氧化钡晶体混合搅拌
难度: 简单查看答案及解析
-
有关下列有机物的描述正确的是
A.
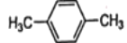 中苯环上的一氯代物有2种
中苯环上的一氯代物有2种B.CH4为正四面体结构
C.H3C-CH=CH2 中所有原子可能共平面
D.
 在FeBr3存在的条件下能与溴水反应
在FeBr3存在的条件下能与溴水反应难度: 中等查看答案及解析
-
以N2和H2为反应物,盐酸酸化的NH4Cl溶液为电解质的原电池,工作原理如图所示,下列说法不正确的是
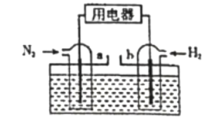
A.b电极为负极
B.反应过程中,溶液中的H+向a电极移动
C.a电极的电极反应式为N2+6e-+8H+=2NH
D.放电一段时间之后,溶液的酸性增强
难度: 中等查看答案及解析
-
"绿色化学"的理想状态是反应物的原子全部转化为目标产物。以下反应不符合绿色化学原则的是
A.工业生产环氧乙烷:2CH2=CH2+O2
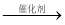
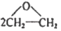
B.水煤气合成甲醇:CO+ 2H2
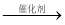 CH3OH
CH3OHC.铝热反应:2Al+ Fe2O3
 2Fe + Al2O3
2Fe + Al2O3D.合成甲基丙烯酸甲酯:
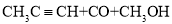
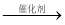
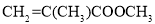
难度: 简单查看答案及解析
-
在温度和容积不变的条件下,可逆反应2NO2(g)⇌2NO(g)+O2(g).能表明该反应达到平衡状态的描述是
A.NO2、NO、O2各物质的浓度之比为2:2:1 B.容器内气体颜色不再变化
C.2v正(NO2)=v逆(O2) D.容器内气体的密度保持不变
难度: 中等查看答案及解析
-
将4molA气体和2molB气体充入到1L的密闭容器中,在一定条件下发生如下反应:2A(g)+ B(g)⇌2C(g)。经2s后达到平衡时,测得C的物质的量为1.2 mol。下列说法中正确的是
A.平衡时,A物质的浓度为2.8 mol·L-1
B.平衡时,B的转化率为70%
C.反应后混合气体的总物质的量为5.2mol
D.用C表示平均反应速率为1.2mol·L-1·s-1
难度: 中等查看答案及解析
-
下列有关实验装置进行的相应的实验,方法正确且能达到实验目的的是
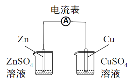
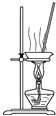
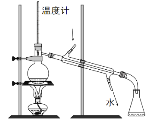
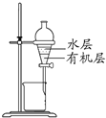
A.图1、检验电流的方向 B.图2、蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.图3、石油的分馏 D.图4、分离CCl4萃取碘水后的有机层和水层
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.48g正丁烷和10g异丁烷的混合物中共价键数目为13NA
B.3.4g羟基(-OH) 和3.4g氢氧根(OH-)均含有2NA个电子
C.7.8g 苯含有碳碳双键的数目为0.3NA
D.标准状况下,22.4L 由CHCl3和CH2Cl2组成的混合物中含有的分子数目为NA
难度: 中等查看答案及解析
-
环丙基乙烯(VCP)结构为
 ,下列关于该物质说法不正确的是
,下列关于该物质说法不正确的是A.环丙基乙烯属于烃类
B.该物质能发生取代反应、加成反应、聚合反应、氧化反应
C.环丙基乙烯与环戊二烯 (
 )互为同分异构体
)互为同分异构体D.环丙基乙烯的一氯代物有4种
难度: 中等查看答案及解析
-
以下X、Y、Z、W、R五种元素均为短周期元素,它们的化合价与原子序数的关系如图,下列说法正确
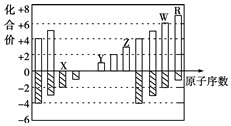
A.简单离子的半径: Y>Z>X
B.最高价氧化物对应水化物的酸性: R>W
C.单质的还原性: Z>Y
D.简单氢化物的沸点: W>X
难度: 中等查看答案及解析
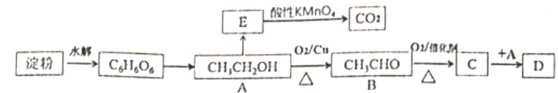
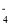 被还原为Mn2+,写出反应的离子方程式_______
被还原为Mn2+,写出反应的离子方程式_______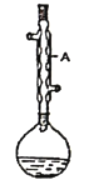
 等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、_____(填化学式),过滤之后,再加入适量盐酸。
等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、_____(填化学式),过滤之后,再加入适量盐酸。