-
酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧化合物
A.②④ B.②③ C.①③ D.①④
难度: 简单查看答案及解析
-
提出元素周期律并根据周期律编制出第一个元素周期表的科学家是( )
A.门捷列夫 B.拉瓦锡 C.道尔顿 D.阿伏加德罗
难度: 简单查看答案及解析
-
下列说法中,错误的是
A.化学的主要特点是在原子、分子水平上认识物质,化学可以识别、改变和创造分子
B.学习化学的基本方法有观察法、实验法、分类法、比较法等
C.化学反应过程中既有物质的变化,同时一定伴随着能量的变化
D.人们通过化学反应可以制造出新元素、新物质
难度: 简单查看答案及解析
-
在已知的化合物中,种类最多的是
A.过渡元素的化合物 B.第IIA族元素的化合物
C.第IVA族元素的化合物 D.第VA族元素的化合物
难度: 简单查看答案及解析
-
下列各组物质混合后,溶液呈蓝色的是
A.淀粉溶液与碘水 B.蛋白质溶液与浓硝酸
C.乙酸与氢氧化钠溶液 D.氨水与酚酞溶液
难度: 简单查看答案及解析
-
以下互为同位素的是
A.石墨与金刚石 B.D2和T2
C.正丁烷与异丁烷 D.35Cl和37Cl
难度: 简单查看答案及解析
-
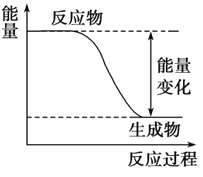
下列反应是吸热反应的是
A.碳酸钙受热分解 B.乙醇燃烧
C.镁与稀盐酸反应 D.氧化钙与水反应
难度: 简单查看答案及解析
-
下列说法正确的是
A.向蛋白质溶液中加入重金属盐溶液可使蛋白质产生盐析
B.油脂在碱性条件下水解生成高级脂肪酸和甘油
C.区别棉花和蚕丝的方法是灼烧后闻其是否有烧焦羽毛的气味
D.淀粉和纤维素组成都是(C6H10O5)n,二者属于同分异构体
难度: 简单查看答案及解析
-
下列关于煤、石油、天然气的叙述正确的是
A.煤的主要成分是单质碳
B.天然气是一种清洁的化石燃料
C.石油的分馏和裂化都是化学变化
D.塑料等合成材料只能以石油为原料制得
难度: 简单查看答案及解析
-
某元素最高价含氧酸的化学式是HRO4,则该元素气态氢化物的化学式可表示为
A.HR B.H2R C.RH3 D.RH4
难度: 简单查看答案及解析
-
下列物质中,既含有离子键,又含有共价键的是
A.KOH B.CO2 C.MgCl2 D.H2O
难度: 中等查看答案及解析
-
下列有关金属冶炼的说法错误的是( )
A.绝大多数金属的冶炼主要依据氧化还原反应原理
B.工业上可利用铝热反应炼铁
C.金属铝的冶炼可采取电解熔融氯化铝的方法
D.金属冶炼常会消耗许多能量,也易造成环境污染
难度: 中等查看答案及解析
-
已知15P、33As位于同一主族.下列关系正确的是( )
A. 原子半径:As>Cl>P B. 非金属性:Cl>S>As
C. 热稳定性:HCl>AsH3>PH3 D. 酸性:H3AsO4>H2SO4>H3PO4
难度: 简单查看答案及解析
-
工业生产硫酸时,其中一步反应是2SO2 + O2
 2SO3,下列说法错误的是( )
2SO3,下列说法错误的是( )A.增大氧气的浓度可提高反应速率
B.升高温度可提高反应速率
C.使用催化剂能显著增大反应速率
D.达到化学平衡时正逆反应速率相等且都为零
难度: 中等查看答案及解析
-
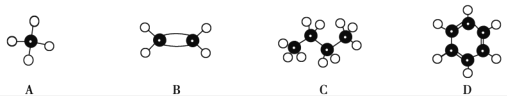
下列物质中,在一定条件下既能起加成反应,又能起取代反应,但不能使KMnO4酸性溶液褪色的是( )
A.苯 B.乙烷 C.乙烯 D.乙醇
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.1mol乙烯和乙醇的混合物完全燃烧时消耗O2的分子数为3NA
B.标准状况下,11.2LCCl4中含有的共价键数目为2NA
C.常温常压下,17g羟基中含有的电子总数为10NA
D.1mol苯分子中含有C=C双键数目为3NA
难度: 中等查看答案及解析
-
下列反应中,属于加成反应的是
A.2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
B.
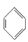 +HNO3
+HNO3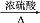
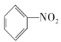 +H2O
+H2OC.CH3CH=CH2+Br2→
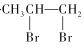
D.2CH3CH2OH+O2
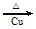 2CH3CHO+2H2O
2CH3CHO+2H2O难度: 简单查看答案及解析
-
下列说法正确的是
A.在化学反应中,化学能只可以转化为热能
B.合成氨工业中使用铁作催化剂可用来改变该反应的限度
C.NH4Cl受热固体消失和干冰升华只需克服分子间作用力
D.化学键的断裂和形成,是化学反应中能量变化的主要原因
难度: 简单查看答案及解析
-
下列实验操作和现象与结论关系不正确的是( )
操作和现象
结论
A
将大小相同的K和Na放入等体积的水中,钾比钠反应剧烈
钾元素的金属性比钠元素强
B
将Ba(OH)2·8H2O和NH4Cl晶体在小烧杯中混合搅拌,用手触摸烧杯外壁感觉变凉
Ba(OH)2·8H2O与NH4Cl的反应是吸热反应
C
在催化剂存在的条件下,石蜡油加强热生成的气体通入溴的四氯化碳溶液中,溶液褪色
石蜡油的分解产物都是烯烃
D
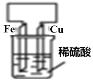
向盛有H2O2溶液的试管中,加入少量FeCl3溶液,产生气泡的速率比不加FeCl3溶液的快
FeCl3可以加快H2O2分解的速率,起了催化作用
A. A B. B C. C D. D
难度: 中等查看答案及解析