-
草木灰主要成分为碳酸钾,某实验小组取用20g草木灰置于烧杯中,将100g稀盐酸分四次加入,充分反应,测得数据如表所示,试计算
次数
累计加入盐酸的质量/g
烧杯内物质总质量/g
一
25
44.56
二
50
69.12
三
75
93.68
四
100
118.28
(1)最终产生二氧化碳的质量为_____ g
(2)所用稀盐酸的溶质质量分数_____。
难度: 中等查看答案及解析
-
某纯碱样品中含有少量氯化钠。为测定样品中碳酸钠的质量分数,现称取该样品11g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为56.6g。计算:
(1)完全反应后生成CO2的质量_______;
(2)纯碱样品中碳酸钠的质量分数_________(结果精确到0.1%)
难度: 困难查看答案及解析
-
小明称取5 g含有氯化镁的氯化钠样品于烧杯中,加入73.8 g水完全溶解,再逐滴加入80 g氢氧化钠溶液至恰好完全反应,将反应后混合物过滤,得到滤液的质量为153 g。
请计算:
(1)反应生成沉淀的总质量为多少g。
(2)所用氢氧化钠溶液的溶质质量分数。
难度: 中等查看答案及解析
-
某化学兴趣小组的同学到化学实验室,用铝和氢氧化钠溶液反应来制备氢气。同学们取了3g纯铝片和40g一定质量分数的氢氧化钠溶液,充分反应后,铝片有剩余,称得反应后剩余物质的总质量为42.7g。试计算:
(1)生成氢气的质量是_____g;
(2)所用氢氧化钠溶液的溶质质量分数为____。(提示:2Al+2NaOH+2H2O=2NaAlO2+3H2↑)
难度: 简单查看答案及解析
-
碱式碳酸铜是孔雀石的主要成分,俗称铜绿,化学式为Cu2(OH)2CO3,受热可分解生成CuO、水和二氧化碳。
(1)碱式碳酸铜的相对分子质量是_____。
(2)铜绿分解生成22g的二氧化碳的同时,生成CuO的质量是_____。
难度: 中等查看答案及解析
-
某化学兴趣小组同学在实验室做木炭还原氧化铁的实验时加入了过量的木炭。欲测定反应后混合物中铁的质量分数,他们取20 g样品于试管中,加入质量分数为20%的硫酸铜溶液至不再有红色物质析出,共消耗硫酸铜溶液200 g。计算混合物中铁的质量分数。
难度: 中等查看答案及解析
-
为测定实验室中某过氧化氢溶液的溶质质量分数,小明取25.0 g过氧化氢溶液放入烧杯中,然后进行如图20所示的实验。请计算:
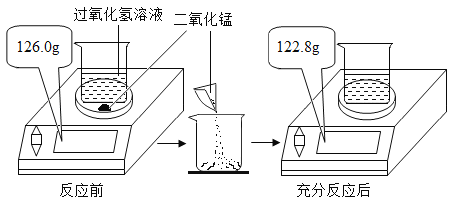
(1)反应后产生气体的质量为 g.
(2)此过氧化氢溶液的溶质质量分数。
难度: 中等查看答案及解析
-
某学习小组设计了图的实验,用稀盐酸测定100g被部分氧化的铜样品中铜的含量。请计算:
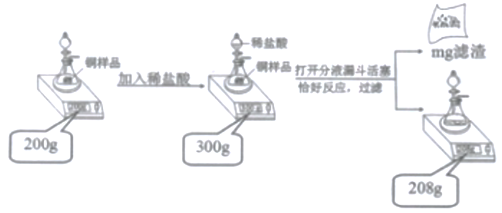
(1)m=________。
(2)所用稀盐酸中溶质的质量分数_____。
难度: 简单查看答案及解析
-
为测定实验室中一瓶未知浓度的烧碱溶液,小明同学根据如图所示实验过程和提供的数据进行分析计算。(注:滴入酚酞试液的质量忽略不计)
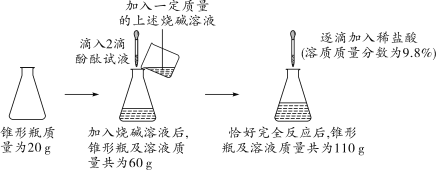
(1)所加稀盐酸的溶质质量是_____g。
(2)该瓶烧碱溶液的溶质质量分数。(计算结果精确至0.1%)
难度: 中等查看答案及解析
-
某同学发现,上个月做实验用的一瓶氢氧化钠固体忘记塞瓶塞(氢氧化钠露置在空气中易发生变质,生成碳酸钠)。 为了测定该样品中氢氧化钠的质量分数,某化学小组进行了如下实验:

请计算:
(1)反应后所得不溶物的质量是________g。
(2)该样品中氢氧化钠的质量分数。
难度: 中等查看答案及解析
-
(2019邢台三模)为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中分次加入相同溶质质量分数的氢氧化钠溶液,反应过程中的数据记录如下,请计算:
第一次
第二次
第三次
第四次
氢氧化钠溶液质量/g
10
10
10
10
反应后溶液质量/g
58.04
66.08
75.10
85.10
(1)反应生成沉淀的总质量是________g。
(2)该硫酸铜溶液中溶质的质量分数。
难度: 中等查看答案及解析
-
小明同学为了测定某Na2CO3溶液中溶质的质量分数,取10g该溶液与烧杯中,然后将400g澄清石灰水分四次加入,烧杯中沉淀的质量与每次加入澄清石灰水的质量关系如下表。
次数
第一次
第二次
第三次
第四次
加入澄清石灰水的质量/g
100
100
100
100
生成沉淀的质量/g
0.4
m
1.0
1.0
请计算:(1)表中m的值为______。
(2)Na2CO3溶液中溶质的质量分数。______
难度: 中等查看答案及解析
-
(2019江西改编)建造“南昌舰”的特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验:取20 g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。
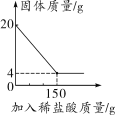
(1)20 g赤铁矿石样品中氧化铁的质量为________g。
(2)计算实验中所用稀盐酸的溶质的质量分数(写出计算过程)。
难度: 中等查看答案及解析
-
向200g NaCl和BaCl2的混合溶液中加入Na2CO3溶液。反应过程中滴加Na2CO3溶液的质量与生成沉淀的质量关系如图所示。请计算:
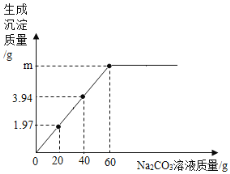
(1)m的值是_____g;
(2)原混合溶液中BaCl2的质量分数是多少_____?
难度: 中等查看答案及解析
-
为测定某工厂废水中硫酸的质量分数,小明进行下列实验:取49g废水样品于烧杯中,再逐滴加入溶质质量分数为10%的氢氧化钠溶液,并不断搅拌,实验过程中溶液pH的变化图像如图所示。
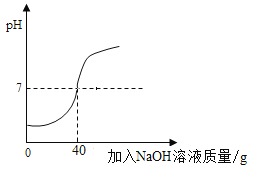
试计算:
(1)恰好完全反应时,加入氢氧化钠溶质的质量为____________g。
(2)此废水中硫酸的质量分数。_______
难度: 中等查看答案及解析
-
用图1所示装置制取氢气并测定稀硫酸中溶质的质量分数,将稀硫酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:
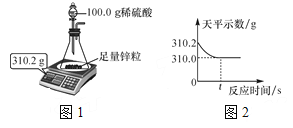
(1)共制取氢气________g;
(2)稀硫酸中溶质的质量分数是_______。
难度: 中等查看答案及解析
-
为测定某治疗胃酸的药片中碳酸氢钠的含量,小聪设计了如图的实验装置,取药片和足量的稀盐酸进行了三次实验(药品中其他成分不参与反应),采集的实验数据如表:
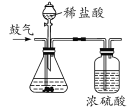
实验序号
1
2
3
药片样品质量/g
3.0
3.0
3.0
反应前总质量/g
194.5
195.0
194.3
反应后总质量/g
193.4
194.0
193.1
请计算:
(1)三次实验生成二氧化碳的平均质量是________g。
(2)该药片中碳酸氢钠的质量分数。
难度: 中等查看答案及解析
-
(2019大庆改编)钙是人体中的常量元素,因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用钙片。现将100 g盐酸分成五等份,逐次加到40 g某钙片制成的粉末中(其他成分不与盐酸反应),得到部分数据与关系图如下。请根据有关信息回答问题。
实验次数
第一次
第三次
第四次
加入盐酸的质量(g)
20
20
20
剩余固体的质量(g)
35
a
20
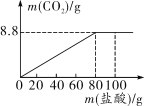
(1)a的值为________。
(2)该盐酸中溶质的质量分数是多少?(计算结果精确至0.1%)
难度: 中等查看答案及解析