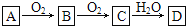-
下列有关SiO2的叙述正确的是
A.SiO2不与任何酸反应
B.玻璃中含有SiO2,所以不能用玻璃瓶盛装稀氢氧化钠溶液
C.SiO2是酸性氧化物,能与NaOH反应
D.SiO2能与水反应生成硅酸
难度: 简单查看答案及解析
-
下列各组物质的性质顺序,不正确的是
A.原子半径:Na<Mg<Al B.热稳定性:HCl>HBr>HI
C.酸性强弱:H2SiO4<H2CO3<H2SO4 D.熔点:SiO2>NaCl>CO2
难度: 中等查看答案及解析
-
熔融氢氧化钠反应选用的器皿是( )
A.陶瓷坩埚 B.石英坩埚
C.普通玻璃坩埚 D.生铁坩埚
难度: 简单查看答案及解析
-
根据表1信息,判断以下叙述正确的是( )
表1 部分短周期元素的原子半径及主要化合价
元素代号
L
M
Q
R
T
原子半径/nm
0.160
0.143
0.112
0.104
0.066
主要化合价
+2
+3
+2
+6、-2
-2
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
难度: 中等查看答案及解析
-
类推思想在化学学习与研究中经常被采用,但类推出的结论是否正确最终要经过实验的验证。以下类推的结论中正确的是( )
A.SO2能使酸性KMnO4溶液褪色,故CO2也能使酸性KMnO4溶液褪色
B.盐酸与镁反应生成氢气,故硝酸与镁反应也生成氢气
C.SO2能使品红溶液褪色,故CO2也能使品红溶液褪色
D.常温下浓硫酸能使铁和铝钝化,故常温下浓硝酸也能使铁和铝钝化
难度: 中等查看答案及解析
-
2013年3月23日20点30分开始“地球一小时”熄灯活动,今年的主题是:我做绿V客,“环保七选一,每周一起来”,以倡导节能减排理念。下列不能达到节能减排目的的是
A.利用太阳能制氢 B.用家用汽车代替公交车
C.利用化石燃料制造燃料电池 D.用节能灯代替白炽灯
难度: 简单查看答案及解析
-
自然界中存在的碘的稳定性核素是碘-127(
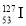 )。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(
)。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(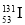 )。碘-131(
)。碘-131(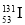 )一旦被人体吸入,就可能会引发甲状腺疾病。对于这两种核素的下列说法正确的是
)一旦被人体吸入,就可能会引发甲状腺疾病。对于这两种核素的下列说法正确的是A.
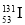 是一种新元素 B.
是一种新元素 B.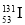 的摩尔质量为131g
的摩尔质量为131gC.
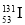 和
和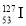 互为同位素 D.
互为同位素 D.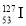 中子数与质子数之差为74
中子数与质子数之差为74难度: 简单查看答案及解析
-
导致下列现象的主要原因与排放SO2有关的是
A.酸雨 B.河水变质 C.臭氧空洞 D.温室效应
难度: 简单查看答案及解析
-
取四线湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加69%的硝酸、98.3%的硫酸、新制氯水、浓氨水,四张试纸最后呈现的颜色是 ( )
A.白、红、白、蓝 B.白、黑、白、蓝
C.白、白、白、蓝 D.红、黑、红、蓝
难度: 中等查看答案及解析
-
取少量无机盐溶液试样对其中的离子进行检验。下列判断正确的是( )
A.加入盐酸,产生白色沉淀,则试样一定有Ag+
B.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32-
C.加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则试样中一定有SO42-
D.加入NaOH溶液微热,产生能使湿润的红色石蕊试纸变蓝的气体,则试样中一定有NH4+.
难度: 中等查看答案及解析
-
某元素最高价氧化物对应的水化物的分子式是H4RO4,则其气态氢化物的分子式是( )
A.RH3 B.RH4 C.H2R D.HR
难度: 简单查看答案及解析
-
常用作环境分析指示物,通常有:2H、13C、15N、18O、34S等微粒,下列对它们的说法正确的是
A.34S原子核内的中子数为16 B.16O与18O互称同位素
C.13C和15N原子核内的质子数相差2 D.2H的核外电子数比1H多一个
难度: 简单查看答案及解析
-
下列气体易液化且遇挥发性酸时冒白烟,宜作制冷剂的是
A.N2 B.NH3 C.NO D.NO2
难度: 中等查看答案及解析
-
构成下列四种物质的微粒间,既存在离子键又存在共价键的是
A.K2S B.Na2O2 C.MgCl2 D.SO3
难度: 中等查看答案及解析
-
共价键、离子键和分子间作用力是粒子之间的三种不同作用力。下列物质的晶体中:①Na2O2②CO2③金刚石 ④NaCl ⑤白磷,含有上述两种作用力的是 ( )
A.①②⑤ B.①②③
C.②④⑤ D.②③⑤
难度: 简单查看答案及解析
-
下列有关物质结构的表述正确的是
A.次氯酸的电子式
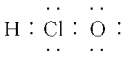
B.二氧化硅的分子式为SiO2
C.形成离子键的阴、阳离子间只存在静电吸引作用
D.钠原子的结构示意图
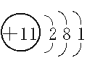
难度: 简单查看答案及解析
-
下列电子式中错误的是
A.Na+ B.
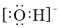 C.
C.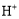
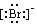 D.
D.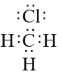
难度: 中等查看答案及解析
-
下列各项中表达正确的是 ( )
A.NH3分子的电子式:
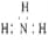 B.CH4分子的比例模型:
B.CH4分子的比例模型: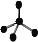
C.O原子的结构示意图:
 D.N2的结构式: N≡N
D.N2的结构式: N≡N难度: 中等查看答案及解析
-
根据化学反应的实质是旧键断裂、新键形成的观点,下列变化没有发生化学键断裂的是
A.电解水 B.干冰受热直接变成气体
C.HCl溶解于水 D.打雷放电时,O2变成O3
难度: 中等查看答案及解析
-
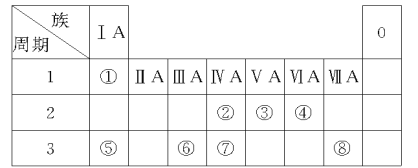
下表是元素周期表的一部分,有关说法正确的是( )
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
c
d
3
a
b
e
f
A.e的氢化物比d的氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.六种元素中,c元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )

A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.与H2化合,Z比W更容易
D.形成的气态氢化物溶于水,溶液呈碱性的是X
难度: 简单查看答案及解析
-
X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是
A.元素非金属性由强到弱的顺序是:Z>Y>X
B.Y元素最高价氧化物对应水化物的化学式可表示为H4YO4
C.3种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z>Y>X
难度: 简单查看答案及解析