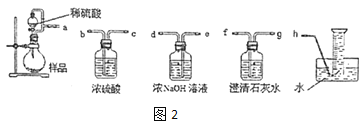
-
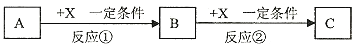
下列反应的离子方程式正确的是
A. 钠与水反应:Na+2H2O=Na++2OH-+H2↑
B. 过氧化钠与水反应:2Na2O2+2H2O=4Na++4OH-+O2↑
C. 向偏铝酸钠溶液中通入过量CO2气体:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D. 磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
难度: 中等查看答案及解析
-
在实验室中,通常将金属钠保存在( )
A. 水中 B. 煤油中 C. 四氯化碳中 D. 汽油中
难度: 中等查看答案及解析
-
下列关于Na和Na+的叙述中,错误的是
A. 它们相差一个电子层
B. 它们的化学性质相似
C. 钠原子,钠离子均为同一元素
D. 灼烧时,它们的焰色反应都呈黄色
难度: 中等查看答案及解析
-
下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是 ( )
①NaHCO3②Al2O3③Al (OH )3④Al.
A. ③④ B. ②③④ C. ①③④ D. 全部
难度: 中等查看答案及解析
-
下列物质中,不属于合金的是
A. 硬铝 B. 黄铜 C. 钢铁 D. 金箔
难度: 简单查看答案及解析
-
下列物质的用途错误的是( )
A. 明矾:净水剂
B. 过氧化钠:供氧剂和漂白剂
C. 氢氧化铝:胃酸中和剂
D. 生石灰:食品抗氧化剂
难度: 简单查看答案及解析
-
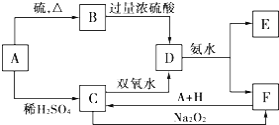
只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3四种溶液, 这种试剂是
A. BaCl2 B. H2SO4 C. NaOH D. AgNO3
难度: 中等查看答案及解析
-
下列有关 Na 2 CO3 与 NaHCO3 说法错误的( )
A. 两者均溶于水,但 NaHCO3 的溶解度小于 Na 2 CO3
B. 两者的溶液中加入澄清石灰水,均有白色沉淀生成
C. 向两者同浓度溶液中滴加几滴酚酞,前者溶液红色比后者深
D. NaHCO3 是发酵粉主要成分, Na 2 CO3 可用于治疗胃酸过多
难度: 中等查看答案及解析
-
小块金属钠投入到盛有 CuSO4 溶液的烧杯,不可能产生的现象是( )
A. 生成红色沉淀 B. 生成蓝色沉淀
C. 剧烈反应,钠浮在水面上 D. 钠熔化成闪亮的小圆球,并四处游动
难度: 中等查看答案及解析
-
下列除杂方法不合理的是( )
A. 除去硝酸钾中少量氯化钠:降温结晶
B. 除去镁粉中的铝粉:加过量氢氧化钠溶液,过滤
C. 除去 FeCl2 溶液中的 FeCl3:加过量铁粉,过滤
D. 除去 NaHCO3 溶液中的 Na 2 CO3 :加氯化钙溶液,过滤
难度: 中等查看答案及解析
-
甲、乙、丙、丁分别是 NaAlO2、NaHCO3、HCl、BaCl2 四种物质中的一种,将丁滴入乙中,先生成沉淀,后沉淀溶解。丁与甲混合时,无明显变化,则丙是( )
A. NaAlO2 B. NaHCO3 C. HCl D. BaCl2
难度: 中等查看答案及解析
-
下列实验现象与实际不符的是( )
A. 向酸性 KMnO4 溶液中加入适量 FeSO4 溶液:溶液紫红色褪去
B. 向紫色石蕊试液中加入过量 Na2O2:溶液先变蓝,后褪色
C. 向含有 Al(OH)3 的浊液中加入过量氨水:浑浊变澄清
D. 向 FeSO4 溶液中加入 NaOH 溶液:最后有红褐色沉淀生成
难度: 中等查看答案及解析
-
下列各组物质相互作用时,生成物不随反应条件或反应物用量改变而改变的是( )
A. Na 和 O2 B. NaOH 和 NaHCO3
C. NaOH 和 AlCl3 D. NaAlO2 和 HCl
难度: 中等查看答案及解析
-
下列有关离子检验的说法错误的是( )
A. 向某溶液中加入稀盐酸,产生无色无味的气体且可使澄清石灰水变浑浊,该溶液不一定含CO32-
B. 向某溶液中加入澄清石灰水,产生白色沉淀,该溶液不一定含 CO32-
C. 向某溶液中加入 BaCl2 溶液,产生白色沉淀,该溶液不一定含 SO42﹣
D. 用洁净铂丝蘸取某溶液在火焰上灼烧钾盐,不必透过蓝色钴玻璃
难度: 中等查看答案及解析
-
下列实验现象或表述正确的是( )
A. 在酒精灯上灼烧铝箔,会发现熔化的铝不断滴落
B. 检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加 KSCN 溶液 2~3 滴即可
C. 制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚 铁
D. 向饱和 FeCl3 溶液中滴入少量 NaOH 溶液,煮沸后即得红褐色 Fe(OH)3 胶体
难度: 中等查看答案及解析
-
下列物质不能通过化合反应直接生成的是( )
A. Fe(OH)3 B. Al(OH)3 C. FeSO4 D. NaHCO3
难度: 中等查看答案及解析
-
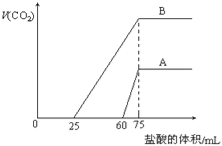
将0..4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
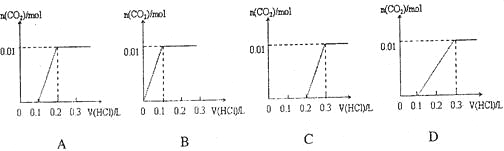
难度: 中等查看答案及解析
-
已知Cu+2Fe3+===2Fe2++Cu2+。向FeCl3、CuCl2的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是
A.加入KSCN溶液一定不变红色 B.溶液中一定含Fe2+
C.剩余固体中一定含Cu D.溶液中一定含Cu2+
难度: 中等查看答案及解析
-
已知 100mL MgCl2 和 AlCl3 混合溶液中,c(Cl-)=1.2mol/L,c(Mg2+)=0.3mol/L。欲使 Mg2+全部沉淀而分离出来,至少需 4 mol/L NaOH 溶液( )
A. 25mL B. 30mL C. 35mL D. 100mL
难度: 困难查看答案及解析
-
两种金属粉末的混合物52g,溶于足量的稀H2SO4中,生成标准状况下的氢气22.4L,则这种混合物不可能是
A、Na和K B、Mg和Al C、Cu和Al D、Al和Fe
难度: 简单查看答案及解析