-
半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是硅,下列有关硅及其化合物叙述正确的是( )
A. 水玻璃可做防火材料 B. 光导纤维的主要成分是高纯硅
C. 可用石英钳埚加热熔融氢氧化钠固体 D. 二氧化硅不和任何酸反应
难度: 中等查看答案及解析
-
要配制浓度约为2 mol·L-1NaOH溶液100 mL,下列操作正确的是( )
A. 称取8 g NaOH固体,放入100 mL量筒中,边搅拌边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL
B. 称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
C. 称取8 g NaOH固体,放入100 mL烧杯中,将烧杯中加满蒸馏水,同时不断搅拌至固体溶解
D. 用100 mL量筒量取40 mL 5 mol·L-1NaOH溶液,倒入250 mL烧杯中,再用同一量筒取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
难度: 简单查看答案及解析
-
下列关于硅单质及其化合物的说法正确的是 ( )
①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料
A. ①② B. ②③ C. ①④ D. ③④
难度: 简单查看答案及解析
-
NaHCO3和NaHSO4的溶液混合后,实际参加反应的离子是
A. H+和CO32− B. HCO3−和HSO4−
C. Na+、HCO3−和H+ D. HCO3−和H+
难度: 中等查看答案及解析
-
下列常用化学仪器中,不能直接用于混合物的分离或提纯的是( )
A. 普通漏斗 B. 锥形瓶 C. 分液漏斗 D. 蒸馏烧瓶
难度: 中等查看答案及解析
-
下列反应不是离子反应的是( )
A. 碳酸钠溶液中滴入氯化钙溶液 B. 金属钠在氯气中燃烧
C. 铁片置于硫酸铜溶液中 D. 氢氧化钡溶液与稀硫酸反应
难度: 中等查看答案及解析
-
将紫色石蕊试液滴入NaOH溶液中,溶液变蓝色,再通入氯气,溶液由蓝色先变成红色,最后颜色慢慢退去,其原因是
①氯气有漂白性 ②氯气与NaOH溶液反应 ③氯气的水溶液呈酸性 ④次氯酸有漂白性 ⑤氯化钠有漂白性
A. ①④ B. ②③④
C. ①②③ D. ④⑤
难度: 简单查看答案及解析
-
下列物质属于电解质的是( )
A. 铜 B. 食盐水 C. 烧碱 D. 蔗糖
难度: 简单查看答案及解析
-
下列各组物质间的反应中,不属于离子反应的是( )
A. Zn和H2SO4(稀)反应 B. NaCl溶液和AgNO3溶液反应
C. C和O2反应 D. Fe和CuSO4溶液反应
难度: 简单查看答案及解析
-
对下列实验过程的评价,正确的是
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体一定会有CO32-
B. 某溶液中滴加了Na2CO3溶液,生成白色沉淀,该溶液中一定会有Ba2+
C. 某无色溶液滴加酚酞试液显红色,该溶液不一定是碱液
D. 验证烧碱溶液中是否含Cl﹣,先加稀HCl除去OH﹣,再加AgNO3溶液,有白色沉淀出现,证明含Cl﹣
难度: 简单查看答案及解析
-
硫酸亚铁溶液含有杂质硫酸铜和硫酸铁,为除去杂质,提纯硫酸亚铁,应该加入下列哪种物质
A. 锌粉 B. 镁粉 C. 铁粉 D. 铝粉
难度: 中等查看答案及解析
-
关于氯的叙述中,下列正确的是( )
A. 氯气是一种黄绿色、有毒的气体
B. 氯元素在自然界中既可以以化合态存在,也可以以游离态存在
C. 氯气可用向下排空气法收集
D. 氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物
难度: 简单查看答案及解析
-
向紫色石蕊溶液中加入过量过氧化钠粉末,振荡,正确的叙述是( )
A. 最后溶液变蓝色 B. 溶液先变蓝色最后褪色
C. 溶液仍为紫色 D. 因为过氧化钠与石蕊发生氧化还原反应而无气泡产生
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 将金属钠置于空气中加热产生白色的氧化钠
B. 铝箔不易被点燃是因为铝与空气中的氧气不反应
C. 铁在空气中点燃剧烈反应,火星四射
D. 钠与氧气反应,本身作还原剂
难度: 简单查看答案及解析
-
某温度下,甲、乙两个烧杯中各盛有100 g相同浓度的氯化钾溶液,现将甲烧杯中的溶液蒸发掉35 g水,析出晶体5 g;将乙烧杯中的溶液蒸发掉45 g水,析出晶体10 g。则原溶液的质量分数为( )
A. 10% B. 15% C. 20% D. 25%
难度: 简单查看答案及解析
-
下列反应中,通入的气体只作还原剂的是( )
A. 二氧化硫通入溴水中
B. 氯气通入氢氧化钠溶液中
C. 二氧化硫通入氢氧化钾溶液中
D. 氧气通入亚硫酸溶液中
难度: 简单查看答案及解析
-
在实验室里,一定不能用同一套仪器制取的气体是( )
A. H2和Cl2 B. H2和O2 C. CO2和O2 D. H2和CO2
难度: 简单查看答案及解析
-
下列变化过程中属于氧化反应的是 ( )
A. MnO2→Mn2+ B. CuO →CuCl2
C. Ag+→Ag2O D. Sn2+→Sn4+
难度: 简单查看答案及解析
-
下列三个实验:①从食盐水中分离出氯化钠、②从酒精水溶液中分离出乙醇、③从碘水提取碘,其实验方法分别是( )
A. 蒸发、蒸馏、萃取 B. 萃取、蒸馏、蒸发
C. 蒸发、萃取、蒸馏 D. 蒸馏、萃取、蒸发
难度: 简单查看答案及解析
-
下列物质中含有的质子数最多的是( )
A. 27 g H2O B. 34 g H2O2
C. 51 g OH- D. 38 g H3O+
难度: 简单查看答案及解析
-
除去氧化铁中的氧化铝,可采用的试剂是( )
A. 盐酸 B. 硝酸 C. 氢氧化钠溶液 D. 氨水
难度: 简单查看答案及解析
-
下列关于硫酸铜溶液和氢氧化铁胶体的说法中,正确的是
A. 前者是混合物,后者是纯净物 B. 两者都具有丁达尔效应
C. 分散质的粒子直径均在1~100nm之间 D. 前者可用于杀菌,后者可用于净水
难度: 中等查看答案及解析
-
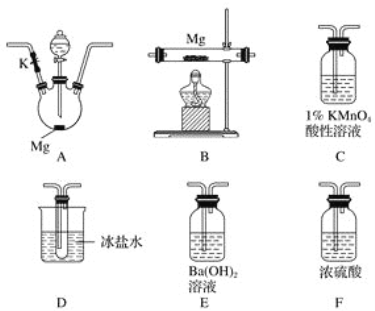
广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是( )
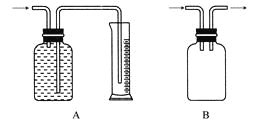
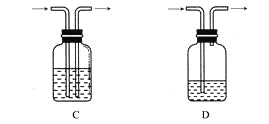
难度: 中等查看答案及解析
-
将2.3 g金属钠放入100 g水中,完全反应后溶液的质量分数为
A.
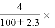 100% B.
100% B. 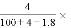 100%
100%C.
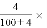 100% D.
100% D. 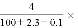 100%
100%难度: 简单查看答案及解析
-
将镁铝铁合金投入到300 mL硝酸溶液中,金属恰好完全溶解生成Mg2+、Al3+和Fe3+;硝酸全部被还原为一氧化氮,其体积为6.72 L(标准状况),当加入300 mL某浓度氢氧化钠溶液时,金属阳离子恰好全部沉淀,干燥后测得质量为27.2 g。下列有关推断正确的是( )
A. 参加反应的硝酸的物质的量为0.9 mol
B. 参加反应的金属的质量为11.9 g
C. 硝酸的物质的量浓度为3 mol·L-1
D. 氢氧化钠的物质的量浓度为6 mol·L-1
难度: 中等查看答案及解析
-
关于硫化氢气体在空气中完全燃烧的产物,叙述正确的是( )
①具有臭鸡蛋气味的气体;②是淡黄色的固体;③它能使溴水褪色;④它的水溶液具有酸性;⑤它具有氧化性和还原性。
A. 只有② B. 只有③ C. ①和④ D. ③、④和⑤
难度: 简单查看答案及解析
-
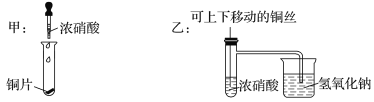
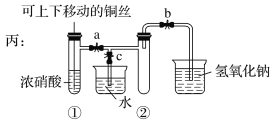
已知高锰酸钾与浓盐酸在常温下反应能产生氯气。若用下图所示的实验装置来制备纯净、干燥的氯气,并试验其与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
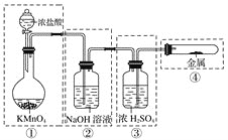
A. ①和②处 B. 只有②处
C. ②和③处 D. ②、③、④处
难度: 简单查看答案及解析
-
为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g样品加热,其质量变为w2g,则该样品的纯度(质量分数):
A.
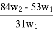 B.
B. 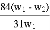 C.
C. 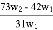 D.
D. 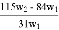
难度: 困难查看答案及解析