-
对化学反应限度的叙述不正确的是
①任何可逆反应都有一定的限度;
②化学反应的限度是不可改变的;
③化学反应的限度与时间的长短无关;
④化学反应达到限度时,正逆反应的速率相等;
⑤达到平衡时,反应停止了,正、逆反应速率都为零。
A. ①④ B. ②⑤ C. ②③ D. ⑤
难度: 中等查看答案及解析
-
Mg-AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
难度: 中等查看答案及解析
-
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.v(W)=3v(Z) B.2v(X)=3v(Z) C.2v(X)=v(Y) D.3v(W)=2v(X)
难度: 简单查看答案及解析
-
下列叙述正确的是 ( )
A.O2分子间存在着非极性共价键 B.CO2分子内存在着极性共价键
C.SO2与H2O反应的产物是离子化合物 D.盐酸中含有H+和Cl-,故HCl为离子化合物
难度: 简单查看答案及解析
-
下列过程中,共价键被破坏的是
A.碘升华 B.溴蒸气被活性炭吸附
C.葡萄糖溶于水 D.HCl气体溶于水
难度: 中等查看答案及解析
-
下列物质中,不属于烷烃的是
A. CH4 B. C3H8 C. C4H8 D. C5H12
难度: 中等查看答案及解析
-
下列有关性质的比较,不能用元素周期律解释的是
A.酸性;H2SO4>H3PO4
B.非金属性:Cl>Br
C.碱性:NaOH>Mg(OH)2
D.热稳定性:Na2CO3>NaHCO3
难度: 简单查看答案及解析
-
 C呼气法在医学上常用于幽门螺杆菌的诊断,下列关于
C呼气法在医学上常用于幽门螺杆菌的诊断,下列关于 C的说法正确的是
C的说法正确的是A.质子数是6 B.质量数是6 C.核外电子数是13 D.中子数是13
难度: 简单查看答案及解析
-
下列反应中生成物总能量高于反应物总能量的是( )
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
难度: 简单查看答案及解析
-
常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是
A.C2H5OH B.CH4 C.C2H4O D.C3H8
难度: 中等查看答案及解析
-
下列微粒中:其核外电子数①
 ②
② ③
③ ④F- 相同的是( )
④F- 相同的是( )A.①②③ B.②③④
C.①②④ D.①③④
难度: 简单查看答案及解析
-
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )

A. 两烧杯中铜片表面均无气泡产生
B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中溶液的pH均减小
D. 产生气泡的速度甲比乙快
难度: 简单查看答案及解析
-
下列反应既属于氧化还原反应,又属于吸热反应的是( )
A.铝片与稀盐酸的反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与CO2的反应 D.甲烷在氧气中的燃烧反应
难度: 简单查看答案及解析
-
X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-, Y+和Z-离子具有相同的电子层结构。下列说法正确的是
A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z- D.原子序数:X>Y>Z
难度: 中等查看答案及解析
-
下列比较中,正确的是( )
A.离子半径:S2->Cl->Na+>Mg2+ B.热稳定性:H2S<H2Se<HCl
C.酸性:HF>HCl>HBr>HI D.氧化性:F2>Cl2>P>S
难度: 中等查看答案及解析
-
分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
难度: 中等查看答案及解析
-
下列说法错误的是
A.食物放在冰箱中会减慢食物变质的速率
B.钾的金属性强,所以钾与水的反应比钠的反应强烈
C.2 mol SO2与1 mol O2混合反应后一定能生成2 mol SO3
D.面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸
难度: 简单查看答案及解析
-
下列石油加工过程属于物理变化的是( )
A.催化裂化 B.石油裂解 C.加热裂化 D.常压、减压分馏
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物
B.两种化合物组成元素相同,各元素质量分数也相同,则两者一定是同分异构体
C.相对分子质量相同的几种化合物,互称为同分异构体
D.组成元素的质量分数相同,且相对分子质量也相同的不同化合物,一定互为同分异构体
难度: 简单查看答案及解析
-
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应
 达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述正确的是( )
达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述正确的是( )
A.反应在c 点达到平衡状态
B.反应物浓度:
 点小于
点小于 点
点C.反应物的总能量低于生成物的总能量
D.
 时,SO2的转化率:
时,SO2的转化率: 段小于
段小于 段
段难度: 中等查看答案及解析
 中的质子数是___________,中子数是_________,核外电子数是__________.
中的质子数是___________,中子数是_________,核外电子数是__________.
 X,同时生成
X,同时生成 Z
Z 。
。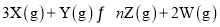 ,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算