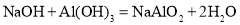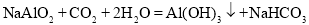-
蔬菜、水果里富含的营养素是
A.油脂
B.维生素
C.无机盐
D.蛋白质
难度: 简单查看答案及解析
-
下列气体会造成酸雨的是
A.氮气
B.氧气
C.水蒸气
D.二氧化硫
难度: 简单查看答案及解析
-
下列化肥属于氮肥的是
A.KCl
B.CO(NH2)2
C.K2SO4
D.Ca3(PO4)2
难度: 简单查看答案及解析
-
下列生活和生产中的做法错误的是
A.工业废水随意排放
B.洗手后及时关闭水龙头
C.合理使用化肥和农药
D.减少使用一次性塑料制品
难度: 简单查看答案及解析
-
补铁酱油、高钙奶粉中的“铁”“钙”指的是
A.单质 B.元素 C.原子 D.分子
难度: 简单查看答案及解析
-
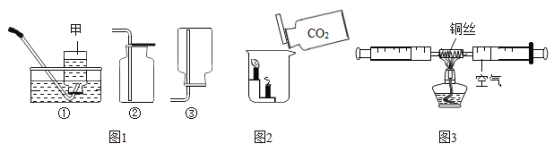
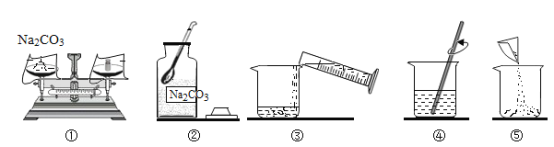
下列化学实验操作正确的是
A.闻气味
 B.滴加蒸馏水
B.滴加蒸馏水
C.引燃酒精灯
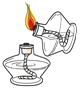 D.装入MnO2粉末
D.装入MnO2粉末
难度: 简单查看答案及解析
-
下列化学用语表示正确的是
A.氦气:He2
B.4个磷原子:P4
C.氟元素:F
D.1个氨分子:NH4
难度: 简单查看答案及解析
-
下列说法错误的是
A.密度最小的气体是H2
B.地壳中含量最多的元素是O
C.空气中含量最多的气体是N2
D.人体内含量最高的金属元素是Fe
难度: 简单查看答案及解析
-
下列关于溶液的说法正确的是
A.溶液都是无色的
B.冰水混合物不属于溶液
C.溶质一定是固体
D.均一的、稳定的液体叫做溶液
难度: 简单查看答案及解析
-
下列物质的用途和性质对应关系错误的是
A.钨——作灯丝——熔点高
B.氮气——作保护气——化学性质不活泼
C.一氧化碳——冶金工业——可燃性
D.二氧化碳——人工降雨——固体升华时吸热
难度: 中等查看答案及解析
-
燃料、能源与生活息息相关。下列说法错误的是
A.石油是一种可再生能源
B.加油站、油库等场所要严禁烟火
C.使用完燃气及时关闭阀门
D.炒菜时油锅着火,可用锅盖盖灭
难度: 简单查看答案及解析
-
下图是制取乙醇的反应微观示意图。下列说法正确的是
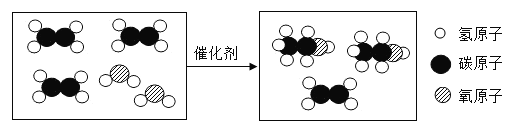
A.反应前后共有四种分子
B.反应物中只有一种物质是氧化物
C.反应前后催化剂的性质不变
D.参加反应的
 和
和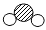 分子个数比是3:2
分子个数比是3:2难度: 中等查看答案及解析
-
某款锂电池中含有碳酸乙烯酯(C3H4O3)。下列有关碳酸乙烯酯的说法正确的是
A.碳酸乙烯酯中含有O3
B.碳酸乙烯酯的相对分子质量是88g
C.碳酸乙烯酯由碳、氢、氧三种元素组成
D.碳酸乙烯酯由3个碳原子、4个氢原子和3个氧原子构成
难度: 简单查看答案及解析
-
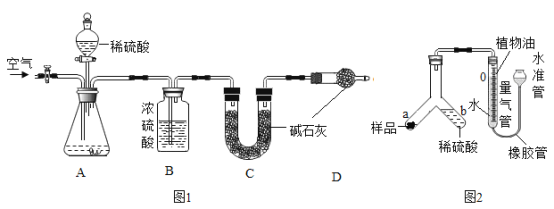
下列实验探究与结论不相符的是
选项
A
B
C
D
实验探究
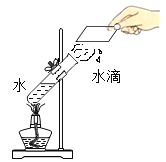
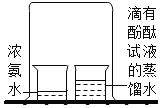
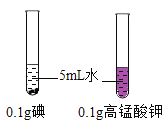
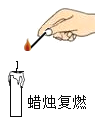
结论
水发生了化学变化
分子在不断运动
不同物质在同一溶剂中的溶解性不同
蜡烛熄灭时产生的白烟具有可燃性
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
根据初中化学所学知识判断,下列物质间的转化不能通过一步反应实现的是
A.C→CO
B.CO2→CO
C.CuSO4→CuCl2
D.KNO3→NaNO3
难度: 中等查看答案及解析
-
在反应
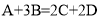 中,28gA与一定质量的B恰好完全反应,生成88gC。若C、D的相对分子质量之比为22:9,则A与B的相对分子质量之比为
中,28gA与一定质量的B恰好完全反应,生成88gC。若C、D的相对分子质量之比为22:9,则A与B的相对分子质量之比为A.7:8
B.8:7
C.7:24
D.24:7
难度: 中等查看答案及解析
-
如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是
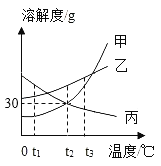
A.三种物质的溶解度大小关系为甲>乙>丙
B.t2℃时,将20g甲加入50g水中,得到70g溶液
C.t3℃时,用等质量的甲、乙、丙固体配成饱和溶液,需要水的质量大小关系是乙>甲>丙
D.将t2℃的三种物质的饱和溶液分别降温到t1℃,所得溶液的溶质质量分数大小关系为乙>丙>甲
难度: 中等查看答案及解析
-
下列各组物质在水中能大量共存且溶液为无色的是
A.HCl 、KNO3、 H2SO4、 NaCl
B.MgCl2 、KOH 、NaOH、 NaCl
C.NaCl 、HNO3、MgCl2 、K2CO3
D.NaNO3 、KCl 、FeCl3 、Ba(NO3)2
难度: 中等查看答案及解析
-
下列实验方法能达到实验目的的是
选项
实验目的
实验方法
A
鉴别碳粉和四氧化三铁粉末
观察颜色
B
除去生石灰中混有的碳酸钙
加入适量的稀盐酸,过滤
C
分离NaCl和CuCl2混合溶液
加入适量的NaOH溶液,过滤
D
除去KNO3溶液中混有的KCl
加入适量的AgNO3溶液,过滤
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
甲、乙、丙、丁是初中化学常见的物质,它们的转化关系如图所示(反应条件已省略)。下列说法正确的是
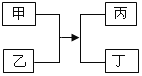
A.若丁是水,则该反应一定属于中和反应
B.若丙为沉淀,则甲、乙中一定有一种物质是盐
C.若甲、丁均为单质,则该反应一定属于置换反应
D.若乙是一种碱、丁是一种盐,则该反应一定属于复分解反应
难度: 困难查看答案及解析
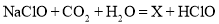 ,生成的HClO具有杀菌作用。化学方程式中X的化学式为______________,HClO中氯元素的化合价为___________________。
,生成的HClO具有杀菌作用。化学方程式中X的化学式为______________,HClO中氯元素的化合价为___________________。