-
下列物质的有效成分及用途对应正确的是
项目
A
B
C
D
名称
光导纤维
漂白粉
复方氢氧化铝抗酸药
小苏打
有效成分
Si
HClO
Al(OH)3
Na2CO3
用途
导电
作消毒剂
作抗酸剂
作发酵剂
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
珊瑚是由无数珊瑚虫分泌出的石灰质长期积淀而形成的。红珊瑚之所以是红色,最有可能的是含有
A.NO2 B.Fe3O4 C.Fe2O3 D.Al2O3
难度: 简单查看答案及解析
-
下列物质属于电解质的是
A.液氯 B.氨水 C.水玻璃 D.烧碱
难度: 简单查看答案及解析
-
下列化学概念的逻辑关系正确的是
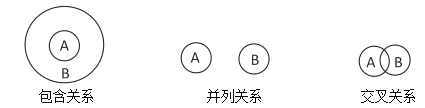
A.复分解反应和氧化还原反应属于包含关系
B.胶体与分散系属于交叉关系
C.过氧化钠与碱性氧化物属于包含关系
D.电解质与非电解质属于并列关系
难度: 简单查看答案及解析
-
下列有关离子检验的叙述正确的是
A.加入氯化钡溶液有白色沉淀生成,原溶液一定含有
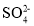
B.加入氢氧化钠溶液共热,有使蓝色石蕊试纸变红的气体生成,原溶液一定含有
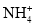
C.灼烧白色粉末火焰成黄色,原粉末中一定含有Na+
D.滴加KSCN溶液显红色,原溶液中一定含有Fe3+
难度: 简单查看答案及解析
-
同温同压下,相同体积的O2和SO2气体,下列叙述中错误的是
A.质量之比为1:2
B.物质的量之比1:2
C.密度之比为1:2
D.氧原子数比1:1
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A.28gN2和CO混合气体所含原子数目为2NA
B.0.3mol/LFeCl3溶液中含有Cl-为0.9NA
C.71gCl2完全反应后得到的电子数为2NA
D.22.4L氨气所含的分子数为NA
难度: 中等查看答案及解析
-
强酸性溶液中,下列离子组一定能大最共存的是
A.Mg2+、
 、
、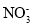 、
、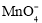
B.Ca2+、CH3COO-、Cl-、
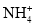
C.
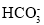 、Na+、Cl-、
、Na+、Cl-、
D.
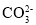 、
、 、Mg2+、Na+
、Mg2+、Na+难度: 中等查看答案及解析
-
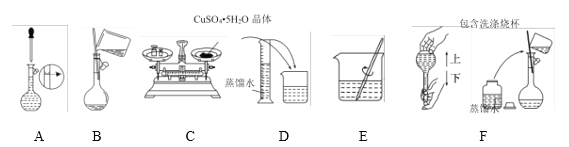
完成下列实验,不能达到实验目的的是
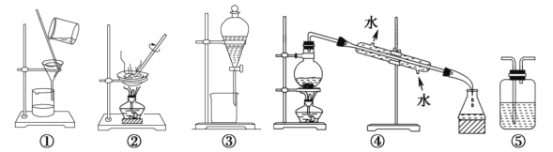
A.用海水制蒸馏水,选④
B.用CCl4提取碘水中的碘,选③
C.从NaCl溶液中获取NaCl晶体,选②
D.分离溶液和胶体,选①
难度: 中等查看答案及解析
-
下列说法正确的是
A.明矾有净水作用,可以做消毒剂
B.pH<7的降雨,称为“酸雨”
C.树林中的晨曦与丁达尔效应有关
D.赤潮的形成与CO2大最排放有关
难度: 简单查看答案及解析
-
下列氯化物既可以由氯气与金属反应制得,又可以由金属与盐酸反应制得的是
A.AlCl3 B.FeCl2 C.FeCl3 D.CuCl2
难度: 中等查看答案及解析
-
在呼吸面具中发生的氧化还原反应,氧化剂和还原剂的质量比是
A.39:22 B.1:2 C.2:1 D.1:1
难度: 简单查看答案及解析
-
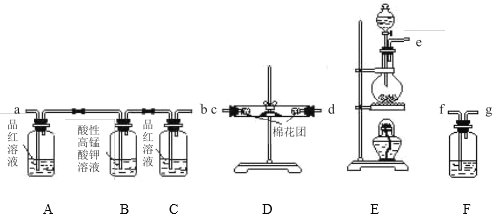
已知:氯化铁易吸收空气中的水分而潮解。某同学利用如图装置制备无水氯化铁,下列有关说法错误的是
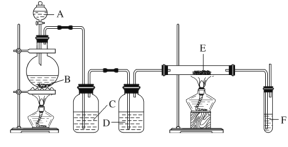
A.装置A的名称是分液漏斗
B.装置C、D中依次盛有浓硫酸、饱和食盐水
C.装置E和装置F之间缺少一个干燥装置,没法制得无水氯化铁
D.装置F的目的是吸收多余的尾气,以防污染空气
难度: 中等查看答案及解析
-
现有NH4Cl、(NH4)2SO4和K2SO4三种无色溶液,只用一种试剂,一次区别开,则该试剂是(必要时可以加热)( )
A.BaCl2溶液 B.Ba(OH)2溶液 C.稀盐酸 D.AgNO3溶液
难度: 中等查看答案及解析
-
某溶液中只含有K+、Al3+、Cl-、
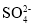 四种离子,已知K+、Al3+、Cl-的个数比为2:2:3,则溶液中 Al3+和
四种离子,已知K+、Al3+、Cl-的个数比为2:2:3,则溶液中 Al3+和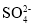 的个数比为
的个数比为A.4:5 B.1:3 C.2:3 D.1:4
难度: 简单查看答案及解析
-
下列溶液中含Cl-浓度最小的是
A.10mL0.1mol/L的FeCl3溶液
B.20mL0.1mol/LBaCl2溶液
C.30mL0.2mol/L的NaCl溶液
D.40mL0.1mol/L的KCl溶液
难度: 中等查看答案及解析
-
碘在地壳中主要以NaIO3形式存在,在海水中主要以I-形式存在。根据二者转化关系,下列说法错误的是

A.氧化性:I2>
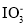
B.Cl2在两个反应中都是氧化剂
C.反应①的离子方程式为:2I-+Cl2=I2+2Cl-
D.反应②中,每消耗lmolCl2,电子转移2NA
难度: 简单查看答案及解析
-
下列反应中,没有明显颜色变化的是
A.FeCl3溶液中滴入KSCN溶液
B.浓硫酸滴在纸上
C.碳酸氢钠固体受热分解
D.含酚酞的烧碱溶液吸收氯气
难度: 简单查看答案及解析
-
从氧化还原的角度看,与水反应时过氧化铜(CuO2)和过氧化钠性质相似。将适量的过氧化铜投入过量稀硫酸中,可以观察到的现象是
A.无明显变化
B.最终生成蓝色沉淀
C.最终得到无色溶液
D.有无色无味气体生成
难度: 简单查看答案及解析
-
实验室用浓盐酸和二氧化锰制氯气。下列说法错误的是
A.浓盐酸在该反应中表现出酸性和还原性
B.该方法是瑞典化学家舍勒最先发现的
C.反应中电子转移4NA时,理论可以生成氯气22.4L
D.该反应的离子方程式为MnO2+4H++2Cl-
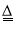 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O难度: 中等查看答案及解析
-
氮化硅陶瓷硬度大、熔点高,被广泛应用于各种热工领域。在烧结氮化硅陶瓷的过程中,二氧化硅、碳、氮气以物质的量之比3:6:2反应生成两种化合物。下列说法错误的是
A.烧结氮化硅陶瓷的反应属于氧化还原反应
B.氮化硅陶瓷可用于制造磨刀材料
C.氮化硅陶瓷不属于硅酸盐
D.产物中有CO2生成
难度: 简单查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A.钠与水反应:2Na+2H2O=2Na++2OH-+O2↑
B.往硫酸铝溶液中加过量氨水:
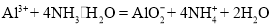
C.工业制漂白粉:Cl2+Ca(OH)2(石灰乳)=Ca2++Cl-+ClO-+H2O
D.NaHCO3溶液与NaOH溶液混合:
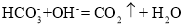
难度: 简单查看答案及解析
-
由Zn、Fe、Mg、Al四种金属中两种组成的20 g混合物与足量的盐酸反应产生2.0 g H2,则混合物中一定含有的金属是( )
A.Zn B.Fe C.Al D.Mg
难度: 中等查看答案及解析
-
将等体积、等浓度的硫酸铝、硫酸钾、硫酸铝钾三种溶液混合,测得该混合溶液中
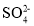 的物质的量浓度为0.4mol/L。取100mL混合液加入0.4mol/LKOH溶液,生成沉淀量最大时,加入的KOH溶液体积为
的物质的量浓度为0.4mol/L。取100mL混合液加入0.4mol/LKOH溶液,生成沉淀量最大时,加入的KOH溶液体积为A.50mL B.100mL C.150mL D.200mL
难度: 中等查看答案及解析
-
将镁、铝的混合物0.1mol溶于100mL2mol/LH2SO4溶液中,然后在所得溶液中滴加1mol/LNaOH溶液,沉淀的质量随加入NaOH溶液的体积变化如图所示。下列说法错误的是
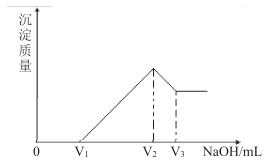
A.0~V1段发生的离子方程式为:H++OH-=H2O
B.V2~V3段发生的离子方程式为:
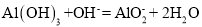
C.Mg2+、Al3+刚好完全沉淀时加入NaOH溶液的休积是400mL
D.若V1=160mL,则V3=500mL
难度: 中等查看答案及解析
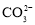 六种离子中的三种。向试管甲的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子中的三种。向试管甲的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题: