-
下列说法正确的是( )
A. 金属氧化物都是碱性氧化物
B. 盐中不一定有金属元素
C. 由同种元素组成的物质一定是单质
D. 非金属氧化物都是酸性氧化物
难度: 简单查看答案及解析
-
混合气体由N2和CH4组成,测得混合气体在标准状况下的密度是0.821g/L,则混合气体中N2和CH4的体积之比为( )
A.5∶1 B.4∶1 C.1∶4 D.1∶5
难度: 简单查看答案及解析
-
下列物质中既能跟稀硫酸反应, 又能跟氢氧化钠溶液反应的化合物是( )
①Al ②Al2O3 ③Al(OH)3④AlCl3 ⑤NaHCO3
A.①③④ B.②③⑤ C.②③④ D.全部
难度: 中等查看答案及解析
-
下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
A.NaHSO4和Ba(OH)2
B.AlCl3和NaOH
C.NaAlO2和H2SO4
D.Na2CO3和H2SO4
难度: 困难查看答案及解析
-
将钠、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积比是( )
A.1∶2∶3 B.6∶3∶2 C.3∶1∶1 D.1∶1∶1
难度: 中等查看答案及解析
-
下列物质可以用铝制容器存放的是
A.浓硝酸 B.稀硫酸 C.浓盐酸 D.浓氢氧化钠溶液
难度: 中等查看答案及解析
-
将0.1mol明矾溶于水形成100mL溶液,以下说法正确的是( )
A.明矾净水是利用了明矾的强氧化性
B.溶液的焰色反应为紫色,这是化学性质
C.加入Ba(OH)2溶液至沉淀物质的量达到最大,消耗Ba(OH)2溶液0.2mol
D.加入Ba(OH)2溶液至SO42-恰好完全沉淀,Al3+全部转化为AlO2-
难度: 中等查看答案及解析
-
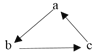
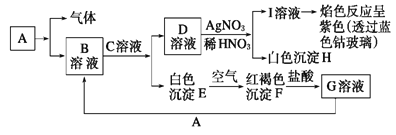
甲、乙、丙三种物质均含有铝元素,在溶液中的转化关系如图所示。下列说法正确的是
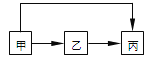
A.若甲是Al,丙是Al(NO3)3,则乙一定是NaAlO2
B.若甲是Al2O3,丙是NaAlO2,则乙一定是Al(NO3)3
C.若甲是Al(NO3)3,丙是NaAlO2,则乙一定是Al(OH)3
D.若甲是Al(OH)3,丙是Al(NO3)3,则乙一定是NaAlO2
难度: 中等查看答案及解析
-
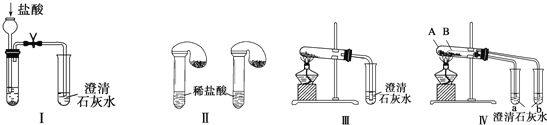
下列制取CO2、通过CO2和NaAlO2溶液制取Al(OH)3、分离并加热Al(OH)3制Al2O3的装置和原理能达到实验目的的是( )
A.制取CO2
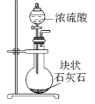 B.
B.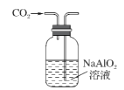 C.分离氢氧化铝
C.分离氢氧化铝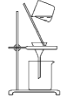 D.制氧化铝
D.制氧化铝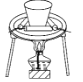
难度: 简单查看答案及解析
-
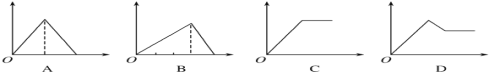
将一定质量的Mg和Al的混合物投入
 的稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示。则下列说法正确的是
的稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示。则下列说法正确的是
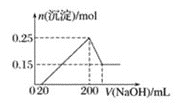
A.Mg、Al的混合物与
 的稀硫酸恰好完全反应
的稀硫酸恰好完全反应B.生成
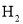 的体积为
的体积为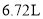
C.当加入20mL氢氧化钠溶液时,溶液中的溶质只有硫酸镁和硫酸铝
D.NaOH溶液的物质的量浓度为
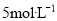
难度: 中等查看答案及解析
-
将Na2O2粉末投入到下列稀溶液中,既有气体又有沉淀产生的是
A.NaHCO3 B.FeCl3 C.NaCl D.HCl
难度: 中等查看答案及解析
-
以面粉为原料的网红“脏脏包”松软可口,通常用碳酸氢钠作发泡剂,因为它
①热稳定性差 ②增加甜味 ③产生二氧化碳 ④提供钠离子
A.①③ B.②③ C.①④ D.③④
难度: 中等查看答案及解析
-
跟Na、Na2O、Na2O2、NaOH、Na2CO3、NaHCO3六种物质都能发生反应的是( )
A.H2O B.CO2 C.Ca(OH)2 D.H2SO4
难度: 简单查看答案及解析
-
下列关于Na2CO3 和NaHCO3的叙述不正确的是
A.在相同情况下,Na2CO3 比NaHCO3易溶于水
B.温度相同,浓度相同Na2CO3 溶液的碱性比NaHCO3溶液碱性强
C.可用相同的离子方程式表示Na2CO3 和NaHCO3分别与Ca(OH)2溶液的反应
D.等质量的Na2CO3 和NaHCO3分别与足量的盐酸溶液反应,后者放出的CO2多
难度: 中等查看答案及解析
-
过氧化钠与足量的NaHCO3混合后,在密闭容器中充分加热,排除气体物质后冷却,残留的是( )
A.Na2CO3和Na2O2 B.只有Na2CO3
C.Na2CO3和NaOH D.Na2O和NaHCO3
难度: 简单查看答案及解析
-
等物质的量的N2、O2、CO2混合气体通过一定量Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为( )
A.6: 7: 3 B.3: 3: 2
C.3: 4: 1 D.6: 9: 0
难度: 中等查看答案及解析
-
为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g 样品加热,其质量变为w2 g ,则该样品的纯度(质量分数)是( )
A.
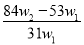 B.
B.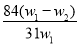 C.
C.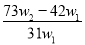 D.
D.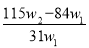
难度: 中等查看答案及解析
-
将CO2和O2的混合气体7.6g通入Na2O2 ,充分反应后,气体质量变为4.8g,原混合气体中O2的质量是( )
A.6.4g B.3.2g C.1.6g D.0.8g
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,4.48L水中含有水分子的数目为0.2NA
B.1molFe与足量水蒸气反应转移的电子数目为3NA
C.0.2mol/LCaCl2溶液中含有氯离子的数目为0.4NA
D.32 g O2和O3的混合气体所含原子数为2NA
难度: 中等查看答案及解析
-
下列物质反应后一定有+3价铁生成的是 ( )
①过量的Fe与Cl2反应②Fe与过量稀H2SO4反应③Fe和Fe2O3的混合物溶于盐酸中
A.只有① B.①② C.①②③ D.①③
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
①Na2O和Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2CO3和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀
③钠在常温下容易被氧化
④Na2O2可作供氧剂,而Na2O不行
⑤除去Na2CO3固体中混有的NaHCO3,将混合物加热至质量不再发生变化
⑥可用玻璃棒蘸取少量待测物质的浓溶液做焰色反应实验
A.③④⑤ B.②④⑥ C.②③④ D.①②⑥
难度: 中等查看答案及解析
-
检验某溶液中是否含有SO42-时,为防止Ag+、CO32-、SO32-等离子的干扰,下列实验方案比较严密的是
A.先加稀HCl将溶液酸化,再滴加BaCl2溶液,看是否生成白色沉淀;
B.先加稀HNO3将溶液酸化,再滴加BaCl2溶液,看是否生成白色沉淀;
C.向溶液中滴加稀盐酸酸化的BaCl2溶液,看是否生成白色沉淀;
D.向溶液中滴加稀硝酸酸化的BaCl2溶液,看是否生成白色沉淀;
难度: 中等查看答案及解析
-
下列溶液中,各组离子一定能大量共存的是( )
A.使酚酞试液变红的溶液:Na+、Cl-、SO
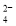 、Fe3+
、Fe3+B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO
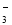 、Cl-
、Cl-C.碳酸氢钠溶液:K+、SO
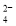 、Cl-、H+
、Cl-、H+D.碱性溶液中:K+、Ba2+、Cl-、NO3-
难度: 中等查看答案及解析
-
配制某物质的量浓度的溶液时,下列情况会造成所配溶液浓度偏小的是
A. 容量瓶中有蒸馏水 B. 溶液转移至容量瓶时,未洗涤玻璃棒和烧杯
C. 溶液未冷至室温就定容 D. 定容时俯视
难度: 中等查看答案及解析
-
溶液、胶体和浊液这三种分散系的本质区别是( )
A.是否有丁达尔现象 B.是否能通过滤纸
C.分散质粒子的大小 D.是否均一、透明、稳定
难度: 简单查看答案及解析
-
将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是( )
A.银、二氧化硫、硫酸、烧碱、食盐
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
难度: 简单查看答案及解析
-
下列现象或应用与胶体的性质无关的是
A.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
B.在河流入海处易形成沙洲
C.一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路
D.在豆浆里加入盐卤或石膏制成豆腐
难度: 简单查看答案及解析