-
W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y。下列说法正确的是
A. Y的低价氧化物与O3漂白的原理相同
B. Y的氢化物和W2Y所含化学键的类型相同
C. 上述三种元素形成的简单离子,X离子半径最小
D. 工业上常用电解相应的盐溶液制备W、X的单质
难度: 中等查看答案及解析
-
下列实验操作所得的现象及结论均正确的是
实验操作
现象及结论
A
将AlC13溶液加热蒸干
得到白色固体,成分为纯净的AlC13
B
将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液
有白色沉淀产生,则Na2SO3已变质
C
向Na2SiO3溶液中通入CO2
有白色沉淀产生,则碳酸的酸性比硅酸强
D
向FeI2溶液中通入少量C12
溶液变黄,则C12的氧化性强于Fe3+
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
化学与生活密切相关,下列有关说法不正确的是
A. 新能源汽车的推广与使用,有助于减少光化学烟雾的产生
B. 氯气泄漏时,可用蘸有肥皂水的湿毛巾捂住口鼻疏散到安全区域
C. 铁在潮湿的空气中放置,易发生化学腐蚀而生锈
D. 煤脱硫后产生的废料中含有的CaSO4 ,可用于制造建筑材料
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3+ + 4NH3•H2O = AlO2- + 4NH4+ + 2H2O
B.澄清石灰水与少量小苏打溶液混合:Ca2+ + OH- + HCO3- = CaCO3↓ + H2O
C.碳酸钙溶于醋酸:CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O
D.氯化铁溶液中加入单质铜:Fe3++Cu= Fe2+ + Cu2+
难度: 困难查看答案及解析
-
通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是
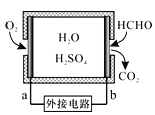
A.b为电池的负极,甲醛被氧化
B.a极的电极反应为O2+4e-+4H+==2H2O
C.传感器工作过程中,电解质溶液中硫酸的浓度不变
D.当电路中转移1×10-4 mol电子时,传感器内参加反应的HCHO为0.75 mg
难度: 困难查看答案及解析
-
已知反应mX(g)+nY(g)
 qZ(g)的△H < 0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g)的△H < 0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是A. 通入稀有气体使压强增大,平衡将正向移动
B. X的正反应速率是Y的逆反应速率的n/m倍
C. 增加X的物质的量,Y的转化率降低
D. 降低温度,混合气体的平均相对分子质量变大
难度: 中等查看答案及解析
-
常温下,用 0.01 mol·L-1NaOH溶液滴定 20.00 mL 0.01 mol·L-1CH3COOH溶液,所得滴定曲线如图。下列说法正确的是
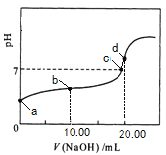
A. a点对应溶液的pH=2
B. b点对应的溶液中:c(OH-)+ c(CH3COO-) = c(Na+)+ c(H+)
C. c点表示NaOH溶液与CH3COOH溶液恰好完全反应
D. d点对应的溶液中,水的电离程度小于同温下纯水的电离程度
难度: 中等查看答案及解析
 CH3OCOOCH3(g)+H2O(g) △H=﹣15.5kJ•mol﹣1
CH3OCOOCH3(g)+H2O(g) △H=﹣15.5kJ•mol﹣1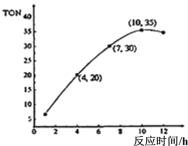
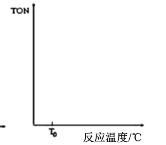
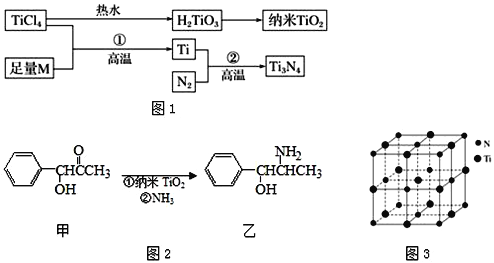
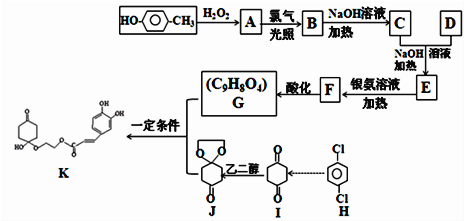
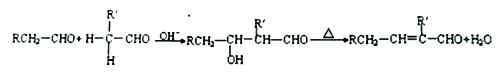
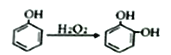
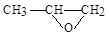 )发生类似反应G+J→K的反应,其生成物的结构简式为_____________________(写一种);
)发生类似反应G+J→K的反应,其生成物的结构简式为_____________________(写一种);