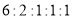-
分子式为C5H10O3的有机物与NaHCO3溶液反应时,生成C5H9O3Na,而与钠反应时生成C5H8O3Na2。则符合上述条件的同分异构体(不考虑立体异构)有
A.10种 B.11种 C.12种 D.13种
难度: 困难查看答案及解析
-
有机化合物分子中基团之间的相互影响会导致物质的化学性质不同。下列事实不可以用上述观点解释的是( )
A.苯不能与溴水发生取代反应,而苯酚能与溴水发生取代反应
B.乙醇不能与碱发生中和反应,而乙酸能与碱发生中和反应
C.2-甲基-1-丙醇能发生消去反应,2,2-二甲基-1-丙醇不能发生消去反应
D.乙烷不能使高锰酸钾溶液褪色,而甲苯能使高锰酸钾溶液褪色
难度: 中等查看答案及解析
-
化学与生活、社会密切相关,下列说法正确的是( )
A.医院一般用体积分数为95%的酒精消毒
B.聚乙烯塑料因发生加成反应而老化
C.以地沟油为原料生产生物柴油,可以提高资源的利用率
D.用氟利昂作制冷剂会加剧雾霾现象
难度: 简单查看答案及解析
-
下列化学用语表示不正确的是( )
A.甲烷的球棍模型:
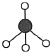 B.氯乙烷的结构简式:
B.氯乙烷的结构简式: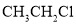
C.乙烯的空间填充模型:
 D.2-甲基-1-丁醇的键线式:
D.2-甲基-1-丁醇的键线式: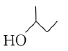
难度: 简单查看答案及解析
-
下列晶体中分类正确的一组是( )
选项
离子晶体
共价晶体
分子晶体
A
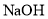
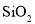
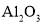
B
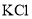
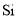
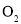
C
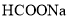
干冰
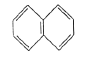
D
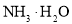
金刚石
玻璃
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列装置或操作能达到实验目的的是( )
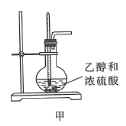
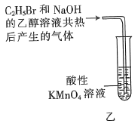
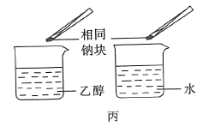
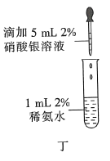
A.装置甲可用于实验室制备乙烯
B.操作乙可用于检验
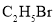 与
与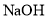 的乙醇溶液反应生成的气体中含有乙烯
的乙醇溶液反应生成的气体中含有乙烯C.操作丙可用于比较乙醇中羟基的氢原子和水分子中氢原子的活泼性
D.操作丁可用于配制银氨溶液
难度: 中等查看答案及解析
-
氯仿常因保存不慎而被氧化,产生剧毒物光气
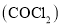 ,反应为
,反应为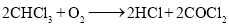 ,光气的结构式为
,光气的结构式为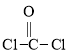 ,下列说法正确的是( )
,下列说法正确的是( )A.
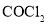 分子中所有原子的最外层都满足8电子稳定结构
分子中所有原子的最外层都满足8电子稳定结构B.
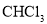 分子中含有4个
分子中含有4个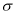 键,中心C原子采用
键,中心C原子采用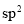 杂化
杂化C.
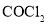 分子为含极性键的非极性分子
分子为含极性键的非极性分子D.
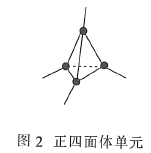
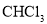 为正四面体结构
为正四面体结构难度: 简单查看答案及解析
-
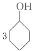
某有机物P的结构简式如图所示,下列关于有机物P的说法不正确的是( )
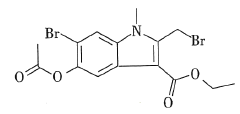
A.分子式为
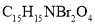
B.
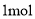
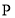 最多能与
最多能与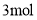
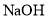 反应
反应C.苯环上的一氯代物有2种
D.分子中所有原子不可能处于同一平面
难度: 简单查看答案及解析
-
四种元素基态原子的电子排布式如下:①
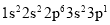 ;②
;②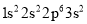 ;③
;③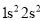 ;④
;④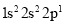 。下列有关比较中正确的是( )
。下列有关比较中正确的是( )A.第一电离能:④>③>②>①
B.原子半径:④>③>①>②
C.电负性:③>④>①>②
D.最高正化合价:④=①>③=②
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.甘油在一定条件下可以发生加聚反应
B.苯和氯气生成
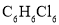 的反应是取代反应
的反应是取代反应C.丙烯和苯均能使溴水褪色,且褪色原理相同
D.分子式为
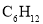 的烃,其核磁共振氢谱可能只出现一个峰
的烃,其核磁共振氢谱可能只出现一个峰难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.能层序数不相同,s原子轨道的形状不相同,但能量相同
B.钠原子由
 时,原子吸收能量,由基态转化为激发态
时,原子吸收能量,由基态转化为激发态C.在同一能级上运动的电子,其自旋方向肯定不同
D.原子价电子排布式为
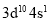 的元素,失电子,单质极易与水反应
的元素,失电子,单质极易与水反应难度: 简单查看答案及解析
-
砷化硼
 是一种具有超高热导率的新型半导体材料,其制备原理为
是一种具有超高热导率的新型半导体材料,其制备原理为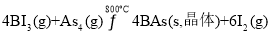 。下列说法错误的是( )
。下列说法错误的是( )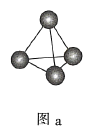

A.图a表示
 结构,
结构,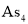 分子中成键电子对与孤电子对的数目之比为3:1
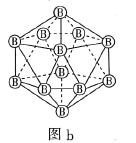
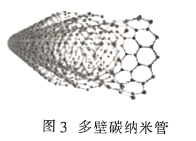
分子中成键电子对与孤电子对的数目之比为3:1B.图b表示晶态单质硼
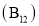 的基本结构单元,该基本结构单元为正二十面体
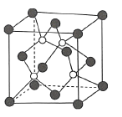
的基本结构单元,该基本结构单元为正二十面体C.图c表示
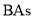 晶胞结构,
晶胞结构,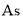 原子的配位数为4
原子的配位数为4D.该反应所涉及的元素中,I的原子半径最大
难度: 中等查看答案及解析
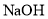 的水溶液,在加热条件下充分反应后,再加入稀硝酸酸化,最后滴加
的水溶液,在加热条件下充分反应后,再加入稀硝酸酸化,最后滴加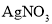 溶液可检验Z中的溴元素
溶液可检验Z中的溴元素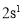
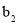 中
中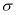 键与
键与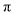 键的数目之比为
键的数目之比为
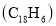 在铜片的催化作用下发生偶联反应得到。
在铜片的催化作用下发生偶联反应得到。
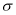 键的数目为________。
键的数目为________。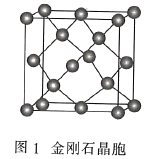
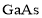 太阳能电池及铜铟镓硒薄膜太阳能电池等。
太阳能电池及铜铟镓硒薄膜太阳能电池等。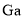 原子的价层电子排布式为_______________。
原子的价层电子排布式为_______________。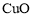 容易转化为
容易转化为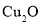 ,试从原子结构角度解释原因:_______________。
,试从原子结构角度解释原因:_______________。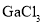 的立体构型为________。
的立体构型为________。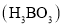 本身不能电离出
本身不能电离出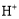 ,在水中易结合一个
,在水中易结合一个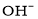 生成
生成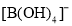 ,而体现弱酸性。
,而体现弱酸性。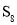 ,
,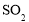 ,
,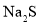 ,该三种物质中熔点最高的是________(填化学式)。
,该三种物质中熔点最高的是________(填化学式)。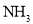 通入
通入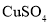 溶液中可以得到
溶液中可以得到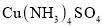 ,
,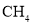 和
和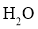 的价电子对数均为4,但键角不同,其原因是________。
的价电子对数均为4,但键角不同,其原因是________。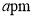 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为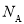 ,则磷化硼晶体的密度为________
,则磷化硼晶体的密度为________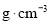 。
。
 ,实验装置如图所示。
,实验装置如图所示。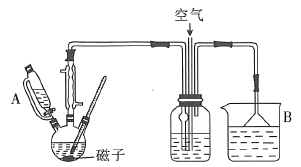
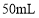 三颈烧瓶中,加入50%
三颈烧瓶中,加入50%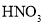 溶液(含
溶液(含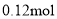
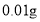 ),缓慢滴加5~6滴环己醇,有红棕色气体二氧化氮产生,将剩余的环己醇滴加完毕,总量为
),缓慢滴加5~6滴环己醇,有红棕色气体二氧化氮产生,将剩余的环己醇滴加完毕,总量为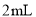 (约
(约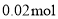 )。在温度为80~90℃时,反应至无红棕色气体逸出。将反应液倒入
)。在温度为80~90℃时,反应至无红棕色气体逸出。将反应液倒入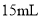 冷水洗涤,干燥后得到粗产品
冷水洗涤,干燥后得到粗产品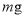 。
。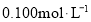 的
的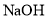 标准溶液进行滴定,下列操作可能使实际消耗
标准溶液进行滴定,下列操作可能使实际消耗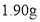 精制己二酸,则己二酸的产率为________(保留三位有效数字)。
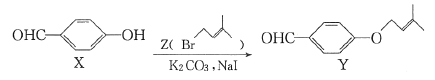
精制己二酸,则己二酸的产率为________(保留三位有效数字)。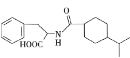 )的合成路线如下(略去部分反应条件):
)的合成路线如下(略去部分反应条件):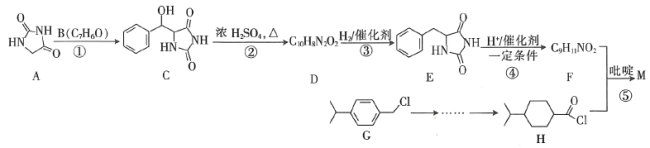
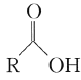
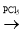
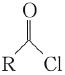
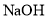 溶液反应
溶液反应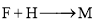 的化学方程式:________。
的化学方程式:________。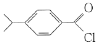 ),写出满足下列条件的I的同分异构体的结构简式:________。
),写出满足下列条件的I的同分异构体的结构简式:________。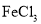 溶液发生显色反应
溶液发生显色反应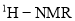 谱中峰面积之比为
谱中峰面积之比为