-
火神山和雷神山医院的建立挽救了众多生命,彰显中国力量。建设中涉及化学变化的是
A.平整场地 B.绑扎钢筋 C.拼接板材 D.消毒环境
难度: 简单查看答案及解析
-
武平百香果成为全国林改第一县的“致富果”,因含有丰富的铁、钾、磷和维生素,又被称为“ 健康果”。人体摄入铁元素能预防
A.佝偻病 B.贫血病 C.夜盲症 D.坏血病
难度: 简单查看答案及解析
-
近日新华社点赞生态文明建设长汀经验。下列做法不符合生态文明建设的是
A.随意排放生活污水 B.综合治理水土流失
C.推进污染防治攻坚 D.建立河流监控覆盖
难度: 简单查看答案及解析
-
Na3OCl 是一种良好的离子导体,可由以下方法制得:nNa+2NaOH+2NaCl=2Na3OCl+H2↑。反应的化学方程式中 n 的值为
A.1 B.2 C.3 D.4
难度: 简单查看答案及解析
-
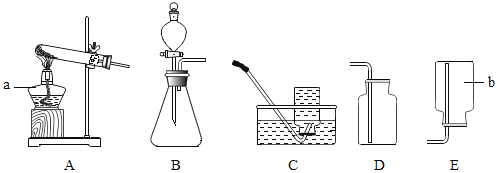
下列实验基本操作正确的是
A.
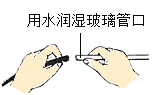 连接仪器
连接仪器B.
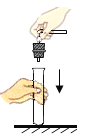 塞紧胶塞
塞紧胶塞C.
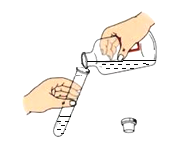 倾倒液体
倾倒液体D.
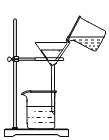 过滤
过滤难度: 简单查看答案及解析
-
合理膳食是人体健康的重要保证。下列说法不正确的是
A.每天应摄入一定量的蛋白质 B.油脂会使人发胖,故应禁食油脂
C.糖类是人体能量的主要来源 D.维生素是人体不可缺少的营养物质
难度: 简单查看答案及解析
-
救治新冠肺炎重症患者采用呼吸机能帮助患者增加氧气吸入量。下列关于氧气的说法,正确的是
A.通过化合反应也可以制得氧气 B.氧气既可燃烧,又支持燃烧
C.氧气与体内物质反应释放能量 D.供人呼吸的氧气,越浓越好
难度: 简单查看答案及解析
-
2019年12月3日,我市某沿街店铺突发大火,浓烟向上翻滚弥漫,消防队员对邻近的店铺进行打湿保护,历经一小时,现场明火被扑灭。下列说法不正确的是
A.店铺内的木质材料是易燃物
B.浓烟是由于可燃物不完全燃烧产生的
C.打湿保护是为了降低可燃物的着火点
D.市民发现火灾发生可拨打电话119报警
难度: 简单查看答案及解析
-
门捷列夫研究元素周期表时,预测铝的下方有一种化学性质与铝类似的“类铝”元素。1875 年法国化学家布瓦德朗发现了这种元素,命名为“镓(Ga)”。下列说法正确的是
A.镓是非金属元素
B.单质镓投入盐酸中不发生反应
C.镓的相对原子质量为 69.72g
D.镓在反应时容易失去 3 个电子转化为Ga3+
难度: 简单查看答案及解析
-
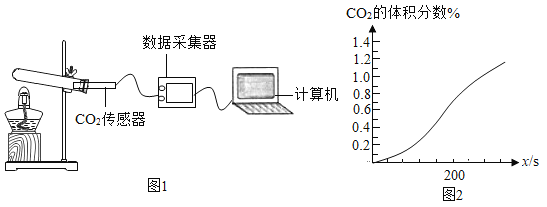
下图是测定空气组成实验的新设计,测定操作过程为:往有机玻璃管右侧装入足量的食品脱氧剂(主要成分为活性铁粉),并迅速向管的左侧注入一滴水,测出 AO 的长度为L1(图 1)。然后轻轻抖动玻璃管,使脱氧剂粉末平铺在玻璃管右侧,待水滴停止移动后,测得 AB 的长度为L2(图 2)。
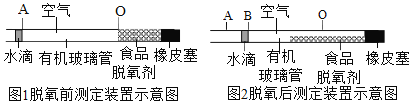
以下说法不正确的是
A.该实验是利用铁锈蚀原理测定空气中氧气的体积分数
B.将脱氧剂粉末平铺在有机玻璃管中的目的是加快反应速率
C.用该方法测得的空气中氧气的体积分数为(L1- L2)/L1×100%
D.用该方法测得的实验结果的精度与有机玻璃管的粗细有关
难度: 中等查看答案及解析