-
下列叙述中正确的是
A. 由金属元素和非金属元素形成的化合物一定是离子化合物
B. 完全由非金属元素形成的化合物一定是共价化合物
C. 离子化合物中只含有离子键
D. 共价化合物中只含有共价键
难度: 中等查看答案及解析
-
下列有关叙述中正确的是( )
A.14C与12C的性质完全不同
B.14C与14N含有的中子数相同
C.14C60和12C60是碳元素的同素异形体
D.14C与12C、13C互为同位素
难度: 中等查看答案及解析
-
下列微粒半径比较正确的是( )
A.Na+ >Na B.Cl- >Cl C.Ca2+ >Cl- D.Mg >Na
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.N、P同主族,PH3比NH3稳定
B.S、Cl同周期,S2-半径比Cl-的小
C.Na和K属于ⅠA族元素,K失电子能力比Na的强
D.P和N属于ⅤA族元素,H3PO4酸性比HNO3的强
难度: 简单查看答案及解析
-
下列各组元素性质的递变情况错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素最高正价依次升高
C.N、O、F原子半径依次增大
D.Na、K、Rb的电子层数逐渐增多
难度: 简单查看答案及解析
-
下列关于元素周期律的说法错误的是( )
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B.第二周期元素从Li到F,非金属性逐渐增强
C.因为Al在反应中失去3个电子而Mg失去2个电子,故金属性Al>Mg
D.O与S为同主族元素,且O比S的非金属性强
难度: 中等查看答案及解析
-
已知R2+核内共有N个中子,R的质量数为A,m g R2+中含电子的物质的量为( )
A.
 mol B.
mol B.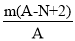 mol
molC.
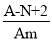 mol D.
mol D.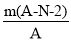 mol
mol难度: 中等查看答案及解析
-
如图是元素周期表中短周期的一部分,若A原子最外层电子数比次外层电子数少3,则下列说法正确的是( )

A.四种元素都是非金属元素
B.氢化物的还原性:D > B
C.A与C的原子序数之和跟B与D的原子序数之和相等
D.四种元素形成的单质在常温下都是气体
难度: 中等查看答案及解析
-
在用锌片、铜片和稀H2SO4组成的原电池装置中,经过一段时间工作后,下列说法中正确的是( )
A.锌片是正极,铜片上有气泡产生
B.溶液中H2SO4的物质的量减小
C.电流方向是从锌片流向铜片
D.电解质溶液的c(H+)保持不变
难度: 简单查看答案及解析
-
下列电子式书写错误的是( )
A.
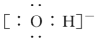
B.

C.
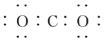
D.
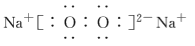
难度: 简单查看答案及解析
-
下列化合物中,只含共价键的是( )
A.Na2S B.CaCl2 C.NH4Cl D.CO2
难度: 简单查看答案及解析
-
在下列四种反应条件下,锌和盐酸反应速率最快的是( )
A.20 ℃时,将锌片放入0.01 mol·L-1的稀盐酸中
B.20 ℃时,将锌片放入0.1 mol·L-1的稀盐酸中
C.50 ℃时,将锌片放入0.01 mol·L-1的稀盐酸中
D.50 ℃时,将锌片放入0.1 mol·L-1的稀盐酸中
难度: 简单查看答案及解析
-
一定条件下,在固定容积的密闭容器中进行下列反应:N2(g)+3H2(g)
 2NH3(g),反应开始时,c(N2)=1.5 mol·L-1,c(H2)=4.5 mol·L-1,10 s后测得容器的压强变为开始时的
2NH3(g),反应开始时,c(N2)=1.5 mol·L-1,c(H2)=4.5 mol·L-1,10 s后测得容器的压强变为开始时的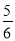 ,计算10 s内用H2表示的化学反应速率为( )
,计算10 s内用H2表示的化学反应速率为( )A.0.15 mol·(L·s)-1 B.0.2 mol·(L·s)-1
C.0.1 mol·(L·s)-1 D.0.015 mol·(L·s)-1
难度: 中等查看答案及解析
-
下列说法中正确的是( )
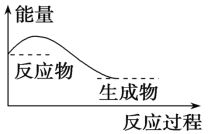
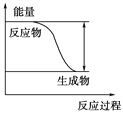
A.任何化学反应都伴随着能量的变化
B.H2O(g)→H2O(l)该过程放出大量的热,所以该过程是化学变化
C.化学反应中能量的变化都表现为热量的变化
D.对于如图所示的过程,是吸收能量的过程
难度: 简单查看答案及解析
-
石墨在一定条件下可转化为金刚石,已知12 g石墨完全转化为金刚石时,要吸收Q kJ的热量,下列说法正确的是( )
A.石墨不如金刚石稳定
B.金刚石与石墨的转化是物理变化
C.等物质的量的石墨与金刚石完全燃烧,金刚石放出的热量多
D.等物质的量的石墨与金刚石完全燃烧,石墨放出的热量多
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A.人类只有通过燃料燃烧才能获得能量
B.碳与O2、CO2的反应均属于放热反应
C.伴有能量变化的物质变化都是化学变化
D.物质发生化学反应的同时伴随着能量的变化,它通常表现为热量变化,这就是化学反应中的放热或吸热现象
难度: 简单查看答案及解析
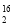 O和D
O和D