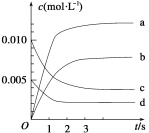
-
下列有关叙述正确的是
A.在中和滴定中,既可用标准溶液滴定待测溶液,也可用待测溶液滴定标准溶液
B.进行中和滴定操作时,眼睛要始终注视滴定管内溶液液面的变化
C.测定中和热时,两烧杯间填满碎纸的作用是固定小烧杯
D.若用50 mL 0.55 mol·L-1的氢氧化钠溶液,分别与50 mL 0.50 mol·L-1的盐酸和50 mL 0.50 mol·L−1硫酸充分反应,两反应的中和热不相等
难度: 中等查看答案及解析
-
已知:①:2C(s)+O2(g)═2CO(q)△H=﹣221.0kJ/mol②2H2(q)+O2(q)═2H2O(g)△H=﹣483.6kJ/mol,则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
A.262.6kJ/mol B.﹣131.3kJ/mol C.﹣352.3kJ/mol D.+131.3kJ/mol
难度: 中等查看答案及解析
-
在下列各说法中,正确的是
A.ΔH>0表示放热反应,ΔH<0表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热
难度: 中等查看答案及解析
-
下列各图所反映的措施中,目的是为了加快其化学反应速率的是
A.
 铁门表面喷漆 B.
铁门表面喷漆 B. 冰箱保存食物
冰箱保存食物C.
 扇子扇煤炉火 D.
扇子扇煤炉火 D.
难度: 简单查看答案及解析
-
已知反应A2(g)+2B2(g)
 2AB2(g)的ΔH<0,下列说法正确的是( )
2AB2(g)的ΔH<0,下列说法正确的是( )A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
难度: 中等查看答案及解析
-
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)
 2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( )①C生成的速率与C分解的速率相等;②单位时间内生成a mol A,同时生成3a mol B;③A、B、C的浓度不再变化;④A、B、C的压强不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦单位时间内消耗a mol A,同时生成3a mol B;⑧A、B、C的分子数之比为1∶3∶2
A.②⑧ B.①⑥ C.②④ D.③⑧
难度: 中等查看答案及解析
-
下列各组离子在指定条件下,一定能大量共存的是( )
A.能使蓝色石蕊试纸变红色的溶液中:K+、Na+、CO
 、NO
、NO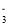
B.c(H+)=1×10-1 mol·L-1的溶液中:Cu2+、Al3+、SO
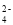 、NO
、NO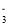
C.能使淀粉碘化钾试纸变蓝的溶液中:Na+、NH
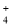 、S2-、Br-
、S2-、Br-D.水电离出的c(H+)=1×10-12 mol·L-1的溶液中:Na+、Mg2+、Cl-、SO
难度: 简单查看答案及解析
 O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1