-
非物质文化遗产是人类文明记忆的载体。下列云南非物质文化遗产技艺中主要涉及化学变化的是
A.西双版纳傣族织锦技艺
B.腾冲手工玉雕技艺
C.昆明滇派风筝制作技艺
D.会泽斑铜烧制技艺
难度: 简单查看答案及解析
-
下列属于纯净物的是
A.奶茶
B.官渡粑粑
C.冰水
D.鲜花酸奶
难度: 简单查看答案及解析
-
5月27日上午11时整,2020珠峰高程测量队8名攻顶队员在克服了峰顶空气稀薄、气候恶劣等重重困难后成功登顶。空气的成分中能供给呼吸的是
A.二氧化碳
B.氧气
C.氮气
D.稀有气体
难度: 简单查看答案及解析
-
随着人类对农产品需求量的增大,科学施用化肥逐渐成为农作物增产的最有力措施。下列属于氮肥的是
A.CO(NH2)2
B.K2SO4
C.Ca3(PO4)2
D.KCl
难度: 简单查看答案及解析
-
初中体育学业水平考试中用到的下列场地和器材的主要材料,不属于有机合成材料的是
A.塑胶跑道
B.钢制篮球架
C.塑料跳绳
D.PVC材质排球
难度: 中等查看答案及解析
-
具备基本的实验技能是进行科学探究的保证。下列实验操作正确的是
A.熄灭酒精灯
 B.测溶液的PH
B.测溶液的PH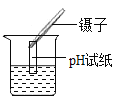
C.过滤泥水
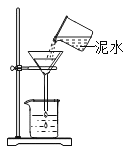 D.量取液体
D.量取液体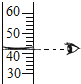
难度: 简单查看答案及解析
-
苏轼在《六幺令·天中节》中写到“粽叶香飘十里,对酒携樽俎”。能闻到粽叶香是因为
A.分子间有间隔
B.分子在不断运动
C.不同分子的化学性质不同
D.分子的体积很小
难度: 简单查看答案及解析
-
把少量下列物质分别放入水中,充分搅拌,能形成溶液的是
A.辣椒粉
B.菜籽油
C.蔗糖
D.面粉
难度: 简单查看答案及解析
-
云南风景秀丽,物产丰富。下列云南各地特产中富含蛋白质的是
A.潞西遮放米
B.蒙自酸石榴
C.寻甸黄牛肉
D.漾濞核桃油
难度: 简单查看答案及解析
-
氮化镁可用作合成人造金刚石的催化剂。氮化镁(Mg3N2)中氮元素的化合价为
A.-3
B.+2
C.+3
D.+5
难度: 简单查看答案及解析
-
某粒子结构示意图如图所示。下列说法不正确的是
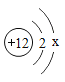
A.x为8
B.该粒子为阴离子
C.该粒子的质子数为12
D.该粒子的核外有两个电子层
难度: 简单查看答案及解析
-
铥广泛用于高强度电光源、激光、高温超导等领域。铥元素的相关信息如图所示,下列有关该元素说法不正确的是
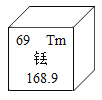
A.属于金属元素
B.原子序数是69
C.元素符号是Tm
D.相对原子质量是168.9g
难度: 简单查看答案及解析
-
碱性洗发水清洗油性头发效果更好。从pH角度考虑,油性发质最好选用的洗发水的pH为
A.8
B.7
C.6
D.4
难度: 简单查看答案及解析
-
下列实验现象描述正确的是
A.硫在空气中燃烧,发出蓝紫色火焰
B.向氯化铜溶液中滴加氢氧化钠溶液,有蓝色氢氧化铜沉淀生成
C.将打磨过的铝片放入稀硫酸中,有气泡产生
D.打开盛有浓盐酸的试剂瓶的瓶塞,瓶口冒白烟
难度: 简单查看答案及解析
-
昭通巧家县多年来大力发展花椒种植业,通过产业改造升级助推脱贫攻坚。花椒果实中含有卡枯醇(C10H10O4),具有降脂、镇咳作用。下列关于卡枯醇说法不正确的是
A.属于有机物
B.由碳、氢、氧三种元素组成
C.1个卡枯醇分子由24个原子构成
D.氧元素的质量分数最小
难度: 中等查看答案及解析
-
东晋化学家葛洪所著的《抱朴子》中有“丹砂烧之成水银”的记载,该反应的微观过程如图所示。下列有关该反应说法不正确的是
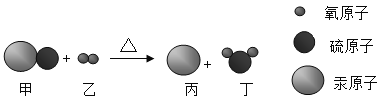
A.该反应属于置换反应
B.反应中乙、丁分子的个数比为1:1
C.丙物质由分子构成
D.反应前后原子的种类、个数不变
难度: 简单查看答案及解析
-
在一个密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下发生反应,测得反应前后各物质的质量如下表。下列说法不正确的是
物质
甲
乙
丙
丁
反应前的质量/g
40
90
10
3
反应后的质量/g
12
19
10
x
A.x=102
B.丁一定是化合物
C.丙可能为该反应的催化剂
D.参加反应的甲和乙的质量之比为4:9
难度: 简单查看答案及解析
-
甲、乙、丙、丁、戊为初中化学五种常见的不同类别的物质,其中甲的水溶液为蓝色,丙含有两种元素,丁是赤铁矿的主要成分。它们之间的相互转化关系如图所示,图中“一”表示相连的物质能相互反应,“→”表示一种物质能转化成另一种物质。下列说法不正确的是
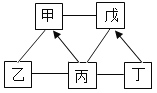
A.甲的水溶液中含有Cu2+
B.乙是Na2CO3
C.丙→甲的反应有H2O生成
D.丁→戊的化学方程式可为
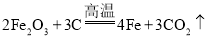
难度: 中等查看答案及解析
-
MnSO4、MgSO4两种物质的溶解度曲线如图所示。下列说法正确的是
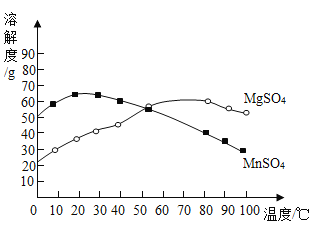
A.MnSO4的溶解度随温度的升高而减小
B.在0℃时将10 g MgSO4加入50g水中,充分搅拌后得到MgSO4的饱和溶液
C.将MgSO4的饱和溶液从60℃降温到0℃,得到的晶体比降温到30℃时多
D.将10℃时MnSO4饱和溶液升温至70℃,溶液中溶质的质量分数不变
难度: 中等查看答案及解析
-
下列说法合理的有
①电木插座破裂后能热修补
②不用其他试剂就能将NaCl、FeCl3、KOH、(NH4)2SO4、H2SO4五种溶液一一区分
③探究Zn、Fe、Ag的金属活动性,可将Fe和Ag分别放入ZnSO4溶液中
④Na2CO3溶液和Ba(OH)2溶液充分反应后,得到白色沉淀A和溶液B,向溶液B中加入少量稀盐酸,无明显现象。则溶液B中不含Na2CO3
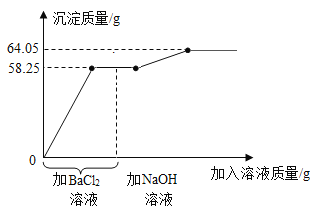
⑤有MgSO4和H2SO4的混合溶液100g,先向其中滴加BaC12溶液,再滴加NaOH溶液,产生沉淀质量与加入溶液质量关系如图所示。则原混合溶液中镁、硫元素的质量比为3:10
A.2个
B.3个
C.4个
D.5个
难度: 中等查看答案及解析
 )
)