-
向盐酸和氯化钙的混合溶液中逐滴滴加碳酸钠溶液,反应现象是( )
A.只看到有大量气泡冒出
B.只有白色沉淀析出
C.开始冒气泡,后出现白色沉淀
D.开始出现白色沉淀,后冒气泡难度: 中等查看答案及解析
-
下列物质中属于纯净物的是( )
A.天然气
B.乙醇汽油
C.液氧
D.生铁难度: 中等查看答案及解析
-
已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:

则下列说法正确的是( )
A.图示中共有4种分子
B.该反应属于化合反应
C.图示中的反应物都是单质
D.该图示不符合质量守恒定律难度: 中等查看答案及解析
-
下列实验数据合理的是:①用托盘天平称取15.6g氧化铜粉末 ②用广泛pH试纸测得溶液的pH为3.52 ③用100mL量筒量取5.26mL的稀硫酸 ④用普通温度计测得某液体的温度为25.62°C ⑤用10mL量筒量取某溶液6.6mL( )
A.①②
B.①⑤
C.④⑤
D.②③④难度: 中等查看答案及解析
-
下列各图所示装置的气密性检查中,漏气的是 ( )
A.、
B.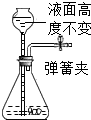
C.
D.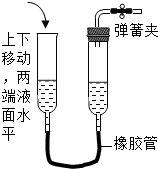
难度: 中等查看答案及解析
-
山茶油是一种绿色保健食品,其主要成分是柠檬醛.现从山茶油中提取7.6g柠檬醛,使其在氧气中完全燃烧,生成22g二氧化碳和7.2g水,则柠檬醛中( )
A.只含有碳、氢元素
B.一定含有碳、氢、氧元素
C.一定含有碳、氢元素,可能含有氧元素
D.含有的元素无法判断难度: 中等查看答案及解析
-
与Na+具有相同质子数和电子数的微粒是( )
A.F-
B.NH4+
C.OH-
D.H2O难度: 中等查看答案及解析
-
向AgNO3、Cu(NO3)2、Mg(NO3)2的混合物溶液中加入一些锌粉,完全反应后过滤.不可能存在的情况是( )
A.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+
B.滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Mg2+
C.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
D.滤纸上有Ag、Cu、Zn、Mg,滤液中有Zn2+难度: 中等查看答案及解析
-
我国近年研制成功一种气体,这种气体的每个分子是由质子数为8,相对原子质量为18的两个原子构成.下列各说法错误的是( )
A.这种气体的相对分子质量为36
B.这种原子的核外不一定有8个电子
C.这种气体中元素的化合价为0
D.这种原子与氢原子能构成相对分子质量为20的水分子难度: 中等查看答案及解析
-
在一定量的硫酸溶液中加入氯化钡溶液直到反应完全,产生沉淀的质量与原硫酸溶液的质量相等,则原硫酸溶液的质量分数为( )
A.42%
B.36%
C.30%
D.24%难度: 中等查看答案及解析