-
化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+1=2”的事实是( )
A.20℃,1L水与1L酒精混合后的体积等于2L
B.20℃,1g镁和1g稀硫酸充分反应后所得的溶液质量为2g
C.20℃,1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫
D.20℃,1g硝酸钾饱和溶液中加入1g硝酸钾固体能得到2g硝酸钾溶液难度: 中等查看答案及解析
-
人类的生活和生产都离不开金属.下面对金属的利用不是由金属活动性决定的是( )
A.用铁回收含银废液中的银
B.用锌与稀硫酸反应制取氢气
C.用金、银制首饰
D.用铝合金制作门窗框架难度: 中等查看答案及解析
-
醋酸、柠檬酸等是食品加工中常用的酸,它们在水中都能解离出( )
A.H+
B.OH-
C.Cl-
D.SO42-难度: 中等查看答案及解析
-
向含有AgNO3、Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体一定为( )
A.Ag、Cu两种单质的混合物
B.Cu、Fe两种单质的混合物
C.Ag、Fe两种单质的混合物
D.Ag、Cu、Fe三种单质的混合物难度: 中等查看答案及解析
-
通过对溶液知识的学习,判断下列有关说法中正确的是( )
A.将10%的硝酸钾溶液倒出一半,剩余溶液中溶质的质量分数仍为10%
B.热糖水降低温度后有固体析出,则原热糖水一定是饱和溶液
C.可以用冷却海水的方式得到氯化钠固体
D.配制溶液时,搅拌可以增大溶质的溶解度难度: 中等查看答案及解析
-
下列有关溶液的叙述中,正确的是( )
A.溶液一定是混合物
B.溶液中一定含有水
C.溶液都是无色透明的
D.凡是均一、稳定的液体一定是溶液难度: 中等查看答案及解析
-
下列生活中的现象,与物质溶解性无关的是( )
A.揭开啤酒瓶盖,有大量气泡溢出
B.盛石灰水的瓶口有一层白膜
C.烧开水时,沸腾前有大量气泡
D.咸菜长期放置在空气中,表面有一层“白霜”难度: 中等查看答案及解析
-
医院里常用溶质分数为5%的双氧水(H2O2)溶液清洗受伤病人的伤口,若要配制5%的双氧水溶液600g,需要30%的高浓度双氧水的质量为( )
A.30g
B.100g
C.200g
D.400g难度: 中等查看答案及解析
-
不能用金属和酸直接反应得到的物质是( )
A.FeCl3
B.FeC12
C.ZnC12
D.MgC12难度: 中等查看答案及解析
-
下列变化属于物理变化的是( )
A.稀盐酸洗铁锈
B.硫酸使紫色石蕊试液变红色
C.浓盐酸在空气中形成白雾
D.用浓硫酸在纸上写字难度: 中等查看答案及解析
-
向一接近饱和的KNO3溶液中,逐渐加入KNO3晶体,下列图象中符合溶液中溶质质量变化规律的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
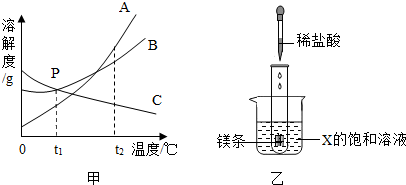
如图是A、B两种固体物质的溶解度曲线下列说法中错误的是( )

A.t1℃时A、B的溶解度相等
B.t2℃时,A的饱和溶液中溶质的质量分数为×100%
C.B的溶解度都随温度升高而增大
D.将t2℃时B的饱和溶液降温到t1℃时,溶液变稀了难度: 中等查看答案及解析
-
下列反应属于置换反应的是( )
A.3CO+Fe2O32Fe+3CO2
B.Zn+CuSO4=ZnSO4+Cu
C.CO2+2NaOH=Na2CO3+H2O
D.NaOH+HCl=NaCl+H2O难度: 中等查看答案及解析
-
如图所示的实验装置,向盛水的试管中慢慢注入3mL浓硫酸,此时可观察到U型管内液面(为了便于观察,液体为红墨水)的变化是( )

A.液面A高于液面B
B.液面B高于液面A
C.无变化
D.A、B液面同时升高难度: 中等查看答案及解析
-
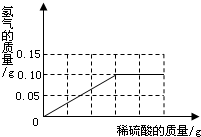
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价)( )
A.放出H2的质量是B>A>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A难度: 中等查看答案及解析