-
苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有
A.氧化性 B.还原性 C.碱性 D.酸性
难度: 简单查看答案及解析
-
氧化还原反应的实质是
A.氧元素的得与失 B.化合价的升降
C.电子的得失或偏移 D.分子中原子重新组合
难度: 简单查看答案及解析
-
下列关于纯净物、混合物、强电解质、弱电解质和非电解质的正确组合是
纯净物
混合物
强电解质
弱电解质
非电解质
A
盐酸
醋酸
碳酸
氨水
氧气
B
Na2CO3
碘酒
KOH
CH3COOH
干冰
C
酒精
石灰石
硫酸
磷酸
水
D
NaOH
天然气
NaCl
NaNO3
蔗糖
难度: 简单查看答案及解析
-
下列关于碱金属某些性质的排列中,正确的是
A.氧化性:Li+<Na+<K+<Rb+<Cs+ B.密度:Li<Na<K<Rb<Cs
C.熔点、沸点:Li<Na<K<Rb<Cs D.原子半径: Li<Na<K<Rb<Cs
难度: 简单查看答案及解析
-
下列各组离子,在滴加石蕊试液后会变蓝的溶液中能大量共存,且溶液为无色透明的离子组是
A.K+、MnO4-、Cl-、SO42- B.Na+、NO3-、HCO3-、Cl-
C.Na+、H+、NO3-、SO42- D.Na+、NO3-、SO42-、Cl-
难度: 简单查看答案及解析
-
.关于Na的描述正确的是 ①Na在自然界中既以游离态又以化合态形式存在;②金属Na着火可以用泡沫灭火器救火;③实验室中少量的Na保存在煤油里;④Na-K合金做原子反应堆的导热剂; ⑤Na比Cu活泼,因而Na可以从CuCl2溶液中置换出Cu ;⑥Na在空气中燃烧,主要产物是Na2O2 。
A.①③④⑤⑥ B.③④⑥ C.③④ D.全部
难度: 简单查看答案及解析
-
已知反应A+B=C+D 为放热反应,对该反应的下列说法中正确的是:
A.A的能量一定高于C
B.B的能量一定高于D
C.A和B的能量总和一定高于C和D的能量总和
D.因该反应为放热反应,故不必加热就可自发进行
难度: 简单查看答案及解析
-
5NH4NO3=2HNO3+4N2↑+9H2O中,发生氧化反应与发生还原反应的氮原子个数之比是
A.1∶3 B.5∶3 C.5∶8 D.5∶4
难度: 简单查看答案及解析
-
.盐酸能发生下列反应:①Zn+2HCl=ZnCl2+H2↑;②2HCl+CuO=CuCl2+H2O;
③MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O ,因此盐酸应当具有的性质是
A.只有酸性 B.只有氧化性
C.只有还原性 D.有酸性、氧化性和还原性
难度: 简单查看答案及解析
-
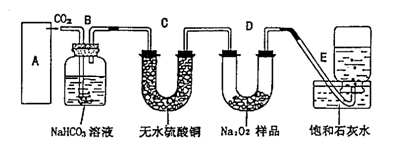
mg过氧化钠和碳酸钠的固体混合物跟干燥的二氧化碳充分作用后,固体质量变为ng,则原混合物中过氧化钠的质量分数是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
根据物质中S元素的化合价判断下列说法错误的是
A、浓H2SO4具有氧化性 B、H2S具有还原性
C、S只有氧化性 D、SO2既有氧化性又有还原性
难度: 简单查看答案及解析
-
下列反应既是离子反应,又是氧化还原反应的是
A.氯化钠溶液中滴入硝酸银溶液 B.氢气在氧气中燃烧
C.铁片置于硫酸铜溶液中 D.CO还原Fe2O3
难度: 简单查看答案及解析
-
已知:(1)H2S+I2=2H++2I—+S¯;(2)H2SO3+2H2S=3S¯+3H2O;(3)2I—+Br2=2Br—+I2;(4)H2SO3+I2+H2O=H2SO4+2HI 。则Br—、I—、H2S和H2SO3还原性由强到弱的顺序是
A.H2S>H2SO3>I—>Br— B.Br—>I—>H2SO3>H2S
C.H2SO3>H2S>Br—>I— D.I—>Br—>H2S>H2SO3
难度: 简单查看答案及解析
-
某溶液中含Fe3+、Cl—、Na+、SO42—,其离子个数比为Fe3+∶Cl—∶Na+∶SO42—=1∶2∶x∶2,则x的值是
A.1 B.2 C.3 D.4
难度: 简单查看答案及解析
-
下列图象不能正确反映对应的变化关系的是
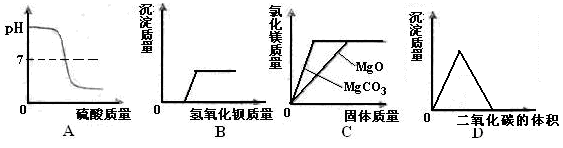
A.向一定量的氢氧化钠溶液中滴加稀硫酸至过量
B.向一定量的盐酸和氯化镁混合溶液中滴加氢氧化钡溶液
C.足量MgCO3和MgO固体分别加入到相同质量、相同质量分数的稀盐酸中
D.澄清石灰水中通入CO2至过量
难度: 简单查看答案及解析