-
能用来分离Fe3+和Al3+离子的试剂是
A.KSCN B. NaOH溶液 C.NH3.H2O D .H2S
难度: 简单查看答案及解析
-
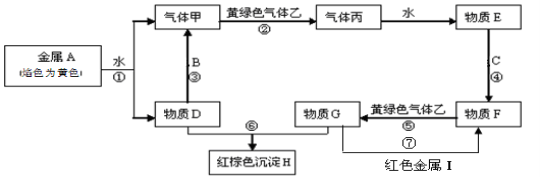
下列化合物中,不能通过单质之间的反应直接制取的是
A.Fe3O4 B.FeCl3 C.FeCl2 D CuCl2
难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.硫酸铁溶液与氢氧化钡溶液反应:Fe3++3OH-===Fe(OH)3↓
B.硫化钠溶液与氯化铁溶液反应:2Fe3++3S2-===Fe2S3
C.过量的铁与稀硝酸溶液:3Fe+8H++2NO3-===3Fe2++4H2O+2NO⇡
D.铁粉放入氯化铁溶液:Fe+Fe3+===Fe2+
难度: 中等查看答案及解析
-
下列关于氯水的叙述正确的是
A.新制氯水可使蓝色石蕊试纸先变红后褪色
B.新制氯水中只含Cl2和H2O分子
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后pH将变大
难度: 中等查看答案及解析
-
漂白粉的有效成分是( )
A.Ca(OH)2 B.Ca(ClO)2 C.CaCl2 D.CaCO3
难度: 简单查看答案及解析
-
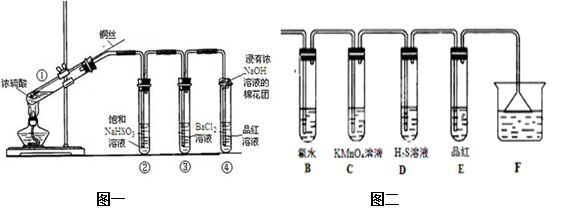
将等物质的量的SO2和Cl2混合后的气体溶解于适量的蒸馏水中,再滴入含有品红和BaCl2的混合溶液,则发生的实验现象是
①红色溶液很快褪色 ②红色溶液不褪色 ③有白色沉淀生成 ④没有白色沉淀生成[A.仅①和④ B.仅①和③ C.仅②和③ D.仅②和④
难度: 中等查看答案及解析
-
酸雨形成的最主要原因是
A.汽车排出的尾气
B.自然界中硫化物的分解
C.工业上大量燃烧含硫燃料
D.可燃冰燃烧
难度: 简单查看答案及解析
-
下列溶液可用于鉴别CO2与SO2气体的有
①品红溶液②氯化钙③酸性高锰酸钾④溴水⑤氢硫酸⑥澄清石灰水.A.①③④⑤ B.①③④⑥ C.①②③④⑥ D.①②③④⑤⑥
难度: 中等查看答案及解析
-
浓硫酸不具有的性质是
A.吸水性 B.腐蚀性 C.强氧化性 D.易挥发性
难度: 简单查看答案及解析
-
下列气体遇空气时,会发生颜色变化的是
A.N2 B.NH3 C.CO2 D.NO
难度: 简单查看答案及解析
-
下列关于NH3性质的说法正确的是( )
A.收集时采用向上排空气法
B.能使湿润的红色石蕊试纸变蓝
C.可用浓硫酸进行干燥
D.不能与氧气反应
难度: 中等查看答案及解析
-
下列有关自然界中氮循环(如右图)的说法不正确的是

A.含氮无机物和含氮有机物可相互转化
B.通过闪电产生NO属于高能固氮
C.硝酸盐被细菌分解为氮气过程,氮元素一定被氧化
D.C、H、O也参与自然界中氮循环
难度: 中等查看答案及解析
-
赏心悦目的雕花玻璃是用下列物质中的一种对玻璃刻蚀而成的。该物质是
A.浓硫酸 B.氢氟酸 C.浓硝酸 D.王水
难度: 简单查看答案及解析
-
下列物质不是硅酸盐材料的是
A.水泥 B.玻璃 C.石灰石 D.陶瓷
难度: 简单查看答案及解析
-
下列有关硅元素的叙述中,正确的是( )
A.SiO2不溶于水,也不溶于任何酸 B.SiO2是良好的半导体材料
C.硅是地壳中含量最多的元素 D.水玻璃可用作木材防火剂
难度: 简单查看答案及解析
-
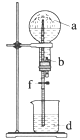
在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体d呈喷泉状喷出,最终几乎充满烧瓶。则a
和b分别是
a(干燥气体)
b(液体)
A
NO
水
B
CO2
饱和NaHCO3溶液
C
Cl2
饱和NaCl溶液
D
NH3
1 mol·L-1盐酸
难度: 中等查看答案及解析