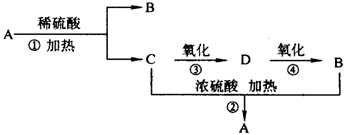
-
小苏打常用于治疗胃酸过多,小苏打属于
A.酸 B.碱 C.盐 D.氧化物
难度: 简单查看答案及解析
-
光导纤维的主要成分是
A.SiO2 B.Si C.SiC D.Na2SiO3
难度: 简单查看答案及解析
-
下列转化中不涉及化学变化的是
A.海水晒盐 B.煤的气化 C.石油裂解 D.皂化反应
难度: 中等查看答案及解析
-
下列物质不需密封保存的是
A.浓硝酸 B.氯化亚铁溶液 C.镁条 D.氯水
难度: 简单查看答案及解析
-
下列除去碳酸钠固体中少量碳酸氢钠的方法正确的是
A.加入盐酸 B.加入氢氧化钙 C.加入氯化钡 D.加热
难度: 中等查看答案及解析
-
下列元素中非金属性最强的是
A.氯 B.氧 C.氟 D.溴
难度: 简单查看答案及解析
-
当光束通过淀粉溶液时,从侧面观察到一条光亮的“通路”,说明淀粉溶液是
A.胶体 B.悬浊液 C.溶液 D.乳浊液
难度: 简单查看答案及解析
-
工业上粗硅的生产原理为2C+SiO2
Si+2CO↑,其中SiO2是
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
难度: 中等查看答案及解析
-
已知空气—锌电池的电极反应为:
锌片:Zn+2OH――2e-=ZnO+H2O;碳棒:
O2+H2O+2e- =2OH- ,据此判断锌片是
A.正极,被还原 B.正极,发生还原反应
C.负极,被还原 D.负极,发生氧化反应
难度: 中等查看答案及解析
-
在溶液中一定能大量共存的离子组是
A.K+、Ca2+、CO32- B.H+、NH4+、SO42-
C.H+、Cl-、HCO3- D.Fe3+、SO42-、SCN-
难度: 中等查看答案及解析
-
医学界通过用14C标记的C60发现一种羧酸衍生物,在特定条件下,它可以通过断裂DNA抑制艾滋病毒的繁殖。下列有关叙述中,正确的是
A.14C与12C的性质完全不同
B.14C与14N含有的中子数相同
C.14C60和12C60是碳元素的同素异形体
D.14C与12C、13C互为同位素
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,22.4 L H2O中含有的分子数为NA
B.28 g N2中含有的分子数为NA
C.1 mol Mg与足量稀盐酸反应转移的电子数为NA
D.1 L 1 mol·L-1 Na2 CO3溶液中含有的钠离子数为NA
难度: 中等查看答案及解析
-
下列有关化学反应与能量的说法正确的是
A.酸碱中和是放热反应
B.炭在氧气中燃烧属于吸热反应
C.化学键的形成需吸收能量
D.化学反应过程中,化学能一定转化成热能
难度: 中等查看答案及解析
-
下列关于O2+2SO2
2 SO3的叙述错误的是
A.增加O2的浓度能加快反应速率
B.若O2足量,则SO2可以完全转化为SO3
C.加入催化剂能加快反应速率
D.升高体系温度能加快反应速率
难度: 中等查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A.冷的氢氧化钠溶液中通入氯气:Cl2+OH-= ClO-+Cl-+H2O
B.碳酸氢钠溶液中滴入氢氧化钠溶液:HCO3-+OH–=CO32-+ H2O
C.在醋酸溶液中加入Na2CO3溶液:CO32-+2H+=CO2↑+H2O
D.三氯化铁溶液与氢氧化钡溶液反应:FeCl3+3OH-=Fe(OH)3↓+3Cl-
难度: 中等查看答案及解析
-
下列有关说法错误的是
A.陶瓷是一种应用广泛的普通硅酸盐材料
B.实验过程中产生的NO2尾气可以用NaOH溶液吸收
C.实验室可用浓硫酸干燥氨气
D.误服重金属盐造成的中毒可服用牛奶解毒
难度: 中等查看答案及解析
-
下列有关化学用语使用正确的是
A.CH4分子的球棍模型:
B.乙烯的结构简式:CH2CH2
C.S的结构示意图:

D.原子核内有l8个中子的氯原子:
难度: 中等查看答案及解析
-
下列说法正确的是
A.乙酸乙酯易溶于水 B.含碳、氢元素的化合物都是有机物
C.乙酸的酸性比碳酸强 D.甲烷和乙烯均可使溴水褪色
难度: 中等查看答案及解析
-
下列由相关实验现象所推出的结论正确的是
A.二氧化硫能漂白某些物质,说明它具有氧化性
B.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+
C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应
D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水
难度: 中等查看答案及解析
-
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子最外层电子数之和与Ca2+的核外电子数相等,Y、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
A.原子半径:Z>Y>X B.Z与X在同一周期
C.氢化物的稳定性:X>Y D.XZ4属于共价化合物
难度: 中等查看答案及解析
-
下列有机化学方程式书写正确的是
A.CH4+Cl2
CH2Cl2+H2
B.
+ HO—NO2
+ H2O
C.H2C=CH2+Br2
CH3CHBr2
D.CH3CH2OH+CH3COOH
CH3COOCH2CH3
难度: 中等查看答案及解析
-
下列实验装置或操作正确的是
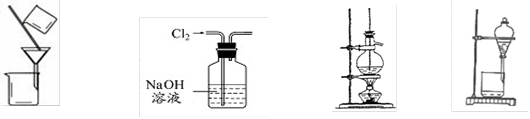
A.分离NaCl溶液中CaCO3 B.除去Cl2中含有的HCl C.石油分馏 D.分离乙醇和水
难度: 中等查看答案及解析
-
三草酸合铁酸钾晶体[K3Fe(C2O4)3•xH2O]是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组实验步骤为:(1)称量9.820 g三草酸合铁酸钾晶体,配制成250 mL溶液。(2)取所配溶液25.00 mL于锥形瓶中,滴加酸性KMnO4溶液至C2O42-全部转化成CO2,同时MnO4-被转化成Mn2+,恰好消耗0. 1000 mol/L KMnO4溶液24.00 mL。[K3Fe(C2O4)3的相对分子质量为437] 下列说法正确的是
A.步骤(2)中KMnO4表现还原性
B.配制三草酸合铁酸钾溶液玻璃仪器只需烧杯和玻璃棒
C.样品中结晶水的物质的量为0.03 mol
D.该晶体的化学式为K3Fe(C2O4)3•3H2O
难度: 中等查看答案及解析
-
性能各异的各种材料的广泛应用大大提高了人们的生活水平。回答问题:
⑴家庭中“钢精锅”是由铝合金做成的,在烧菜时能否放大量醋炖煮?________。(填能或否)
⑵下列关于铁制品保护措施的说法中不正确的有________(填序号)。
A.在自行车钢圈上镀上一层金属铬,摩擦部位加上机油或黄油
B.相同条件下,马口铁(表层镀锡)与白铁(表层镀锌)相比,马口铁更为耐用
C.在海轮的外壳上常焊有铜块,且定期更新
D.将不锈钢制成刀具和餐具,有的刀具还进行烤蓝处理
⑶生产普通玻璃和硅酸盐水泥所需用到的共同原料是________,导电塑料可表示为
,它属于________材料(填序号)
A.新型无机非金属材料 B.有机高分子材料 C.金属材料
难度: 中等查看答案及解析
-
人类健康与食品、药物等关系密切:
⑴有些学生从小偏食,不爱吃水果、蔬菜造成营养缺乏、发育不良,这主要是由于摄取的________(选填脂肪、维生素或蛋白质)不足引起的。
⑵生活中应合理地摄取人体必需的元素,体内 ________元素不足会引起甲状腺肿疾病。
⑶糖类、油脂和蛋白质都是人体所必需的营养物质,其中可以在体内消化后为人体提供高级脂肪酸的是________。
⑷邻羟基苯甲酸的结构简式为
,俗名为水杨酸,在医学上具有________作用
难度: 简单查看答案及解析
-
保持洁净安全的生存环境已成为全人类的共识。
⑴某地河流中含有大量的重金属离子,我们常采用________法除去。
⑵天然水中含有的细小悬浮颗粒可以用明矾做________剂进行净化处理,明矾水解得到的________可以吸附细小悬浮颗粒。
⑶为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量。为控制大气中二氧化硫的排放,常采取的措施是在煤炭中加入石灰石粉末对化石燃料进行________处理,其原理用方程式可表示为________。
难度: 中等查看答案及解析
-
聚苯乙烯是一种发泡塑料,可用于包装材料等。聚苯乙烯的结构简式为:
,试回答下列问题:
(1)聚苯乙烯的单体是(写结构简式):________。该单体可发生的化学反应类型有________。(写两种)
(2)试推测聚苯乙烯是________型分子(填“线型”或“体型”),它能否溶解于CHCl3,________。(填“能”或“否”),它具有________性(填“热塑”或“热固”)。
难度: 简单查看答案及解析
-
下图各物质是中学化学中常见的物质,甲和A的焰色反应为黄色,常温常压下B为无色无味气体,丁可使带火星的木条复燃。请回答下列问题:
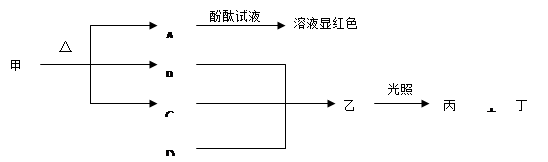
⑴写出B的电子式________。
⑵工业上生产D采用石灰乳与某种气体反应。D常用作________剂
⑶写出由A变甲的化学方程式。
⑷B与甲烷在一定条件下生成氢气和CO的化学方程式________。
难度: 困难查看答案及解析