-
下列物质属于纯净物的是 ( )
A.液氯 B.漂白粉 C.氯水 D.食盐水
难度: 简单查看答案及解析
-
据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列说法正确的是 ( )
A.42He原子核内含有4个质子 B.32He原子核内含有2个中子
C.32He和42He互为同位素 D. 42He的性质很活泼
难度: 简单查看答案及解析
-
下列叙述正确的是 ( )
A、1molNaOH的摩尔质量为40g B、64gSO2中含有1molO2
C、1molN2的体积约为22.4L D、0.5molCO2约含有3.01×1023个CO2分子
难度: 简单查看答案及解析
-
实验室有两瓶溶液,都已经失去标签,已知其中一瓶是硫酸溶液,另一瓶是蔗糖溶液。同学们设计了下列方案对溶液进行鉴别:
①用pH试纸分别测定两溶液的pH,pH﹤7的是硫酸溶液,另一瓶是蔗糖溶液。
②取样,分别向两溶液中滴加盐酸酸化的氯化钡溶液,生成白色沉淀的是硫酸溶液,不产生沉淀的是蔗糖溶液。
③取样,分别向两溶液中加入一小块铜片,产生气体的是硫酸溶液,不产生气体的是蔗糖溶液。
④取样,分别进行导电性实验,能导电的是硫酸溶液,不能导电的是蔗糖溶液。
⑤分别取极少量溶液尝一尝,有甜味的是蔗糖溶液,有酸味的是硫酸溶液。
则上述实验方案及结论正确的是 ( )
A.①②③④⑤ B.①④⑤ C.①②④⑤ D.①②④
难度: 简单查看答案及解析
-
设NA代表阿伏加德罗常数,下列说法正确的是 ( )
A、23g金属钠变为钠离子时失去的电子数为NA
B、12 g C-13含有的原子数为NA个
C、标准状况下,22.4 L氦气所含的原子数目为2NA
D、常温常压下,28g N2和CO的混合气体所含原子数为NA
难度: 简单查看答案及解析
-
下列能达到实验目的的是 ( )
A.用NaOH溶液除去CO2中混有的HCl气体
B.用分液漏斗分离四氯化碳和水的混合物;
C. 加入盐酸以除去硫酸钠中的少许碳酸钠杂质
D.配制一定浓度的氯化钾溶液1000mL,准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容
难度: 简单查看答案及解析
-
对于某些离子的检验及结论一定正确的是 ( )
A.加入盐酸酸化无现象,再加氯化钡溶液有白色沉淀产生,一定有SO42-
B.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32—
C.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
D.加入稀氢氧化钠溶液,用湿润红色石蕊试纸检验产生的气体没有变蓝,一定没有NH4+
难度: 简单查看答案及解析
-
在同温同压下,A容器中的氧气(O2)和B容器中的氨气(NH3)所含的原子个数相同,则A、B两容器中气体的体积之比是 ( )
A. 1:2 B.2:3 C. 2:1 D.3:2
难度: 简单查看答案及解析
-
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应并不改变的是( )
A.Na和O2 B.NaOH和CO2 C.H2和Cl2 D.木炭和O2
难度: 简单查看答案及解析
-
下面有关Na2CO3与NaHCO3的性质比较中错误的是( )
A.相同浓度溶液的碱性Na2CO3>NaHCO3
B.常温下在水中的溶解度Na2CO3>NaHCO3
C.等质量的固体与足量盐酸反应放出CO2的质量Na2CO3>NaHCO3
D.热稳定性:NaHCO3<Na2CO3
难度: 简单查看答案及解析
-
下列有关氯水的叙述,正确的是( )
A.新制氯水只含有氯分子和次氯酸分子;
B.新制氯水可使紫色石蕊试液先变红后褪色;
C.氯水光照时有气泡逸出,该气体的主要成分是氯气;
D.氯水放置数天后,其酸性逐渐减弱。
难度: 简单查看答案及解析
-
海藻中含有丰富的、以离子形式存在的碘元素.下图是实验室从海藻里提取碘的流程的一部分。
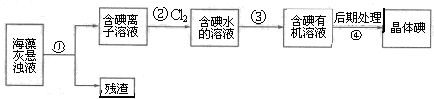
下列判断正确的是( )
A.步骤①、③的操作分别是过滤、萃取分液
B.可用淀粉溶液检验步骤②的反应是否进行完全
C.步骤③中加入的有机溶剂是乙醇
D.步骤④的操作是过滤
难度: 简单查看答案及解析
-
下列各组溶液中离子,能在溶液中大量共存的是( )
A.H+、Ca2+、NO3-、CO32- B.K+、Na+、Br-、NO3-
C.Ag+、Na+、Cl-、K+ D.NH4+、Cl—、OH¯、SO42—
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A.钠和冷水反应:Na+2H2O=Na++2OH-+H2↑
B.氯气通入溴化钾溶液:Cl2+2Br-=Br2+2Cl-
C.铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
D.稀硫酸和氢氧化铜反应:H++OH-=H2O
难度: 简单查看答案及解析
-
对于反应3Cl2+6NaOH ==5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的Cl原子和被还原的Cl原子的物质的量的比为5∶1
C.Cl2既是氧化剂又是还原剂
D.每生成1mol的NaClO3转移6mol的电子
难度: 简单查看答案及解析
