-
下列是同周期元素基态原子的最外层电子排布式,所表示的原子最容易得到电子的是
A.ns2 B.ns2np1 C.ns2np4 D.ns2np5
难度: 中等查看答案及解析
-
(2013·江苏无锡高三月考)下列每组物质中化学键类型和分子的极性都相同的是
A.CO2和CS2 B.NaCl和HCl C.H2O和CH4 D.O2和HBr
难度: 中等查看答案及解析
-
对Na、Mg、Al的有关性质的叙述正确的是
A.碱性:NaOH<Mg(OH)2<Al(OH)3 B.第一电离能:Na<Mg<Al
C.电负性:Na>Mg>Al D.还原性:Na>Mg>Al
难度: 中等查看答案及解析
-
(2013·长沙模拟)短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如下图所示。下列说法正确的是
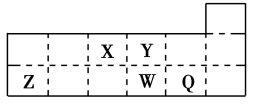
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ。
C.Y2-和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
难度: 中等查看答案及解析
-
(2013·江苏连云港高三模拟)有下列物质:①白磷;②金刚石;③石墨;④二氧化硅;⑤甲烷;⑥四氯化碳;⑦单质硅;⑧铵根离子,其分子结构或晶体结构单元中存在正四面体的是
A.除③外 B.①②⑤⑥ C.除③⑧外 D.③④⑦⑧
难度: 中等查看答案及解析
-
以下各分子(或离子)中,所有原子都满足最外层为8电子结构的是
A.H3O+ B.BF3 C.CCl4 D.PCl5
难度: 中等查看答案及解析
-
在有机物中,若碳原子上连接的四个原子或原子团不相同,则这个碳原子称为手性碳原子。含有手性碳原子的分子一般是手性分子具有镜像异构及光学活性,下列分子中具有光学活性的是
A.CBr2F2 B.CH3CH2OH
C.CH3CH2CH3 D.CH3CH(OH)COOH
难度: 中等查看答案及解析
-
下列中心原子的杂化轨道类型和分子几何构型不正确的是
A.PCl3中P原子sp3杂化,为三角锥形
B.BCl3中B原子sp2杂化,为平面三角形
C.CS2中C原子sp杂化,为直线形
D.H2S分子中,S为sp杂化,为直线形
难度: 中等查看答案及解析
-
有关CH2=CH-C≡N分子的说法正确的是
A.3个
键,3个π键 B.4个
键,3个2π键
C.6个
键,2个π键 D.6个
键,3个π键
难度: 中等查看答案及解析
-
(2014·合肥八中月考)基态碳原子的最外能层的各能级中,电子排布的方式正确的是

难度: 中等查看答案及解析
-
下列有机物命名正确的是
A. 2,2,3-三甲基丁烷 B. 2-乙基戊烷
C. 2-甲基-1-丁炔 D. 2,2-甲基-1-丁烯
难度: 中等查看答案及解析
-
下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3∶1的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
由2—氯丙烷制得少量的CH2OHCHOHCH3 需要经过下列几步反应
A.消去→加成→水解 B.加成→消去→取代
C.取代→消去→加成 D.消去→加成→消去
难度: 中等查看答案及解析
-
普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型)。下列关于普伐他汀的描述正确的是
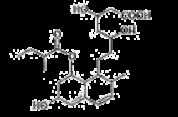
A.分子中含有3种官能团
B.可发生加成反应、氧化反应
C.在水溶液中羧基和羟基均能电离出H+
D.1 mol该物质最多可与l molNaOH反应
难度: 困难查看答案及解析
-
下列醇既能被催化氧化生成醛,又能发生消去反应生成烯烃的是
A.CH3OH B.
C.
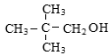 D.
D.难度: 中等查看答案及解析
-
在乙醇CH3CH2OH中化学键如图,则下列说法中正确的是

A.当该醇发生催化氧化时,被破坏的键是②③
B.当该醇与Na反应时,被破坏的键是①
C.当该醇与羧酸发生酯化反应时,被破坏的键是②
D.当该醇发生消去反应时,被破坏的键是①和④
难度: 中等查看答案及解析
-
下列属于同分异构体的是
A.CH4和CH3CH3
B.CH3-CH2-Cl和CH2Cl-CH2Cl
C.CH2=CHCH2CH3和CH3CH=CHCH3
D.
难度: 中等查看答案及解析
-
可以用来鉴别乙烷和乙烯的方法是
A.用足量的NaOH溶液 B.用溴的CCl4溶液
C.在光照条件下与Cl2反应 D.在Ni催化、加热条件下通入H2
难度: 中等查看答案及解析
-
下列5种烃:①2-甲基戊烷 ②2,2-二甲基丙烷 ③己烷 ④庚烷 ⑤戊烷,按它们的沸点由高到低的顺序排列正确的是
A.①>②>③>④>⑤ B.②>③>⑤>④>①
C.④>③>②>①>⑤ D.④>③>①>⑤>②
难度: 中等查看答案及解析
-
某有机物的结构式如图所示:
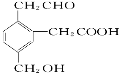 ,它在一定条件下可能发生的反应有①加成反应②水解反应③酯化反应④氧化反应⑤中和反应⑥消去反应
,它在一定条件下可能发生的反应有①加成反应②水解反应③酯化反应④氧化反应⑤中和反应⑥消去反应A.②③④ B.①③⑤⑥ C.①③④⑤ D.②③④⑤⑥
难度: 中等查看答案及解析
-
某有机物的结构简式如下,关于该有机物的下列叙述不正确的是
A.不能使酸性KMnO4溶液褪色
B.能使溴水褪色
C.在加热和催化剂作用下,最多能和4 mol H2反应
D.一定条件下,能发生取代反应
难度: 中等查看答案及解析
-
下列叙述错误的是
A.用新制的银氨溶液可区分甲酸甲酯和乙醛
B.用高锰酸钾酸性溶液可区分己烷和3-己烯
C.用水可区分苯和溴苯
D.用金属钠可区分乙醇和乙醚
难度: 中等查看答案及解析
-
四联苯
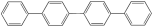 的一氯代物有
的一氯代物有A.3种 B.4种 C.5种 D.6种
难度: 中等查看答案及解析
-
高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如右图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是
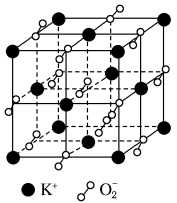
A.超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2-
B.晶体中每个K+周围有8个O2-,每个O周围有8个K+
C.晶体中与每个K+距离最近的K+有8个
D.晶体中,0价氧与-2价氧的数目比为2:1
难度: 中等查看答案及解析
-
实验测得 BeCl2为共价化合物,两个Be—Cl键间的夹角为180°。由此可见,BeCl2属于
A.由极性键构成的极性分子 B.由极性键构成的非极性分子
C.由非极性键构成的极性分子 D.由非极性键构成的非极性分子
难度: 中等查看答案及解析