-
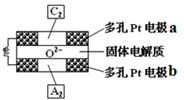
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是( )
A.正极反应式:Ag+Cl--e-=AgCl
B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Na+不断向“水”电池的负极移动
D.AgCl是还原产物
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 40K和40 Ca原子中的质子数和中子数都相等
B. 某元素最外层只有一个电子,则它一定是金属元素
C. 任何原子或离子的组成中都含有质子
D. 同位素的不同核素物理、化学性质完全相同
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.虽然油脂的相对分子质量都较大,但油脂不属于高分子化合物
B.淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体
C.酯化反应属于取代反应
D.乙烯使酸性高锰酸钾溶液褪色与乙烯使溴水褪色的原理不同
难度: 中等查看答案及解析
-
下列有关环境问题的说法正确的是( )
A.臭氧的体积分数超过10-4 %的空气有利于人体健康
B.pH在5.6~7.0之间的雨水通常称为酸雨
C.燃煤时加入适量石灰石,可减少废气中SO2的量
D.含磷合成洗涤剂易于被细菌分解,故不会导致水体污染
难度: 简单查看答案及解析
-
下列有关化学用语表示正确的是( )
A.H2O2的电子式:
B. F的结构示意图:
C.中子数为20氯原子: 2017Cl
D.次氯酸的结构式:H—O—Cl
难度: 中等查看答案及解析
-
不能说明氧的非金属性比硫强的事实是( )
A.H2O的热稳定性强于H2S
B.硫化氢水溶液露置于空气中变浑浊
C.H2O是液体,H2S常温下是气体
D.氧气和氢气化合比硫和氢气化合容易
难度: 中等查看答案及解析
-
海带中含碘元素,从海带中提取碘有如下步骤:①加入足量双氧水(含稀硫酸);②将
海带焙烧成灰后加水搅拌;③加CCl4振荡;④用分液漏斗分液; ⑤过滤。合理的操作顺序是( )
A. ①②③④⑤ B. ①③⑤②④ C. ②⑤①③④ D. ②①③⑤④
难度: 简单查看答案及解析
-
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W
X
Y
Z
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性
难度: 简单查看答案及解析
-
Na3N是离子化合物
,它和水作用可产生NH3。下列叙述正确的是( )
A.Na3N与盐酸反应生成的都是盐
B.Na+和N3-的电子层结构不相同
C.Na+的半径大于N3-的半径
D.在Na3N与水的反应中,Na3N做还原剂
难度: 简单查看答案及解析
-
W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。W、Z最外层电子数相同,Z的核电荷数是W的2倍。工业上一般通过电解氧化物的方法获得Y的单质,则下列说法不正确的是 ( )
A. W、X、Y形成的简单离子核外电子数相同
B. Z和W可形成原子个数比为1:2和1:3的共价化合物
C. Y和Z形成的化合物可以通过复分解反应制得
D. X、Y和Z三种元素形成的最高价氧化物对应的水化物能两两反应
难度: 简单查看答案及解析
-
通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
化学键
Si-O
Si-Cl
H-H
H-Cl
Si-Si
Si-C
E(kJ·mol−1)
460
360
436
431
176
347
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi-Si键),该反应的产生的热量为( )
A.吸收412 kJ·mol-1 B.放出412 kJ·mol-1
C.吸收236 kJ·mol-1 D.放出236 kJ·mol-1
难度: 中等查看答案及解析
-
把下列四种X溶液分别加入四个盛有10mL2mol/L盐酸的烧杯中,均加水稀释到50mL,此时X和盐酸缓缓地进行反应.其中反应速率最大的是( )
A.10℃,20mL3mol/L的X溶液 B.50℃20mL3mol/L的X溶液
C.50℃ 10mL4mol/L的X溶液 D.10℃10mL2mol/L的X溶液
难度: 简单查看答案及解析
-
在密闭容器中进行如下反应:X2(g)+Y2(g)
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时各物质的浓度有可能是( )
A.X2为0.2 mol·L-1
B.Y2为0.45 mol·L-1
C.Z为0.35 mol·L-1
D.Z为0.4 mol·L-1
难度: 中等查看答案及解析
-
某有机物2.3克,完全燃烧后的产物依次通过浓硫酸与NaOH溶液,分别增重2.7克与4.4克,该有机物可能是 ( )
A、CH4 B、C2H4 C、C2H6 D、C2H6O
难度: 简单查看答案及解析
-
现有三种有机物甲、乙、丙,其结构如图所示:
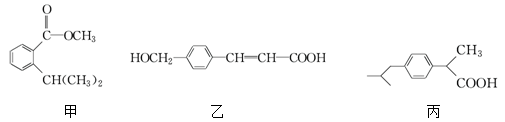
下列有关说法中正确的是( )
A.均能与碳酸氢钠反应
B.只用碳酸钠溶液和银氨溶液能检验甲、乙、丙
C.与足量氢气反应,相同物质的量的甲、乙、丙消耗氢气的物质的量之比为3∶4∶3
D.甲的化学式为C11H13O2,乙含有两种含氧官能团
难度: 中等查看答案及解析
-
对于苯乙烯(
)的下列叙述:①能使KMnO4酸性溶液褪色 ②可发生加聚反
应 ③可溶于水 ④可溶于苯中 ⑤能与浓硝酸发生取代反应 ⑥所有的原子可能共平面,其中正确的是
A.①②④⑤ B.①②
⑤⑥ C.①②④⑤⑥ D.全部
难度: 简单查看答案及解析
-
下列各组指定物质的同分异构体数目相等的是( )
A.苯
的二氯代物和苯的一硝基代物
B.C3H6Br2和C5H11Br
C.乙烷的二氯代物和丙烷的一氯代物
D.丙烷的一氯代物和戊烷
难度: 中等查看答案及解析
-
1molX气体跟amolY气体在体积可变的密闭容器中发生如下反应X(g)+aY(g)
bZ(g), 反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是( )
A.a=1,b=1 B.a=2,b=1 C.a=2,b=2 D.a=3,b=3
难度: 简单查看答案及解析