-
下列实验或操作不能达到目的的是( )
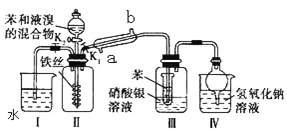
A. 制取溴苯:将铁屑、溴水、苯混合加热
B. 用 NaOH 溶液除去溴苯中的溴
C. 鉴别己烯和苯:向己烯和苯中分别滴入酸性 KMnO4 溶液,振荡,观察是否褪色
D. 除去甲烷中含有的乙烯:将混合气体通入溴水中
难度: 简单查看答案及解析
-
甲烷是最简单的烃,下列关于甲烷的叙述中不正确的是( )
A. 甲烷是烃类物质中相对分子质量最小的物质
B. 甲烷与空气的体积比为 1∶2 时,混合气点燃爆炸最剧烈
C. 1 mol CH4 在光照条件下最多能与 4 mol Cl2 反应
D. 甲烷的二氯代物只有一种可以证明甲烷为正四面体结构
难度: 简单查看答案及解析
-
下列反应中前者属于取代反应,后者属于加成反应的是( )
A. 甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液的褪色
B. 乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷
C. 苯滴入浓硝酸和浓硫酸的混合液中,有油状液体生成;乙烯与水生成乙醇的反应
D. 在苯中滴入溴水,使溴水褪色;乙烯与氯化氢反应制取氯乙烷
难度: 简单查看答案及解析
-
下列关于常见有机化合物的说法中,正确的是( )
A. 氯乙烯、聚乙烯、苯乙烯都是不饱和烃
B. 乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应
C. 苯、乙烯都既能发生加成反应,也能发生氧化反应
D. 通过石油裂化和裂解可得到乙烯、丙烯和苯等重要的化工原料
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 某有机物燃烧只生成 CO2 和 H2O,且二者物质的量相等,则此有机物一定为 CnH2n
B. 相同质量的烃,完全燃烧,消耗 O2 越多,烃中含氢量越高
C. 某气态烃 CxHy 与足量 O2 恰好完全反应,如果反应前后气体体积不变(温度>100 ℃), 则 y=2
D. 一种烃在足量的氧气中燃烧,将产生的气体通过浓 H2SO4,与反应前相比减少的体积 就是生成的水蒸气的体积
难度: 中等查看答案及解析
-
下列有关苯及其同系物的说法错误的是( )
A. 苯在空气中燃烧,火焰明亮伴有浓烟
B. 用酸性高锰酸钾溶液验证苯环上是否存在碳碳双键
C. 苯能与氢气在一定条件下发生加成反应
D. 甲苯能使酸性高锰酸钾溶液褪色,说明甲基使苯环变活泼
难度: 中等查看答案及解析
-
2005年度的诺贝尔化学奖分别奖给美国和法国的三位科学家,表彰他们对“烯烃复分 解”反应研究方面作出的贡献。“烯烃复分解”是指在金属钨或钼等催化剂的作用下,碳碳双键断裂并重新组合的过程。例如:
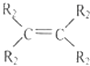 +
+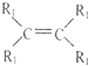 →
→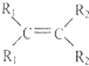 +
+ 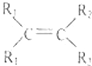
则对于有机物CH2=CHCH2CH=CH2发生烯烃复分解反应时可能生成产物的判断中正确的 是( )
①②CH2=CH2③
 ④CH2=C=CH2
④CH2=C=CH2A. 只有③ B. 只有②③ C. 只有①②③ D. 只有④
难度: 中等查看答案及解析
-
下列有关镀锌钢管的叙述正确的是( )
A. 电镀时,钢管做阳极,锌棒做阴极,锌盐溶液做电解质溶液
B. 钢管镀锌后,镀锌层破损后,钢管不能受到保护
C. 镀锌的目的是为了在钢管表面形成 Fe-Zn 合金,增强钢管的耐腐蚀能力
D. 镀锌层破损后,钢管仍可受到保护
难度: 中等查看答案及解析
-
电解装置如图所示,电解槽内装有 KI 及淀粉溶液,中间用阴离子交换膜 隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变 浅。已知:3I2+6OH﹣=IO3﹣+5I﹣+3H2O,下列说法不正确的是( )
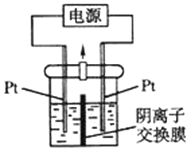
A. 右侧发生的电极反应式:2H2O+2e﹣=H2↑+2OH﹣
B. 电解结束后,右侧溶液中含有 IO3﹣
C. 电解槽内发生反应的总化学方程式:KI+3H2O
KIO3+3H2↑
D. 如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变
难度: 困难查看答案及解析
-
下列说法正确的是( )
A. 丙烷是直链烃,所以分子中3个碳原子也在一条直线上
B. 丙烯所有原子均在同一平面上
C.
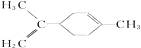 所有碳原子一定在同一平面上
所有碳原子一定在同一平面上D.
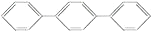 至少有16个原子共平面
至少有16个原子共平面难度: 中等查看答案及解析
-
有4种碳骨架如下的烃,下列说法正确的是( )
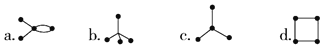
①a和d是同分异构体 ②b和c是同系物
③a和d都能发生加聚反应 ④只有b和c能发生取代反应
A. ①② B. ①④ C. ②③ D. ①②③
难度: 中等查看答案及解析
-
聚丙烯酸钠(
)具有超强吸水性,能吸收空气中的水分,可用于矿 山道路运输抑尘等。下列叙述不正确的是( )
A. 聚丙烯酸钠属于纯净物 B. 聚丙烯酸钠可用于生产尿不湿
C. 聚丙烯酸钠的单体为CH2=CH—COONa D. 路面喷洒聚丙烯酸钠溶液能抑制扬尘,一定程度上能预防雾霾和 PM2.5
难度: 中等查看答案及解析
-
下列有关冶炼金属的说法正确的是( )
A. 工业上冶炼钠,是通过电解氯化钠饱和溶液
B. 工业上冶炼铝,如果以石墨为电极,则阳极石墨需要不断补充
C. 工业上冶炼镁,是电解熔融氧化镁
D. 工业上精炼铜是粗铜为阴极
难度: 中等查看答案及解析
-
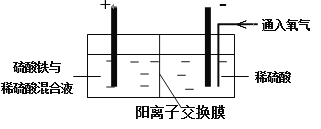
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
),其原理如图所示,下列说法正确的是( )
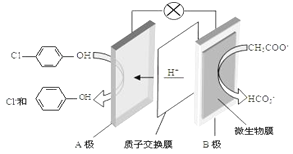
A. 当外电路中有0.2mole―转移时,A极区增加的H+个数为0.2NA
B. A极的电极反应式为
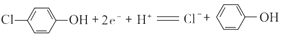
C. 该装置为电解池,电流方向从A极沿导线经小灯泡流向B极
D. B 极接电池的正极,发生还原反应
难度: 中等查看答案及解析
-
下列鉴别方法不可行的是( )
A. 用水鉴别乙醇、甲苯和溴苯
B. 用燃烧法鉴别乙醇、苯和四氯化碳
C. 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
D. 用酸性高锰酸钾溶液鉴别苯、环己烯和环己烷
难度: 中等查看答案及解析
-
下列有关电化学装置的说法正确的是

A. 利用图a装置处理银器表面的黑斑Ag2S,银器表面的反应为Ag2S+2e-=2Ag+S2-
B. 图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出
C. 图c中的X极若为负极,则该装置可实现粗铜的精炼
D. 图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
难度: 中等查看答案及解析
-
如图装置中发生反应的离子方程式为:Zn+2H+→Zn2++H2↑,下列说法错误的是( )
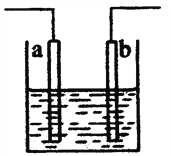
A. 该装置可能是原电池,电解质溶液为稀盐酸
B. 该装置可能是电解池,电解质溶液为稀盐酸
C. a、b 不可能是同种材料的电极
D. 该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
难度: 中等查看答案及解析
-
香叶醇是合成玫瑰香油的主要原料,其结构简式如下:下列有关香叶醇的叙述正确的 是( )
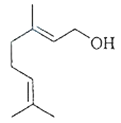
A. 能发生加成反应不能发生取代反应 B. 不能使溴的四氯化碳溶液褪色
C. 不能使酸性高锰酸钾溶液褪色 D. 香叶醇的分子式为 C10H18O
难度: 中等查看答案及解析
-
甲苯的苯环上有5个氢原子,其中若有两个氢原子分别被羟基(—OH)和氯原子(—Cl)取代,则可形成的有机物同分异构体有( )
A. 9种 B. 10种
C. 12种 D. 15种
难度: 困难查看答案及解析
-
下列说法正确的是( )
A. 烷烃的通式为 CnH2n+2,随 n 值增大,碳元素的质量百分含量逐渐减小
B. 乙炔与苯的实验式为 CH,是含碳量最高的物质
C. 1 摩尔苯恰好与 3 摩尔氢气完全加成,说明一个苯分子中有三个碳碳双键
D. n=7,主链上有 5 个碳原子的烷烃共有五种
难度: 中等查看答案及解析
-
分子式为 C8H8 的两种同分异构体 X 和 Y。X 是一种芳香烃,分子中只有一个环;Y 俗称立方烷,其核磁共振氢谱显示只有一个吸收峰。下列有关说法错误的是( )
A. X、Y 均能燃烧,都有大量浓烟产生
B. X 既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,还能发生加聚反应
C.
与 X 互为同系物
D. Y 的二氯代物有三种
难度: 中等查看答案及解析
-
对复杂的有机物的结构,可用键线式简化表示,如有机物CH2=CHCHO写成
。则与键线式为 如图的物质互为同分异构体的是( )

A. A B. B C. C D. D
难度: 中等查看答案及解析
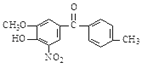 ,该有机物中含氧官能团有:______、______、________、______(写官能团名称)。
,该有机物中含氧官能团有:______、______、________、______(写官能团名称)。 的系统名称是_____,将其在催化剂存在 下完全氢化,所得烷烃的系统名称是_____。
的系统名称是_____,将其在催化剂存在 下完全氢化,所得烷烃的系统名称是_____。 (R、R′表示烷基或氢原子)
(R、R′表示烷基或氢原子)

 +H2O;
+H2O;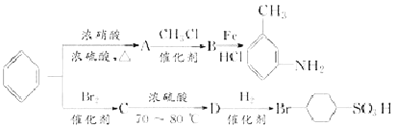
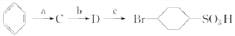 ”的所有反应中属于取代反应的是_________(填字母),属于加成反应的是________(填字母);用1H核磁共振谱可以证明化合 物D中有__________种处于不同化学环境的氢。
”的所有反应中属于取代反应的是_________(填字母),属于加成反应的是________(填字母);用1H核磁共振谱可以证明化合 物D中有__________种处于不同化学环境的氢。