-
用特殊方法把固体物质加工到纳米级(1nm-100nm)的超细粉末粒子,然后制得纳米材料.下列分散系中的分散质的粒子的大小和这种纳米粒子大小具有相同的数量级的是( )
A.溶液
B.悬浊液
C.胶体
D.乳浊液难度: 中等查看答案及解析
-
在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记的是( )
A.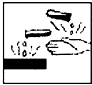
B.
C.
D.难度: 中等查看答案及解析
-
下列仪器在使用之前需要检查是否漏液的是( )
①分液漏斗 ②长颈漏斗 ③容量瓶 ④蒸馏烧瓶 ⑤洗气瓶.
A.①②③
B.①③
C.①③⑤
D.①②③④难度: 中等查看答案及解析
-
下列溶液中,溶质的物质的量浓度为1mol/L的是( )
A.含Na+为2mol的Na2SO4溶液
B.将80gSO3溶于水并配成1L的溶液
C.将0.5mol/L的某饱和溶液100mL,加热蒸发掉50g水后的溶液
D.将58.5gNaCl溶于1L水所得的溶液难度: 中等查看答案及解析
-
下列变化需要加入氧化剂才能实现的是( )
A.Na2CO3→CO2
B.HCl→Cl2
C.H2SO4(浓)→SO2
D.CuO→Cu难度: 中等查看答案及解析
-
下列图示实验操作中,正确的是( )
A.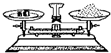
称取氢氧化钠
B.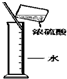
浓硫酸稀释
C.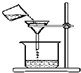
过滤溶液
D.
点燃酒精灯难度: 中等查看答案及解析
-
下列各电离方程式中,错误的是( )
A.NaOH=Na++O2-+H+
B.Na2SO4=2Na++SO42-
C.HNO3=H++NO3-
D.MgCl2=Mg2++2Cl-难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.0.5NA个氯气分子的物质的量是0.5mol
B.32gO2所含的原子数目为NA
C.通常状况下,1NA个CO2分子占有的体积为22.4L
D.标准状况下,22.4LCO2和SO2混合气中氧原子数为0.2NA难度: 中等查看答案及解析
-
下列反应中,属于氧化还原反应且氧化剂与还原剂是不同物质的是( )
A.2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
B.SO2+Cl2+2H2O═H2SO4+2HCl
C.CaCO3+2HCl═CaCl2+CO2↑+H2O
D.2KClO3=2KCl+3O2↑难度: 中等查看答案及解析
-
某无色溶液中,可大量共存的离子组是( )
A.Na+、HCO3-、SO42-、Br--
B.Cu2+、NO3-、Cl-、SO42-
C.H+、Cl-、Na+、CO32-
D.Na+、Mg2+、SO42-、OH-难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A.稀H2SO4滴在铁片上:2Fe+6H+=2Fe3++3H2↑
B.过量的CO2通入NaOH溶液中:CO2+2OH-═CO32-+H2O
C.硫酸铜与氢氧化钡溶液混合:Cu2++2OH-=Cu(OH)2
D.氧化铜与盐酸反应:CuO+2H+=Cu2++H2O难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.1mol任何气体的体积一定是22.4L
B.在标准状况下,体积为22.4L的物质都是1mol
C.同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同
D.在非标准状况下,1mol任何气体的体积不可能是22.4L难度: 中等查看答案及解析
-
把NaHCO3和Na2CO3•10H2O混合物6.56g溶于水制成100mL溶液,测得溶液中钠离子的浓度为0.5mol/L.向该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量为( )
A.2.93g
B.5.85g
C.6.56g
D.无法确定难度: 中等查看答案及解析
-
在下列反应中,水既不是氧化剂又不是还原剂的是( )
A.F2+H2O(生成O2和HF)
B.Na+H2O
C.NaH+H2O(生成H2和NaOH)
D.Na2O2+H2O难度: 中等查看答案及解析
-
在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为( )
A.0.1mol
B.0.5mol
C.0.15mol
D.0.25mol难度: 中等查看答案及解析
-
用98%的浓硫酸(密度为1.84g/cm3)配制100mL 1 mol/L的稀硫酸.现给出下列仪器(配制过程中可能用到):①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,按使用仪器的先后顺序排列正确的是( )
A.④③⑦⑤⑥
B.②⑤⑦⑥
C.①③⑤⑥⑦
D.②⑥③⑦⑤⑥难度: 中等查看答案及解析
-
科学家发现,食用虾类等水生加壳类动物的同时服用维生素C容易中毒.这是因为对人体无害的+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化合物.下列说法中不正确的是( )
A.维生素C具有还原性
B.1mol+5价砷完全转化为+3价砷,共失去2mol电子
C.上述过程中+5价砷元素发生还原反应
D.上述过程中+5价砷类物质作为氧化剂难度: 中等查看答案及解析
-
除去NaCl中含有的Ca2+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl,加入试剂合理的操作顺序是( )
A.①②③④
B.③①②④
C.④②①③
D.③②①④难度: 中等查看答案及解析
-
硫酸越浓密度越大.现有98%的硫酸溶液的物质量浓度为C1,49%的硫酸溶液的物质量浓度为C2,则C1和C2的关系( )
A.C1=2C2
B.C1>2C2
C.C1<2C2
D.无法确定难度: 中等查看答案及解析