-
在日常生活中出现了“加碘食盐”“增铁酱油”“高钙牛奶”“富硒茶叶”“含氟牙膏”等名词,这里的碘、铁、钙、硒、氟应理解为( )
A. 元素 B. 单质 C. 分子 D. 氧化物
难度: 简单查看答案及解析
-
如图所示的实验操作中,正确的是( )。
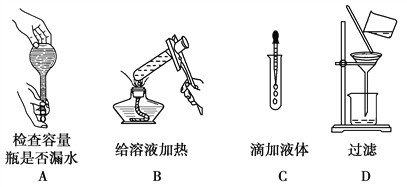
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离这三组溶液用到的方法分别是( )
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
难度: 中等查看答案及解析
-
实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )。
A. 950 mL 111.2 g B. 500 mL 117 g
C. 1 000 mL 117 g D. 任意规格 111.2 g
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数,下列说法中,正确的是( )。
A. 2.4 g金属镁所含电子数目为0.2 NA B. 16 g CH4所含原子数目为NA
C. 17 g NH3 所含原子数目为10 NA D. 18 g水所含分子数目为NA
难度: 简单查看答案及解析
-
能够直接鉴别BaCl2、NaCl、Na2CO3三种溶液的试剂是 ( )
A. AgNO3溶液 B. 稀硫酸 C. 稀盐酸 D. 稀硝酸
难度: 简单查看答案及解析
-
有一份气体样品的质量是14.2 g,体积是4.48 L(标准状况下),该气体的摩尔质量是
( )。
A. 28.4 B. 28.4 g/mol C. 71 D. 71 g/mol
难度: 简单查看答案及解析
-
粗盐中含可溶性CaCl2、MgCl2及Na2SO4,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,加入的先后顺序可以是( )。
A. ①②③④ B. ②③①④ C. ②①③④ D. ①③②④
难度: 中等查看答案及解析
-
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )。
A. 所用NaOH已吸潮 B. 向容量瓶加水时眼睛一直仰视液面
C. 有少量NaOH溶液残留在烧杯内 D. 向容量瓶加水时眼睛一直俯视液面
难度: 中等查看答案及解析
-
下列物质溶于水电离出的Cl-数目,与2mol NaCl溶于水电离出的Cl- 数目相同的是( )。
A. 1mol MgCl2 B. 2mol KClO3 C. 1mol AlCl3 D. 1.5mol CaCl2
难度: 中等查看答案及解析
-
下列溶液中的氯离子浓度与50 mL 1 mol/L的AlCl3溶液中氯离子浓度相等的是( )。
A. 150 mL 1 mol/L的NaCl B. 75 mL 1.5 mol/L的CaCl2
C. 150 mL 2 mol/L的KCl D. 75 mL 2 mol/L的NH4Cl
难度: 简单查看答案及解析
-
在5L Na2SO4溶液中含有Na+离子4.6g,则溶液中SO42-离子的物质的量浓度为( )
A. 0.2mol·L-1 B. 0.04 mol·L-1 C. 0.08 mol·L-1 D. 0.02mol·L-1
难度: 简单查看答案及解析
-
下列说法错误的是( )
A. 84g NaHCO3溶于1L水配得1 mol·L-1 NaHCO3溶液
B. 在标准状况下,44.8LHCl溶于水配成1L溶液配得2mol·L-1盐酸溶液
C. 在标准状况下,22.4L NH3溶于水配成1L溶液,浓度是1 mol·L-1;取出10mL,浓度也是1mol·L-1
D. 1mol·L-1的CaCl2溶液1L,取出100mL,含0.2mol Cl-
难度: 中等查看答案及解析
-
下列溶液中含Cl-物质的量最大的是:( )
A. 10mL 0.1mol·L-1的AlCl3溶液 B. 20mL 0.1mol·L-1的CaCl2溶液
C. 30mL 0.2mol·L-1的KCl溶液 D. 10mL 0.25mol·L-1的NaCl溶液
难度: 简单查看答案及解析
-
用胆矾(CuSO4·5H2O)配制0.1mol/L的硫酸铜溶液,下列操作中正确的是( )
A. 取25g胆矾溶于1L水中
B. 取16g胆矾溶于水配成1L溶液
C. 取25g胆矾溶于水中配成1L溶液
D. 将胆矾加热除去结晶水,再取无水硫酸铜16g溶于1L水中
难度: 中等查看答案及解析
-
在NaCl、MgCl2、MgSO4形成的混合溶液中,c(Na+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.2mol/L,则c(SO42-)为 ( )
A. 0.15 mol/L B. 0.10 mol/L C. 0.25 mol/L D. 0.20 mol/L
难度: 中等查看答案及解析
-
标准状况下,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,充入时体积如图所示,若将装置右边H2、O2的混合气体点燃引爆,活塞先左弹,恢复至原温度后,活塞右滑最终停在容器的正中央,则原来H2、O2的体积比最接近于( )
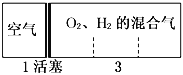
①2∶7 ②5∶4 ③4∶5 ④7∶2
A. ①② B. ②④ C. ①③ D. ③④
难度: 中等查看答案及解析