-
根据元素的核电荷数,不能确定的是
A. 原子核内质子数 B. 原子核内中子数
C. 原子最外层电子数 D. 原子核外电子数
难度: 简单查看答案及解析
-
关于化学键的下列叙述中,不正确的是 ( )
A. 离子化合物可能含共价键 B. 共价化合物一定含共价键
C. 离子化合物中只含离子键 D. 共价化合物中不含离子键
难度: 中等查看答案及解析
-
下列各组微粒中,核外电子数相等的是( )
A. Na+和Cl- B. Cl-和Ar C. Mg和Mg2+ D. S和S2-
难度: 中等查看答案及解析
-
下列互为同位素的是 ( )
A. T2O和H2O B. O3和O2 C. CO和CO2 D. 12C和13C
难度: 中等查看答案及解析
-
人类探测月球发现,在月球的土壤中含有较丰富的质量数为3的氦,它可以作为未来核聚变的重要原料之一。氦的该种同位素表示为( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列物质中,属于共价化合物的是( )
A. NH4Cl B. H2SO4 C. NaCl D. I2
难度: 中等查看答案及解析
-
下列元素的原子间不能形成离子键的是 ( )
A. 钠和氟 B. 镁和溴 C. 钙和氧 D. 氯和氧
难度: 简单查看答案及解析
-
与OH-具有相同质子数和电子数的粒子是
A. F- B. Cl- C. NH3 D. NH4+
难度: 简单查看答案及解析
-
Ca 和Ca2+ 两种微粒中,不同的是 ( )
(1) 核内质子数 (2)核外电子数 (3) 最外层电子数 (4)核外电子层数
A. (1) (2) B. (2) (3) C. (3) (4) D. (2) (3) (4)
难度: 简单查看答案及解析
-
H、D、T、H2和H+,表示( )
A. 五种不同的氢元素 B. 五种不同的氢原子
C. 五种由氢元素组成的不同微粒 D. 五种由氢元素组成的不同分子
难度: 中等查看答案及解析
-
下列叙述正确的是 ( )
A. 摩尔是物质质量的单位 B. 摩尔是物质的量的单位
C. 摩尔是物质数量的单位 D. 摩尔是一个数值
难度: 简单查看答案及解析
-
下列叙述中,错误的是 ( )
A. 1mol硫酸中含有4mol氧原子 B. 硫酸的摩尔质量是98g
C. 6.02×1023个硫酸分子的质量是98g D. 0.5mol硫酸中含有1g氢元素
难度: 中等查看答案及解析
-
在标准状况下,下列物质占体积最大的是
A. 98g H2SO4
B. 6.02×1023个氮分子
C. 44.8L HCl
D. 6g氢气
难度: 简单查看答案及解析
-
质量相等的下列各种物质中,含分子数最少的是 ( )
A. H2O B. Cl2 C. SO2 D. NO2
难度: 简单查看答案及解析
-
原子显电中性的原因是( )
A. 构成原子的各种微粒均不带电
B. 原子核外电子数大于核内质子数
C. 原子核所带电量和核外电子的电量相等,但电性相反
D. 核内质子数等于核电荷数
难度: 简单查看答案及解析
-
下列物质中,不存在化学键的是 ( )
A. 食盐 B. 氯气 C. 氦气 D. 氨气
难度: 简单查看答案及解析
-
在共价化合物中,元素化合价有正负的主要原因是 ( )
A. 电子有得失 B. 电子既有得失又有电子对偏移
C. 共用电子对有偏移 D. 有金属元素的存在
难度: 简单查看答案及解析
-
在100mL0.1mol·L-1的NaOH溶液中,所含的NaOH的质量为
A.40g B.4g
C.0.4g D.0.04g
难度: 中等查看答案及解析
-
根据化学反应的实质是旧键断裂、新键形成这一观点,下列变化不属于化学反应的是( )
A. 干冰气化 B. 氧气转化成臭氧
C. 二氧化碳溶于水 D. 加热碳酸氢铵
难度: 简单查看答案及解析
-
某元素一价阴离子,核外电子数是18,其原子的质量数是35,则核内中子数与质子数之差 ( )
A. 1 B. 0 C. 35 D. 17
难度: 简单查看答案及解析
-
下列各组原子序数所表示的两种元素,能形成AB2型离子化合物的是( )
A. 6和8 B. 11和13 C. 11和16 D. 12和17
难度: 中等查看答案及解析
-
下列关于1.0mol·L-1的NaCl溶液说法正确的是 ( )
A. 溶液中含1mol NaCl B. 1L溶液中含58.5克NaCl
C. 1mol NaCl溶于1L水中 D. 58.5克NaCl溶于941.5克水中
难度: 简单查看答案及解析
-
下列物质中,不属于共价分子的是 ( )
A. MgO B. HCl C. CCl4 D. H2
难度: 简单查看答案及解析
-
同温同压下,下列气体的密度最大的是( )
A. F2 B. Cl2 C. HCl D. CO2
难度: 简单查看答案及解析
-
标准状况下,5.6L氯化氢溶于水得到0.5L盐酸,其物质的量浓度为( )
A. 0.5 g/L B. 0.5 g C. 0.5 mol/L D. 5.6 mol/L
难度: 简单查看答案及解析
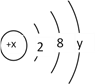 ,试回答:
,试回答: